第九章Web Topic
Web Topic 9.1 分光光度法原理
我们对光合作用装置的大部分了解都是通过光谱学获得的——即测量光与分子相互作用的技术。分光光度法是光谱学的一个重要分支,专注于测量技术。这里我们将探讨四个主题:比尔定律、吸光度的测量、作用光谱和差示光谱。
比尔定律
对于任何分子物种而言,一个基本信息是其存在的数量。浓度的定量测量是生物科学的基石之一。在所有已设计的浓度测量方法中,应用最广泛的是吸收分光光度法。关于吸收分光光度法经典方法的综述可参见 Blankenship (2002)。在该技术中,测量样品在特定波长下吸收的光量,并通过与适当的标准品或参考数据进行比较来确定样品的浓度。光吸收最有用的度量是吸光度(A),通常也称为光密度(OD),后者应避免使用,除非存在主要的光散射组分,例如在细菌悬浮液中(网络图 9.1.A)。吸光度定义为A= logI0/I,其中I0是入射到样品上的光强度,I是样品透射的光强度。
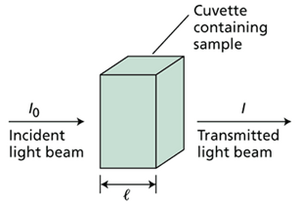
样品的吸光度可以通过比色定律与吸光物质的浓度相关联:
A = ε×c×l
其中,c 是浓度,通常以摩尔每升为单位;l 是光程长度,通常为 1 厘米;ε 是一个比例常数,称为摩尔消光系数,单位为升每摩尔每厘米。ε 的值是待测化合物和波长的函数。叶绿素在蓝光和红光区域(它们吸收最强的区域)的 ε 值通常约为 100,000 L mol⁻¹ cm⁻¹,但在绿光区域则低得多。当复杂混合物中有不止一种组分在给定波长下吸光时,各个组分产生的吸光度通常是加和的。
分光光度计
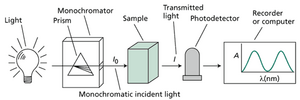
吸光度由称为分光光度计的仪器测量(网络图 9.1.B)。分光光度计的基本组成部分包括光源、波长选择装置(如单色仪或滤光片)、样品室、光检测器、读数装置以及用于存储和分析光谱的计算机。最有用的仪器可以扫描照射到样品上的入射光波长,并输出吸光度随波长变化的光谱图,如教科书图 9.7 所示。
作用光谱
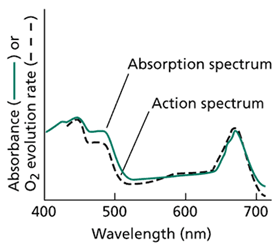
作用光谱的应用对于我们目前理解光合作用的发展至关重要。作用光谱是一种图表,表示观察到的生物效应大小随波长变化的函数关系。作用光谱所测量的效应例子包括氧气释放(网络图 9.1.C,即教科书图 9.8)以及由光敏色素作用引起的激素生长响应(参见教科书第 16 章)。通常,作用光谱可以识别出引起特定光诱导现象的发色团。作用光谱在发现产氧光合生物中两个光系统的存在方面起到了关键作用。
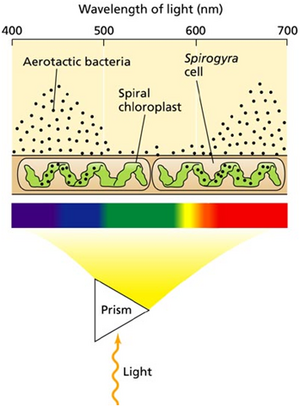
最早的一些作用光谱是由 T. W. Engelmann 在 19 世纪末测量的(网络图 9.1.D)。Engelmann 使用棱镜将太阳光色散成彩虹,让其照射到水生藻丝上。系统中引入了寻求氧气的细菌群体。细菌聚集在释放氧气最多的藻丝区域。这些区域正是被蓝光和红光照射的区域,而叶绿素对这些光吸收强烈。如今,作用光谱可以在房间大小的摄谱仪中测量,科学家进入一个巨大的单色仪,并将待辐照的样品放置在充满单色光的大房间区域内。但实验原理与 Engelmann 的实验相同。
差示光谱
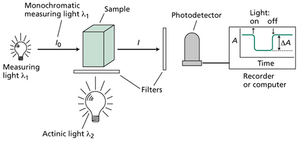
光合作用研究中的一项重要技术是光诱导差示光谱法,它测量吸光度的变化(网络图 9.1.E)。在该技术中,使用明亮的、常称为光化光(个人译名,actinic light)的光照射样品,同时使用一束微弱的光来测量样品在非光化光波长下的吸光度。通过这种方式获得差示光谱(difference spectrum),它代表了样品在光化光照射下吸收光谱的变化。光照后消失的吸收带显示为负峰;光照后新出现的吸收带显示为正峰。差示光谱为识别参与光合作用光反应的分子种类提供了重要线索。P700(一种吸收波长 700 纳米光的叶绿素,见教科书图 9.18)光氧化的差示光谱如网络图 9.1.F 所示。
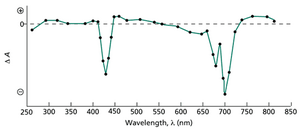
通过使用极快的光闪光激发光合作用,并用另一束光测量吸光度变化,可以在闪光激发后的给定时间记录差示光谱。测量光束通常是单色的,意味着其波长范围很窄。
当测量光束的波长处于能够激发光化学反应的范围内时,它必须比激发光弱得多,以防止其自身激发大量的光化学反应。
在某些情况下,以固定的时间间隔连续测量透射光。首先在黑暗中测量基线,然后进行闪光激发,从而在一系列时间尺度上观察透射率的变化。可以用不同的单色测量光束重复该实验。结合这些数据,既可以观察任一波长处随时间的变化,也可以观察任一时间点发生的总变化。在某些情况下,测量光束可以包含更宽的波长范围,这些光在通过样品后被分离开,并使用一组光检测器分别进行测量。这种方法允许同时记录多个波长下的吸光度变化。
在其他情况下,称为脉冲-探测实验,激发光和测量光都以短脉冲形式给出,并且在激发脉冲和测量脉冲之间存在延迟。这种方法具有的优势是,使用超短激光脉冲和光学延迟线可以获得极高的时间分辨率,延迟线通过改变激发脉冲和测量脉冲各自在空间中传播的距离来调整它们到达的延迟时间。两个脉冲传播距离相差 30 厘米约等于 1 纳秒(10⁻⁹ 秒)。这些技术可以具有极高的时间分辨率,在某些情况下可达皮秒(10⁻¹² 秒)甚至飞秒(10⁻¹⁵ 秒),并为光合能量储存过程的最早期事件提供了深刻的见解。在如此短的时间尺度上进行测量有助于理解光捕获和电子转移的初始反应,但在更长时间尺度上发生的过程也很重要,并且需要一套不同的仪器来测量这些较慢的现象。
无论如何,在闪光激发后不同时间记录的多个差示光谱可用于构建随时间变化的光合作用过程的复合光谱。差示光谱的形状可用于识别所涉及的化学物种,从而可以对过程步骤进行建模。
参考文献
Blankenship, R. E. (2002) Molecular Mechanisms of Photosynthesis, Blackwell Scientific, Oxford, pp. 295–317.
Ke, B. (1973) The primary electron acceptor of photosystem I. Biochim. Biophys. Acta 301: 1–33.
Web Topic 9.2 叶绿素及其他光合色素的分布
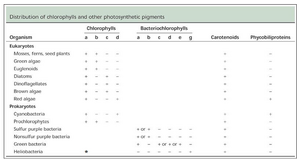
参考文献
Some reviews on the biosynthesis of chlorophylls and related pigments:
Chew, A. G. M., and Bryant, D. A. (2007) Chlorophyll biosynthesis in bacteria: The origins of structural and functional diversity.Annu. Rev. Microbiol. 61: 113–129.
Qiu, N. W., Jiang, D. C., Wang, X. S., Wang, B. S., and Zhou F. (2019) Advances in the Members and Biosynthesis of Chlorophyll Family.Photosynthetica57(4): 974–984.
Saer, R. G. and Blankenship, R. E. (2017) Light-harvesting in phototrophic bacteria: structure and function.Biochem. J.474: 2107–2131.
Recent reviews and insights on chlorophylls d and f:
Bryant, D. A., Shen, G., Turner, G. M., Soulier, N., Laremore, T. N., and Ho, M-Y. (2020) "Far-Red Light Allophycocyanin Subunits Play a Role in Chlorophyll D Accumulation in Far-Red Light."Photosynthesis Research143: 81–95.
Chen, M., and Blankenship R. E. (2011) Expanding the solar spectrum used by photosynthesis.Trends Plant Sci. 16: 427–431.
Larkum, A. W. D., Ritchie, R. J., and Raven, J. A. (2018) Living off the Sun: chlorophylls, bacteriochlorophylls and rhodopsins.Photosynthetica56: 11–43.
Mascoli, V., Bersanini, L., and Croce, R. (2020) Far-Red Absorption and Light-Use Efficiency Trade-Offs in Chlorophyll F Photosynthesis.Nature Plants6(8): 1044–1053.
Review on green bacterial chlorosomes
Oostergetel, G. T., van Amerongen, H., and Boekema, E. J. (2010) The chlorosome: a prototype for efficient light harvesting in photosynthesis.Photosynthesis Research104: 245–255.
A recent review on Heliobacteria and their unique chlorophylls:
Orf, G. S., and K. E. Redding. 2021. "Photosynthesis | The Heliobacteria."Encyclopedia of Biological Chemistry III. https://doi.org/10.1016/b978-0-12-819460-7.00220-6.
Web Topic 9.3 量子产额
一个过程中分子释放其激发能(或“衰变”)的量子产额(Φ)是指通过该途径衰变的激发态分子所占的比例(Clayton 1971, 1980)。从数学上讲,一个过程(如光化学反应)的量子产额定义如下:
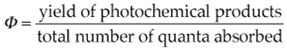
特定过程的Φ值范围可以从0(如果该过程从未参与激发态的衰变)到1.0(如果该过程总是使激发态失活)。所有可能过程的量子产额之和为1.0。
在弱光下保存的功能性叶绿体中,光化学反应的量子产额约为0.95,荧光的量子产额为0.05或更低,其他过程的量子产额可以忽略不计。因此,大多数激发的叶绿素分子会导致光化学反应。
光合作用产物(如O2)形成的量子产额可以相当精确地测量。在这种情况下,量子产额大大低于光化学反应的数值,因为在任何O2分子形成之前,必须发生多次光化学事件。对于O2的产生,测得的最大量子产额约为0.1,这意味着每释放一个O2分子需要吸收10个光量子。量子产额的倒数称为量子需要量。因此,O2释放的最小量子需要量约为10(见教材图9.11)。对光的吸收以及光中所含能量去向的定量测量对于理解光合作用至关重要。
参考文献
Clayton, R. K. (1971)Light and Living Matter: A Guide to the Study of Photobiology. McGraw-Hill, New York.
Clayton, R. K. (1980)Photosynthesis: Physical Mechanisms and Chemical Patterns. Cambridge University Press, Cambridge.
Web Topic 9.4 光对细胞色素氧化的拮抗效应
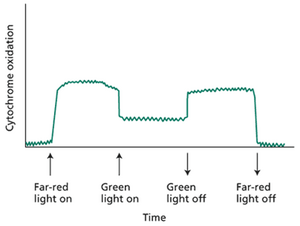
荷兰的Louis Duysens进行的实验解释了令人困惑的红降效应和增益效应(Duysens等,1961)。他提出,两个光化学事件导致了增益效应。一个光化学事件产生氧化作用,而另一个产生还原作用。叶绿体含有细胞色素,这是一类含铁蛋白质,在光合作用中作为中间电子载体发挥作用(见教材图9.19)。Duysens发现,当用长波长的光照射红藻样品时,细胞色素大部分被氧化。如果也存在较短波长的光,则该效应被部分逆转(网络图9.4.A)。这些拮抗效应可以通过一个涉及两个光化学事件的机制来解释:一个倾向于氧化细胞色素,另一个倾向于还原它(Hill和Bendall 1960)。
我们现在知道,在光谱的红色区域,被称为光系统I(PS-I)的一个光反应优先吸收波长大于680 nm的远红光,而被称为光系统II(PS-II)的第二个光反应能很好地吸收680 nm的红光,但很难被远红光驱动。这种波长依赖性解释了增益效应和红降效应。两个光系统之间的另一个区别是,光系统I产生一种强还原剂(能够还原NADP+)和一种弱氧化剂。光系统II产生一种非常强的氧化剂(能够氧化水),以及一种比光系统I产生的还原剂弱的还原剂。光系统II的这个还原剂重新还原了光系统I产生的氧化剂(见教材图9.12),这就解释了拮抗效应。
参考文献
Duysens, L. N. M., Amesz, J., 和 Kamp, B. M. (1961) 光合作用中的两个光化学系统。Nature 190: 510–511.
Hill, R., 和 Bendall, F. (1960) 叶绿体中两种细胞色素组分的功能:一个工作假说。Nature 186: 136–137.
Web Topic 9.5 两种细菌反应中心的结构
1984年,慕尼黑的Hartmut Michel、Johann Deisenhofer、Robert Huber及其同事解析了紫色光合细菌 Rhodopseudomonas viridis 反应中心的三维结构(Deisenhofer和Michel 1989)。这项里程碑式的成就(于1988年获得诺贝尔奖)是首次对整合膜蛋白进行高分辨率X射线结构解析,也是首次解析反应中心复合物的结构。该结构如网络图9.5.A所示。
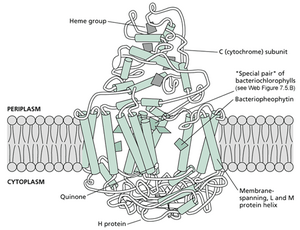
该复合物的蛋白质部分由四个独立的多肽组成。其中两个多肽称为L和M(代表轻链和中链),它们结合了复合物中所有的细菌叶绿素、醌和类胡萝卜素辅助因子。该结构关于垂直于膜平面的轴具有双重对称性,暗示了反应中心的二聚体性质。L和M肽的十个跨膜部分(各五个)以α-螺旋排列,并且在膜内部几乎没有带电荷的氨基酸残基。H(重链)蛋白具有单个跨膜螺旋,主要定位于膜的细胞质侧。C(细胞色素)亚单位位于周质区域(细菌质膜与外膜之间的区域)。色素和醌(电子受体)的几何排列如网络图9.5.B所示,图中移除了蛋白质。在另一种紫色光合细菌 Rhodobacter sphaeroides 的反应中心中也发现了类似的排列,只是不存在C亚基。
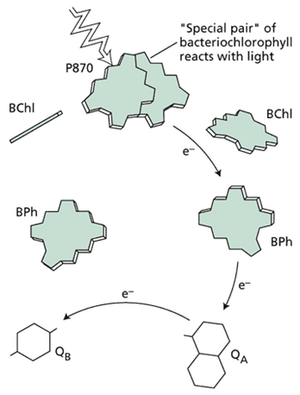
两个细菌叶绿素分子彼此紧密接触,被称为特殊对。这个二聚体(其存在通过核磁共振研究预测到)是复合物的光活化部分。电子从这个二聚体沿着复合物右侧的电子载体序列转移。对这些结构的详细分析,以及对众多突变体的分析,揭示了所有反应中心所执行的能量储存过程中涉及的许多基本过程。
人们认为细菌反应中心的结构在许多方面类似于产氧生物的光系统II中发现的结构,尤其是在链的电子受体部分(见教材图9.21)。构成细菌反应中心核心的蛋白质在序列上与其光系统II的对应物相对相似,这暗示了进化上的关联性。
参考文献
Deisenhofer, J., and Michel, H. (1989) The photosynthetic reaction center from the purple bacterium Rhodopseudomonas viridis. Science 245: 1463–1473.
Web Topic 9.6 中点电位与氧化还原反应
光合作用和呼吸作用涉及还原剂和氧化剂之间的电子转移。了解这些过程的热力学对于理解这些生物化学电子传递过程(例如在线粒体(第13章)和叶绿体(第9章)中发现的过程)的能量学和途径至关重要。
氧化还原反应、中点电位及其与热力学定律的关系在网络附录1中讨论,其中介绍了化学反应自由能变化(ΔG)的概念。
电子转移反应是光合作用(和呼吸作用)的核心,因此理解一些特定的概念和术语非常重要。
氧化还原反应遵循相同的热力学规则,但由于电子可以按不同的化学计量在分子之间转移,并且因为电子的电位可以直接使用电极测量,所以自由能电位的术语和单位是不同的。
氧化还原中点电位(Em)是衡量氧化还原对从其他化合物获取电子的倾向的指标。Em类似于在生理条件下测得的反应标准自由能(ΔG0')。
氧化还原对是一对相差一个或多个电子的物种(即具有氧化型和还原型)。Em是标准电极(具有特定电压)与该氧化还原对在处于氧化和还原中间状态(即一半氧化,一半还原)时测量到的电压。具体操作方法描述如下。
较大的正中点电位意味着该化合物是强氧化剂;较大的负值意味着该化合物是强还原剂。
Em类似于在生理条件下测定的反应标准自由能(ΔG0';参见网络附录1),但重要的是,它以电位(V)为单位,而非每摩尔的能量。因此,就像利用自由能变化一样,人们可以利用中点电位来估计反应的方向性以及反应发生时释放(或吸收)的能量大小。在这种情况下,需考虑从电子供体对到电子受体对的中点电位差,从而估算出自由能的变化为 ΔEm = Em(受体) - Em(供体)。
Em值可以很容易地通过法拉第常数,并考虑反应中涉及的电子数,与反应的标准自由能(ΔG')联系起来。然而,ΔG 和 ΔEm 之间存在两个重要区别。首先,Em值以电位(V)为单位。由于电子能量越高,电压越负,所以一个自发反应将具有负的自由能变化 ΔG,但却是正的 ΔEm。其次,一个反应可能涉及不止一个电子,因此 ΔEm 的变化必须乘以每个反应物的电子数。以下提供了一个方便的转换公式:
ΔG = nFΔEm
其中 n 是反应中交换的电子的摩尔数,F 是法拉第常数,可以表示为以 kJ 为单位给出 ΔG(96.485 kJ 伏特⁻¹ 摩尔⁻¹)。由此,可以清楚地看出,平衡常数也可以从中点电位预测,其方式与自由能同平衡常数的关联方式相同(参见网络附录1,公式 A1.14)。
许多化学和生化反应的中点电位已被测量并制成表格。教科书图 9.18 中的 Z 方案的 y 轴显示了电子载体的中点电位,负值高于正值。这种选择使得自发(释放自由能)的反应在图表上呈现为"下坡",但请注意,更高的能量状态具有更负的 Em。
电化学家(研究氧化还原反应的化学家)为了方便可以使用不同的标准电极。这些标准电极具有不同的标准氧化还原电位,会使测量的中点电位发生偏移。为了比较不同测量中的数值,通常会对测量值进行校正,以反映使用"标准氢电极"时会获得的值。请注意,Em 值总是会因标准电极的电压而发生偏移(亦见下文),但在计算 ΔEm 时,这种偏移会相互抵消。
阅读科学论文时,可能会遇到中点电位的不同名称,这可能会引起一些混淆。在标准化学条件下(反应物和产物浓度为 1M,pH 0,压力 1 大气压,温度 0°C),Em 被称为 E0,但这样的条件是非生理性的。在特定的生理条件下,经常使用术语 E0'。在这里,我们交替使用 Em 和 E0'。
必须注意,Em 只能针对一个氧化还原对来定义;单个物质的 Em 是未定义的。如果我们考虑光系统 II 中的初级叶绿素供体 P680 的例子,其原因就很明显了。该物质可以以其还原态 P680 或其氧化态 P680⁺ 存在。P680/P680⁺ 对的中点电位非常高,这意味着它作为一种强氧化剂,这对于水的氧化至关重要。当 P680 叶绿素对被光化学激发时,会得到一个非常不同的 Em。在这种情况下,该对将是 P680*/P680⁺,其电位非常负,这意味着它倾向于提供电子,这对于光系统 II 中导致脱镁叶绿素和 QA 还原的初始电子转移反应至关重要(教科书图 9.18)。
如果质子参与氧化还原反应(例如,在 O₂ 还原为 2 H₂O 的过程中伴随吸收 4 H⁺),则中点电位将取决于 pH 值,Em 通常在下标中带有附加项来表示(例如,Em,7 表示 pH 7 时的中点电位)。重要的一点是,物质 P680⁺ 出现在两个对中,但每一对都具有非常不同的氧化还原特性。
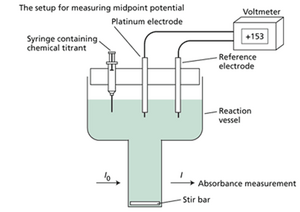
研究人员通常通过进行氧化还原滴定来估算氧化还原电位(Dutton 1978)。他们通常通过添加少量氧化剂或还原剂,将样品调控(或称“平衡”)在特定的氧化还原电位。必须包含氧化还原介体,即允许样品与测量系统电极之间快速平衡的小分子,以确保测量时系统处于平衡状态。在一系列氧化还原电位下进行多次测量。样品在包含铂电极和参比电极的特殊电解池中搅拌,并加入化学氧化剂和还原剂来调整氧化还原电位,该电位由伏特计读取(网络图 9.6.A)。
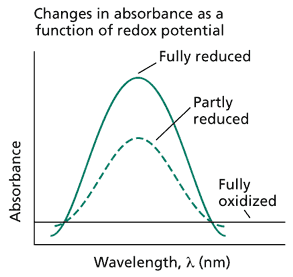
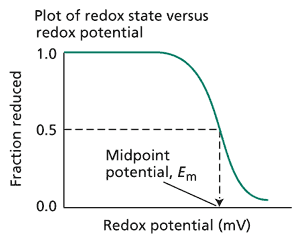
通过在每个电位下测量样品的特定性质(通常是吸光度),可以跟踪氧化还原反应的程度。在网络图 9.6.B 所示的例子中,该化合物的还原形式具有吸光度,且随着化合物被氧化,其吸光度降低。每个电位下的还原形式分数被绘制出来与氧化还原电位对应,中点电位 (Em) 被确定为该化合物一半被氧化、一半被还原时的电位(网络图 9.6.C)。
参考文献
Dutton, P. L. (1978) Redox potentiometry: Determination of midpoint potentials of oxidation-reduction components of biological electron-transfer systems. Methods Enzymol. 54: 411–435.
Web Topic 9.7 氧气释放
光合作用水氧化的化学机制一直是大量研究的主题。考虑到这个反应对地球生命有多么重要,这并不奇怪!近期工作的快速进展使人们在分子生物物理水平上达到了惊人的理解程度。这需要开发复杂的工具,包括以前所未有的细节水平和在催化循环的不同阶段解析光系统 II 的结构。
有趣的是,几十年前,基于相对简单的实验,建立了氧气释放的基本模型。这些实验易于理解,并且至今仍是更详细、被普遍接受的模型的基础。
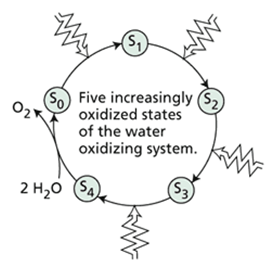
基础实验由皮埃尔·约利奥在20世纪60年代首次完成,方法是将一份绿藻样本暴露于一系列"饱和、单周转"的闪光中。这些闪光非常强烈,因此能激发样本中几乎每一个光系统II(PSII)中心;同时闪光也非常短暂,因此每个中心只能进行一次周转。这样,每次闪光(或多或少)同步地使PSII中心向前推进一步。然后使用灵敏电极测量样本释放的O₂量。当样本起始于暗适应状态时,O₂的出现表现出依赖于闪光次数的特征性规律。前两次闪光产生很少或不产生氧气,第三次闪光释放大量氧气,第四次闪光释放较少。这种模式不断重复,因此在每四次闪光时观察到一个氧气释放的峰值。科克及其同事(Kok et al. 1970)对这些观察结果进行了解释,并提出了一个称为S态机制的模型。该模型包含五个状态的序列,称为S₀到S₄,它们代表水氧化酶系统(或称放氧复合体)逐渐氧化的形式(网络图9.7.A)。
在黑暗中,系统主要弛豫到S₁状态。闪光使系统从一个S状态前进到下一个状态,从S₁到S₂到S₃,直到达到S₄状态。S₄状态极不稳定,无需进一步的光输入即可产生O₂,并使系统返回到S₀。因此,第一次O₂将出现在三次推进(即三次约利奥闪光)之后。下一次O₂在经过四轮循环、四次闪光后产生,依此类推。偶尔,一个中心在闪光激发后未能前进到下一个S状态("脱漏"),而一个中心被单次闪光激发两次的情况则更为少见("双命中")。这些脱漏和双命中导致系统受到阻尼,因此最终每个后续闪光大约每四个PSII中心产生一个O₂,并且O₂产率的振荡消失。在这些条件下,S₀、S₁、S₂和S₃状态将大致均匀分布。如果将样本随后置于黑暗中,不稳定的S₂和S₃状态将弛豫到S₁状态,而稳定的S₀状态将保持不变。几分钟后,约75%的放氧复合体将处于S₁状态,其余的处于S₀状态。这种状态分布解释了为什么在给暗适应的叶绿体一系列闪光时,第三次闪光后观察到最大的O₂产额。
这个S态机制解释了观察到的O₂释放模式,但并未解释S状态的化学本质,也没有说明是否形成了任何部分氧化的中间体,例如H₂O₂。通过测量随着闪光推进S态时质子释放的模式(参见教材公式9.8),获得了更多信息。除了氧气,氢离子(质子,H⁺)也是水氧化的产物,并有助于形成驱动ATP合成的质子驱动力。
参考文献
Kok, B., Forbush, B., and McGloin, M. (1970) Cooperation of charges in photosynthetic O2evolution. I. A linear four step mechanism.Photochem. Photobiol. 11: 457–475.
Web Topic 9.8 光系统 I
植物光系统I(PSI)是自然界中最复杂的膜复合体之一。它包含两个复合体:一个反应中心和一个光捕获复合体(LHC),它们共同形成PSI-LHC超级复合体(Caspy and Nelson 2018)。PSI反应中心由一个多蛋白复合体组成,该复合体至少有14个蛋白亚基(按照绿色植物命名法为PsaA–PsaL、PsaN和PsaO)。PsaA和PsaB是最大的亚基;它们高度同源,是由基因复制形成的(Gisriel et al. 2017)。反应中心叶绿素P700和大约100个核心天线叶绿素结合在PsaA和PsaB这两个蛋白上,它们的分子量在66至70 kDa之间(Krauss et al. 1993, 1996; Jordan et al. 2001; Mazor et al. 2017)。已从多种生物(植物、藻类和蓝细菌)中分离出PS-I反应中心复合体,发现其含有PsaA和PsaB蛋白,以及数量不等的、分子量在4至25 kDa之间的较小蛋白质(参见教材图9.26)。PsaD和PsaE作为可溶性电子载体铁氧还蛋白的结合位点,而PsaF和PsaN对于与腔体电子供体质体蓝素的相互作用很重要。PsaH、PsaL和PsaO参与LHCII的动态结合,以平衡PSI和PSII之间的激发能传递。而PSI的主要天线LHCI则通过PsaK和PsaG与PSI结合(Jensen et al., 2007)。PsaC是一个8 kDa的蛋白质,含有一些作为光系统I中早期电子受体的结合态铁硫中心。来自植物的PSI复合体结构已被高分辨率解析,所有叶绿素和电子传递组分的位置都已确定(Krauss et al. 1996; Schubert et al. 1997; Jordan et al. 2001; Nelson and Ben-Shem 2004; Mazor et al. 2017; Caspy et al. 2020; 参见教材图9.26)。
初级电子供体P700是一个叶绿素对,在被光激发后,会将一个电子转移给附近的受体,也称为电子载体。在还原形式下,作用于光系统I受体区域的电子载体都是极强的还原剂。这些还原态物质极不稳定,因此难以鉴定(即测量)。有证据表明,这些早期受体之一是一个叶绿素分子(A₀),另一个是醌类物质,叶绿醌(A₁),也称为维生素K₁(Nugent 1996)。
其他的电子受体包括一系列三个膜结合的铁硫蛋白,或称为结合态铁氧还蛋白,也称为Fe–S中心 Fe–SX、Fe–SA 和 Fe–SB。Fe–S中心 Fe–SX 是P700结合蛋白的一部分;Fe–SA 和 Fe–SB 中心位于作为PSI反应中心复合体一部分的8 kDa PsaC蛋白上。电子通过Fe–SA 和 Fe–SB 中心转移到铁氧还蛋白,后者是一种小的水溶性铁硫蛋白。膜结合的黄素蛋白铁氧还蛋白–NADP还原酶(FNR)将NADP⁺还原为NADPH,从而完成了起始于PSII处水氧化的非循环电子传递序列(Karplus et al. 1991)。
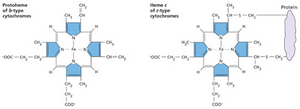
从PSII到PSI的电子传递由质体氢醌、细胞色素b6f复合体和质体蓝素介导(见教材图9.19)。细胞色素b6f复合体包含两个b型血红素和一个c型血红素(网络图9.8.A)。
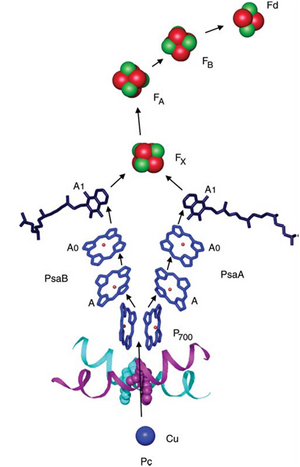
PSI中电子载体组织的模型如网络图9.8.B所示。P700二聚体位于结构底部,两条对称臂从P700向外辐射(Malkin和Niyogi 2000)。每条臂包含一个辅助叶绿素a和另一个暂定为A0的叶绿素分子。其他结构包括Fe-S中心FX,以及另外两个Fe-S中心F1和F2。
PSI反应中心在功能上与厌氧绿色硫细菌和螺旋菌中发现的反応中心有一些相似之处。这些细菌含有低电位的Fe-S中心作为早期电子受体,并且可能能够进行类似于光系统I还原NADP+的、由铁氧还蛋白介导的NAD+还原。这些复合体与产氧生物的光系统I之间几乎肯定存在进化关系。
参考文献
Caspy, I. 和 Nelson, N. (2017). Structure of the plant photosystem I. Biochemical Society Transactions 46: 285–294.
Caspy, I., Borovikova-Sheinker, A., Klaiman, D., Shkolnisky, Y. 和 Nelson, N. (2020). The structure of a triple complex of plant photosystem I with ferredoxin and plastocyanin. Nat Plants 6: 1300–1305.
Gisriel, C., Sarrou, I., Ferlez, B., Golbeck, J.H., Redding, K.E. 和 Fromme, R. (2017) Structure of a symmetric photosynthetic reaction center–photosystem. Science 357: 1021–1025
Jensen, P.E., Bassi, R., Boekema, E.J., Dekker, J.P., Jansson, S., Leister, D., Robinson, C. 和 Scheller, H.V. (2007). Structure, function and regulation of plant photosystem I. Biochim. Biophys. Acta. 1767: 335–352.
Jordan, P., Fromme, P., Witt, H.T., Klukas, O., Saenger, W., 和 Krauss, N. (2001) Three-dimensional structure of cyanobacterial photosystem I at 2.5 Å resolution. Nature. 411: 909–917.
Karplus, P. A., Daniels, M. J., 和 Herriott, J. R. (1991) Atomic structure of ferredoxin-NADP+ reductase: Prototype for a structurally novel flavoenzyme family. Science 251: 60–66.
Krauss, N., Hinrichs, W., Witt, I., Fromme, P., Pritzkow, W., Dauter, Z., Betzel, C., Wilson, K. S., Witt, H. T., 和 Saenger, W. (1993) Three-dimensional structure of system I of photosynthesis at 6 Å resolution. Nature 361: 326–331.
Krauss, N., Schubert, W-D., Klukas, O., Fromme, P., Witt, H. T., 和 Saenger, W. (1996) Photosystem I at 4 Å resolution represents the first structural model of a joint photosynthetic reaction centre and core antenna system. Nature Struct. Biol. 3: 965–973.
Malkin, R. 和 Niyogi, K. (2000) Photosynthesis. In: Buchanan, B. B., Gruissem, W., and Jones, R., eds. (2000) Biochemistry and Molecular Biology of Plants. American Society of Plant Physiologists, Rockville, MD, pp. 575–577.
Mazor, Y., Borovikova, A., Caspy, I. 和 Nelson, N. (2017). Structure of the plant photosystem I supercomplex at 2.6 Å resolution. Nature Plants 3: 17014.
Nelson, N. 和 Ben-Shem, A. (2004) The complex architecture of oxygenic photosynthesis. Nature Rev. Mol. Cell Biol. 5: 971–982.
Nelson, N. 和 Yocum, C.F. 2006. Structure and Function of Photosystems I and II. Annu. Rev. Plant Biol. 57, 521–565.
Nugent, J. H. A. (1996) Oxygenic photosynthesis: Electron transfer in photosystem I and photosystem II. Eur. J. Biochem. 237: 519–531.
Schubert, W. D., Klukas, O., Krauss, N., Saenger, W., Fromme, P., 和 Witt, H. T. (1997) Photosystem I of Synechococcus elongatus at 4 angstrom resolution: Comprehensive structure analysis. J. Molec. Biol. 272: 741–769.
Web Topic 9.9 ATP合酶
在光合作用和氧化磷酸化过程中,ATP的合成机制由保罗·博耶(Paul Boyer)提出(Boyer 1993, 1997),并通过一系列生化和结构研究进一步详细阐明,其中包括1997年获得诺贝尔奖的突破性结构研究(获奖者为保罗·D·博耶和约翰·E·沃克)。
如第9章所述,光合作用的光反应在类囊体膜两侧产生质子动力势(PMF)。ATP合成是由(或偶联于)该PMF驱动的质子流驱动的。该机制在许多综述中已有详细描述(例如Boyer 1999),它涉及两个不同的亚复合体,称为CF0和CF1。请注意,相同的基本机制和结构也适用于线粒体和细菌的ATP合酶,它们通常表示为F0和F1(不带“C”)。
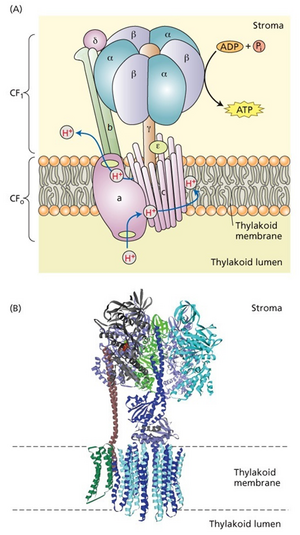
CF0是一个跨膜复合体,由亚基a、b和c组成(网络图9.9.A)。跨膜c亚基形成一个环,在膜的疏水跨膜区含有可质子化的氨基酸残基。a亚基与该环结合,允许质子从膜的两侧传递到可质子化残基。质子完全穿过类囊体的运动在c亚基环和a亚基之间产生旋转运动(和扭矩;见网络图9.9.A)。如下所述,b亚基将CF0连接到CF1的不同点上。
CF1 是基质侧表面的亲水片段(参见网络图 9.9.A),由两个大亚基 α 和 β,以及三个较小亚基 γ、δ 和 ε 组成。每个 CF1 分子包含三个 α 亚基和 β 亚基的拷贝,以及一个 γ、δ 和 ε 亚基的拷贝。α-和 β-亚基形成一个环状异源六聚体(三个 α- 和三个 β- 亚基)。β-亚基结合 ADP 和磷酸,并催化 ADP 磷酸化为 ATP。
CF0 产生的扭矩通过连接 CF0 和 CF1 的两个亚基的组合传递到 CF1 亚复合体:γ 亚基(连接 CF0 c-环到 α–β 六聚体的中心)以及 b-亚基(连接 a-亚基到 α–β 六聚体并充当“定子”,防止整个 CF1 复合体自由旋转)。这样,γ-亚基的旋转引起 α–β 的机械变形,导致 CF1 上的核苷酸结合位点发生变化(Noji 等人,1997),其作用方式与内燃机中的凸轮轴非常相似(参见Web Topic 13.4)。
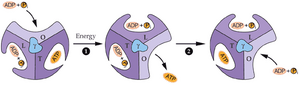
Paul Boyer 在 1997 年提出了 CF0 旋转导致的机械变形如何实现 ATP 合成作用的机制。在这个结合变化机制中(网络图 9.9.B),质子跨膜转移施加并通过 γ 和 b 亚基传递的机械能,用于形成和变形 β 亚基,从而使它们交替形成一个相对于 ADP 和 Pi 的结合,能松散或非常紧密地结合 ATP 的口袋。紧密结合在热力学上稳定 ATP 胜过 ADP 和 Pi,从而允许 ATP 形成。通过扭曲结合位点(即机械变形它)来释放紧密结合的 ATP 需要加入能量。此过程在网络图 9.9.B 中有更详细的展示。CF1 在其 β 亚基上有三个核苷酸结合位点,但它们的特性取决于 γ-亚基的取向,形成称为 L、T 和 O(分别代表松散、紧密和开放)的不同位点。推测 ADP 和无机磷酸首先结合到 L 位点。γ-亚基的运动将 O 位点转变为 T 位点,有利于 ATP 的形成。γ 亚基的进一步旋转将 T 位点转换为 O,释放形成的 ATP。
对 CF1 γ-亚基旋转的直接观察为结合变化机制提供了强有力的实验支持(Yasuda 等人,2001)。
ATP 合酶产生的 ATP 化学计量在不同物种中是不同的。每个 CF1(或 F1)亚复合体有三个 β 亚基拷贝,因此 γ-亚基完整的 360 度旋转应该产生 3 个 ATP 分子。
据认为,需要一个质子来使 c-环移动一个 c-亚基。已经证明,不同物种的 c-环中 c-亚基的数量不同,因此需要不同数量的质子跨膜转移来实现 γ-亚基的完整旋转。已发现不同物种每个环有 8 到 17 个 c-亚基(Cheuk and Meier 2021)。这种化学计量的变化将改变光反应期间每还原一分子 NADPH 所产生的 ATP 的比例,以及维持这些过程所需的质子动力(PMF)。c-环越小,制造 ATP 所需的质子越少,但驱动该过程所需的 PMF 越高,类似于改变汽车或自行车的齿轮。
已发现维管植物的叶绿体每个 c-环有 14 个亚基,导致每产生 3 个 ATP 需要 14 个 H+ 跨膜转移,即 4.666 H+/ATP。这意味着从水到 NADPH 的线性电子流应产出 2.67 ATP/2 NADPH 的比例,低于支持卡尔文-本森循环所需的 3/2 比例,需要从循环电子流等过程获得额外的 ATP(参见教材图 9.16B)。因此,高 c-亚基化学计量可能看起来效率低下,但有人提出这是为了防止形成非常大的 PMF 所必需的,否则会使膜过度激发能量,引起光损伤(Davis and Kramer 2020)。
参考文献
Boyer, P. D. (1993) The binding change mechanism for ATP synthase—Some probabilities and possibilities. Biochim. Biophys. Acta 1140: 215–250.
Boyer, P. D. (1997) The ATP synthase—A splendid molecular machine. Annu. Rev. Biochem. 66: 717–749.
Boyer, P. D. (1999) What makes ATP synthase spin? Nature 402: 247–249.
Cheuk, A., and Meier, T. (2021) Rotor subunits adaptations in ATP synthases from photosynthetic organisms. Biochem Soc Trans. 49 (2): 541–550.
Davis, G. A., and Kramer, D. M. (2020) Optimization of ATPsynthase c–rings for oxygenic photosynthesis. Frontiers in Plant Science 10: 1778.
Junge, W., Lill, H., and Engelbrecht, S. (1997) ATP synthase: An electrochemical transducer with rotatory mechanics. Trends Biochem. Sci. 22: 420–423.
Kuhlbrandt, W. (2019). Structure and Mechanisms of F-Type ATP Synthases. Annu. Rev. Biochem. Vol. 88: 515–549.
Malkin, R. and Niyogi, K. (2000) Photosynthesis. In: Buchanan, B. B., Gruissem, W., and Jones, R., eds. Biochemistry and Molecular Biology of Plants. American Society of Plant Physiologists, Rockville, MD, pp. 575–577.
Noji, H., Yasuda, R., Yoshida, M., and Kinosita, K., Jr. (1997) Direct observation of the rotation of the F1-ATPase. Nature 386: 299–302.
Yasuda, R., Noji. H., Yoshida, M., Kinoshita, K., and Itoh, H. (2001) Resolution of distinct rotational substeps by sub-millisecond kinetic analysis of F1-ATPase. Nature 410, 898–904.
Web Topic 9.10 一些除草剂的作用方式
在现代农业中,使用除草剂杀死不需要的植物非常普遍。已开发出许多不同类别的除草剂,它们通过阻断氨基酸、类胡萝卜素或脂质生物合成,或通过破坏细胞分裂来发挥作用。了解除草剂的作用方式一直是研究植物代谢的重要工具,并促进了它们在不同农业实践中的应用。一类主要的除草剂——约占具有商业重要性化合物的一半——通过中断光合电子流来发挥作用(Ashton and Crafts 1981)。网络图 9.10.A 显示了其中两种化合物的化学结构。已发现这些药剂中许多的精确作用位点要么位于光系统 I 的还原侧(例如,在百草枯中),要么位于两个光系统之间电子传递链中的醌受体复合物处(例如,在敌草隆中;参见网络图 9.10.B)。
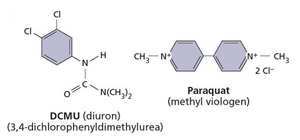
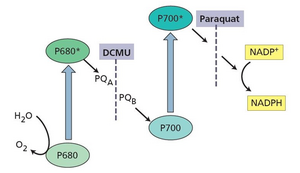
作用于醌受体复合物的除草剂(例如,DCMU)与质体醌竞争 QB 结合位点。如果存在除草剂,它会取代氧化态的质体醌,占据醌受体的特定结合位点,该位点被认为位于 D1 除草剂结合蛋白上。除草剂不能接受电子,因此电子无法离开第一个醌受体 QA。因此,除草剂的结合有效地阻断了电子流并抑制了光合作用。许多以此方式作用的除草剂也抑制具有醌型电子受体复合物的光合细菌中的电子流(Trebst 1986)。
百草枯通过截获结合态铁氧还蛋白受体与NADP之间的电子,并将氧还原为超氧阴离子(O2–)来发挥作用。超氧阴离子是一种自由基,能与叶绿体中的多种分子发生非特异性反应,导致叶绿体活性迅速丧失。细胞膜中的脂质分子尤其敏感。
已开发出一系列具有类似作用模式的除草剂,它们都与QB位点结合(参见Battaglino等人的综述,2020年),包括莠去津等流行产品,由于某些物种(例如玉米)能够分解它,使得可以杀死杂草而不伤害作物,因此被广泛使用。其他还包括多种三嗪类化合物,如特丁津、苯氨基甲酸酯、哒嗪酮、三嗪、三嗪酮、尿嘧啶、酰胺、脲、腈和苯基哒嗪。这些化合物的分子形状大致模拟了质体醌,因此能与QB位点结合。然而,它们结合在口袋内的不同位置,而像溴苯腈这样的化合物直接影响QA的氧化还原特性,产生活性氧并加速光损伤(Fufezan等人,2002年)。
一段时间以来,杂草能迅速对除草剂产生抗性这一点已经很明显(Dover和Croft,1986年),尤其值得注意的是莠去津,其抗性可能源于QB结合口袋中甚至单个氨基酸改变的突变,使得该位点对这些除草剂产生抗性(参见Jia等人的综述,2007年)。因此,这类除草剂正变得越来越无效。此外,许多除草剂被发现具有次生有害效应。百草枯因其对人类的高毒性——小剂量即可致死并与帕金森病相关——以及20世纪70年代美国政府将其用于大麻作物而声名狼藉。同样,莠去津被发现是环境中一种强效的内分泌干扰物,即使在环境中持续存在的低浓度下,也能干扰青蛙的性发育。这些化学品仍然是研究的有用工具,但不出所料,它们在许多欧洲国家被禁用,但在其他国家仍在使用。
参考文献
Ashton, F. M., and Crafts, A. S. (1981)Mode of Action of Herbicides, 2nd ed. Wiley, New York.
Battaglino, B., Grinzato, A., and Pagliano, C. (2021) Binding Properties of Photosynthetic Herbicides with the QBSite of the D1 Protein in Plant Photosystem II: A Combined Functional and Molecular Docking Study Plants 10: 1501. https://doi.org/10.3390/plants10081501
Chase, C. A., Bewick, T. A., and Shilling, D. G. (1998) Characterization of paraquat resistance inSolanum americanumMill. II. Evidence for a chloroplast mechanism.Pesticide Biochem. andPhysiol. 60: 23-30.
Dover, M. J., and Croft, B. A. (1986) Pesticide resistance and public policy.BioScience36: 78-85.
Forouzesh, A. E., Soufizadeh, S., and Samadi Foroushani, S. (2015) Classification of herbicides according to chemical family for weed resistance management strategies-an update.Weed Res. 55: 334-358.
Fufezan, C., Rutherford, A. W., and Krieger-Liszkay, A. (2002) Singlet oxygen production in herbicide-treated photosystem II.FEBS Lett. 532: 407-410.
Jia, Xiaoping, Jincheng Yuan, Yunsu Shi, Yancun Song, Guoying Wang, Tianyu Wang, and Yu Li. (2007) A Ser-Gly Substitution in Plastid-Encoded Photosystem II D1 Protein Is Responsible for Atrazine Resistance in Foxtail Millet (Setaria italica).Plant Growth Regulation52 (1): 81-89.
Trebst, A. (1986) The topology of the plastoquinone and herbicide binding peptides of photosystem II in the thylakoid membrane.Z. Naturforsch. 41c: 240-245.
Web Topic 9.11 叶绿素生物合成
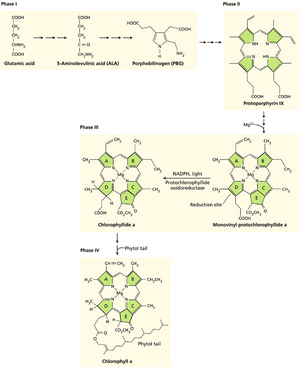
在叶绿素生物合成的第一阶段,氨基酸谷氨酸被转化为5-氨基乙酰丙酸(ALA)(网络图9.11.A)。该反应不同寻常之处在于它涉及一个共价中间体,其中谷氨酸附着在一个转移RNA分子上。这是生物化学中极少数的例子之一,其中tRNA被用于蛋白质合成以外的过程。然后两个ALA分子缩合形成胆色素原(PBG),最终形成叶绿素中的吡咯环。下一阶段是从四个PBG分子组装卟啉结构。此阶段包括六个不同的酶促步骤,以产物原卟啉IX结束。
到此为止的所有生物合成步骤对于叶绿素和血红素的合成都是相同的(参见教科书图9.33)。但在此处途径发生分叉,分子的命运取决于哪种金属被插入到卟啉环的中心。如果镁被一种叫做镁螯合酶的酶插入,那么将发生将分子转化为叶绿素所需的额外步骤;如果插入铁,该物种最终成为血红素。
叶绿素生物合成途径的下一阶段是通过其中一个丙酸侧链的环化形成第五个环(E环),从而生成原叶绿素酸酯。该途径涉及使用NADPH还原D环中的一个双键。在被子植物中,这一过程由光驱动,并由一种叫做原叶绿素酸酯氧化还原酶(POR)的酶执行。不释放氧的光合细菌在没有光的情况下进行此反应,使用一套完全不同的酶。蓝细菌、藻类、低等植物和裸子植物同时含有依赖光的POR途径和不依赖光的途径。在完全黑暗中生长的被子植物幼苗缺乏叶绿素,因为POR酶需要光。这些黄化植物在暴露于光下时会非常迅速地变绿。叶绿素生物合成途径的最后一步是植醇尾部的连接,由一种叫做叶绿素合酶的酶催化(Malkin和Nyogi,2000年)。
参考文献
Malkin, R. and Niyogi, K. (2000) Photosynthesis. In: Buchanan, B. B., Gruissem, W., and Jones, R., eds. (2000)Biochemistry and Molecular Biology of Plants. American Society of Plant Physiologists, Rockville, MD, pp. 575–577.
