第五章Web Topic
Web Topic 5.1 毛细上升计算
在第5.2节中我们了解到,水的内聚力、粘附力和表面张力特性导致了毛细现象,即水在毛细管中短距离向上移动。
对于具有圆形横截面的垂直放置的毛细管,毛细作用方程如下:
H = 2λcos(θ)/(ρgr)
其中 H 是气-水界面相对于水源表面的高度(m),λ 是水的表面张力(N/m),θ 是水在管壁表面的接触角,ρ 是水的密度(kg/m³),g 是重力加速度(m/s²),r 是毛细管半径(m)。
关键要点是毛细管半径越小,毛细上升高度越大。对于管壁可润湿(θ ~ 0)且具有圆形横截面的毛细管,水的移动距离可使用以下公式计算:
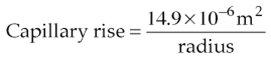
其中毛细上升高度和半径均以米为单位表示。 对于一个半径为 25 µm 的木质部导管,毛细上升高度约为 0.6 m。这个距离对于高大树木的水分向上运输而言太小,可以忽略不计。
纤维材料(如细胞壁)可以像灯芯一样,通过毛细作用从邻近的木质部吸水。这种毛细作用确保直接暴露于空气中的细胞壁表面(如叶肉中的细胞壁)保持湿润而不干燥。由于细胞壁毛细管半径极小,约为 10⁻⁸ m(或 10 nm),因此在紧贴细胞壁蒸发面下方水体中可以产生非常大的物理力。
Web Topic 5.2 扩散半衰期计算
扩散在短距离内很快,但在长距离上极其缓慢
扩散描述了分子群在热扰动下随机运动的行为。请复习教材图5.8。如果设定条件使所有溶质分子都集中在起始位置,那么浓度前沿会随时间推移从起始位置向外移动。随着物质从起点向外扩散,浓度梯度变得平缓(△cs减小),因此净移动速度变慢。
表征扩散运输的时间尺度由下式给出:
时间 ~ (距离)²/Ds
其中 Ds 是扩散系数。这个特征运输时间随距离的平方而增加,因为扩散运输源于单个分子的随机运动:在任何时刻,进行随机行走的分子都可能朝向或背离其原始起点运动。特征时间是理解扩散运输在何种长度尺度上重要的有用指南。对于任何实际系统,扩散的实际时间将取决于边界条件、空间维数以及系统的其他细节。
让我们考虑不同长度尺度下扩散的特征运输时间。小分子(如葡萄糖)在水中的扩散系数约为 10⁻⁹ m²s⁻¹。因此,在一个细胞长度(10 µm)上,扩散的特征时间尺度为:
(10 x 10⁻⁶ m)² / 10⁻⁹ m²s⁻¹ = 0.1 s
这个计算表明小分子在细胞尺度上扩散很快。但对于更长距离的扩散,例如与叶片或整个植物相关的尺度呢?
下表列出了葡萄糖在水中扩散一段距离的特征时间。
| 距离 | 扩散运输的特征时间 |
|---|---|
| 1μm | 1ms |
| 10μm | 0.1s |
| 100μm | 10s |
| 1mm | ~0.3h |
| 1cm | ~30h |
| 1m | 32年 |
这表明,扩散在细胞尺度内是有效的,但对于长距离的运输而言则过于缓慢。正如您将在第 6 章学到的,作为叶片水蒸气损失的驱动力,扩散非常重要,因为分子在空气中的扩散系数远大于在水溶液中的扩散系数。
Web Topic 5.3 水势组分的替代惯例
计划进一步研究植物水分关系的学生应注意,正文中定义的水势(希腊字母 psi)组分有时会有不同的名称和符号。
特别是,教材中的方程 5.5:
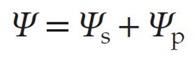
通常被以下等价方程替代:
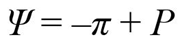
在这种替代惯例中,P 等同于 Ψp。它是溶液的静水压力,可能为正(如膨胀细胞中),也可能为负(如木质部水中)。符号 π(希腊字母 pi)称为渗透压,是 Ψs 的负值。也就是说,π 为正值,而 Ψs 为负值。渗透压是物理化学家、动物学家和许多其他人用来表示溶解溶质对水自由能影响的术语。大多数物理和化学手册使用术语渗透压和符号 π。上述方程中 π 前面的负号解释了溶解溶质导致水势 (Ψw) 降低的原因。因此,Ψs = –π。
遗憾的是,一些作者混合使用了 Ψs和 π 的惯例,导致符号 π 的含义产生了不必要的混淆。因此,π 有时被错误地称为渗透势而非渗透压,并且可能被视为正值或负值。
Web Topic 5.4 温度与水势
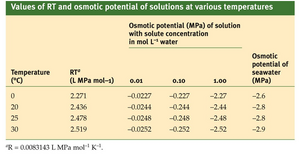
不同温度下的 RT 值以及不同溶质浓度溶液的 Ψs 值列于下方的网络表 5.4.A。对于解离成两个或更多颗粒的离子溶质,必须将 cs 乘以解离的颗粒数,以考虑溶解颗粒数量的增加。这不适用于酸或碱解离释放的 H+ 或 OH- 离子,因为这些离子是溶剂的一部分,而不是稀释剂。
Web Topic 5.5 活细胞中是否存在负膨压?
理解植物水分关系具有挑战性的一个方面是植物体内存在着显著的压力范围,包括正压和负压。负压(或张力)依赖于水的内聚强度以及木质化细胞壁抵抗变形的强度,在通过木质部的水分运输中起着重要作用。正压依赖于质膜的半透性和初生细胞壁的弹性,存在于所有水合状态的活植物细胞中,但在筛管和保卫细胞中尤其大。通常认为活植物细胞只具有正压(例如教材图 5.11)。然而,似乎没有理由认为活植物细胞的细胞质内也不能出现负压。本Web Topic探讨了负膨压在植物中的存在和潜在作用。
当细胞失水时,膨压下降,溶质浓度增加。在膨压丧失点(ψp = 0),细胞液的静水压等于大气压,这意味着没有净力作用于细胞壁。如果细胞继续失水,细胞质内部的压力将降至大气压以下,导致向内的力不平衡。具有未木质化细胞壁的活细胞在干燥时相对容易变形,这个过程称为细胞皱缩(cytorrhysis)。在这些细胞中,当细胞体积减小时,细胞水势降低到膨压丧失点以下,会通过溶质浓度增加来平衡。请注意,质膜仍紧贴细胞壁(即不会发生质壁分离),因为细胞质中的静水压仍然大于质外体中的静水压(另见教材图 5.10)。
具有厚细胞壁和/或部分木质化细胞壁的活细胞情况可能大不相同。测量使细胞壁塌陷所需的力表明,具有厚壁的细胞能够承受高达 1.0 MPa 的压力差(Oertli 等人,1990)。当这些细胞失水时,膨压下降,溶质浓度增加。然而,一旦膨压降至零,细胞壁可能会抵抗变形,从而允许细胞质内产生负压。这使得细胞水势的进一步降低可以通过细胞内越来越负的压力来平衡,而不是通过渗透浓度的增加来平衡。因此,负膨压的产生使得细胞能够降低水势而不发生细胞体积的重大变化。
负膨压可以使细胞受益,因为它允许细胞避免因细胞皱缩而对细胞壁或膜造成的潜在损伤,以及可能对膜和蛋白质构象产生不利影响的高浓度溶质。潜在的缺点包括产生刚性细胞壁的代谢成本,以及厚壁可能对生理功能造成的任何限制。另一个问题是,细胞内的负压是否可能导致空气栓塞的形成,就像在木质部中发生的那样。
总之,负膨压是一个引人入胜但研究甚少的植物水分关系领域(Ding 等人,2014;Yang 等人,2017)。负膨压在防止与严重干燥相关的机械损伤和渗透损伤方面的潜在益处,使得这一主题值得进一步研究。
参考文献
Ding, Y., Zhang, Y., Zheng, Q. S., and Tyree, M. T. (2014) Pressure-volume curves: revisting the impact of negative turgor during cell collapse by literature review and simulations of cell micromechanics.New Phytologist203: 378-387.
Oertli, J. J., Lips, S. H., and Agami, M. (1990) The strength of sclerophyllous cells to resist collapse due to negative turgor pressure.Acta Oecol. 11: 281-289.
Yang, D., Li, J., Ding, Y., and Tyree, M. T. (2017) Experimental evidence for negative turgor pressure in small leaf cells ofRobinia pseudoacaciaL. versus large cells ofMetasequoia glyptostoboidesHu et W.C. Cheng. 2. Höfler diagrams below the volume of zero turgor and the theoretical implications for pressure-volume curves of living cells.Plant, Cell and Environment40: 340-350.
Web Topic 5.6 水分势的测定
植物学家投入了相当大的精力来设计准确可靠的方法以评估植物的水分状况。这里介绍四种已广泛用于测量Ψ、Ψs和Ψp的仪器:湿度计、压力室、冰点渗透压计和压力探针。
湿度计(Ψ 测定)
湿度测量法(Psychrometry,前缀 "psychro-" 来源于希腊语单词psychein,意为 "冷却")基于这样一个事实:水的蒸汽压随其水分势的降低而降低。湿度计测量溶液或植物样本的水汽压,其原理是水的蒸发需要能量,从而使水蒸发的表面冷却。
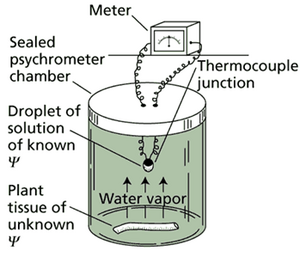
一种被称为等压湿度测量法(isopiestic psychrometry)的湿度测定技术,已被约翰·博耶及其同事广泛使用(Boyer和Knipling 1965),并在网络图5.6.A中予以说明。
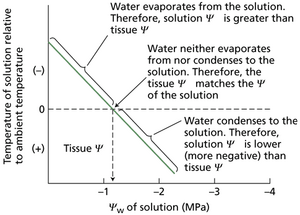
研究人员进行测量的方法是,将一小块组织密封在一个小室内,室内有一个温度传感器(本例中为热电偶)与一小滴已知溶质浓度的标准溶液(已知Ψs,因此已知Ψ)接触。如果组织的水分势低于液滴,水就会从液滴蒸发,通过空气扩散,并被组织吸收。水的这种轻微蒸发会使液滴冷却。组织与液滴之间的水分势差越大,水分转移的速率就越高,从而液滴冷却得越厉害。如果标准溶液的水分势低于待测样品,水将从组织扩散到液滴,导致液滴升温。测量几种已知Ψ的溶液其液滴的温度变化,就可以计算出液滴与组织之间水分净迁移为零时的溶液水分势(网络图5.6.B),这标志着液滴与组织具有相同的水分势。
湿度计可用于测量离体和完整植物组织的水分势。此外,该方法也可用于测量溶液的Ψs。这对于植物组织特别有用。例如,用湿度计测量组织的Ψ,然后压碎组织,用同一仪器测量压出的细胞液的Ψs值。结合这两个测量值,研究人员可以估算出组织被压碎前细胞中存在的膨压(Ψp = Ψ – Ψs)。
这种方法的一个主要困难是测量对温度波动极为敏感。例如,0.01°C 的温度变化对应于约 0.1 MPa 的水分势变化。因此,湿度计必须在恒温条件下操作。因此,该方法主要在实验室环境中使用。(湿度测量技术有很多变体;感兴趣的读者可以参考 Brown 和 Van Haveren 1972;Slavik 1974;Boyer 1995。)
压力室(Ψ 测定)
一种用于估算大块组织(如叶片和小枝条)水分势的相对快速的方法是使用压力室。该方法由都柏林三一学院的亨利·迪克森在二十世纪初开创,但直到斯克里普斯海洋研究所的 P. Scholander 及其同事改进了仪器设计并展示了其实用性后,才得到广泛应用(Scholander 等人,1965)。
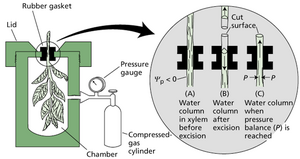
在此技术中,待测器官从植株上切下,并部分密封在压力室中(网络图 5.6.C)。在切割之前,木质部中的水柱处于张力之下。当器官被切下破坏了水柱时(即其张力得到缓解,使其Ψp上升至零),水分通过渗透作用迅速从木质部被拉入周围的活细胞。因此切割表面显得暗淡而干燥。为了进行测量,研究人员用压缩气体给压力室加压,直到活细胞和木质部导管之间的水分分布恢复到初始的、切割前的状态。这可以通过目视观察水分何时返回到切割表面可见的木质部导管的开口端来检测。使水分恢复到初始分布所需的压力称为平衡压力,通过切割表面外观的变化很容易检测到,当达到该压力时,切割表面变得湿润且有光泽。
压力室常被描述为测量木质部张力的工具。然而,这严格来说仅适用于对不蒸腾的叶片或枝条(例如,先前用塑料袋包裹过的)进行的测量。当没有蒸腾作用时,叶细胞的水势和木质部的水势将达到平衡。在这种不蒸腾枝条上测得的平衡压力,其大小与木质部压力(Ψp)相等,但符号相反。由于我们不蒸腾叶片的水势等于木质部的水势,只要收集木质部汁液样本以测定其Ψs,就可以通过将木质部的Ψp和Ψs相加来计算叶片的水势。幸运的是,与木质部典型的中午张力(Ψp为-1至-2 MPa)相比,木质部Ψs通常很小(> -0.1 MPa)。因此,对木质部汁液Ψs的校正经常被省略。
对蒸腾叶片进行平衡压力测量则更难解释。水从木质部流向叶片的事实意味着水势差异必然存在。当蒸腾叶片或枝条被切断时,木质部的张力立即解除,水被吸入叶细胞,直到木质部和叶细胞的水势达到平衡。由于叶细胞的总体积远大于木质部汁液的体积,这种平衡水势将极大地偏向于叶细胞的水势。因此,对此类叶片或枝条进行任何平衡压力测量,所得值将近似为叶片水势,而非木质部的张力。(确切地说,需要将木质部汁液的Ψs与平衡压力的负值相加,才能得到叶片水势。)通过比较在覆盖(即不蒸腾)与未覆盖(蒸腾)叶片上测量的平衡压力,可以探究木质部水势与蒸腾叶片水势之间的差异。
压力室测量提供了一种快速、准确的叶片水势测量方法。由于压力室法不需要精密的仪器或温度控制,它已在野外条件下得到广泛应用(Tyree和Hammel,1972)。(关于压力室理论和操作的更完整描述,请参阅Boyer 1995。)
冰点渗透压计(Ψs测量)
冰点渗透压计通过测量溶液的冰点来测定其渗透势。溶液具有依数性,这些性质总体上取决于溶解粒子的数量,而与溶质的性质无关。例如,溶质会降低溶液的蒸气压、升高其沸点并降低其冰点。溶质的具体性质无关紧要。溶液的依数性之一是其冰点随着溶质浓度的增加而下降。例如,每千克水中含有1摩尔溶质的溶液,其冰点为-1.86°C,而纯水为0°C。
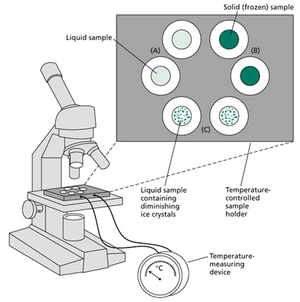
可以使用各种仪器来测量溶液的冰点降低(例如,参见Prager和Bowman 1963,以及Bearce和Kohl 1970)。使用冰点渗透压计时,小至1纳升(10⁻⁹ L)的溶液样本被放置在显微镜控温台上的油介质中(网络图5.6.D)。非常小的样本量允许测量来自单个细胞的汁液,并能使样本与控温台快速达到热平衡。为防止蒸发,研究者将样本悬浮在银板(银具有高导热性)的注油孔中。将控温台的温度迅速降至约-30°C,使样本冻结。然后非常缓慢地升高温度,并通过显微镜观察样本中的融化过程。当样本中最后一块冰晶融化时,记录下控温台的温度(注意熔点和凝固点是相同的)。从冰点降低值计算溶质浓度很简单;根据溶质浓度(cs),Ψs计算为–RTcs。该技术已用于测量从单个细胞中提取的液滴(Malone和Tomos,1992)。
压力探针(Ψp测量)
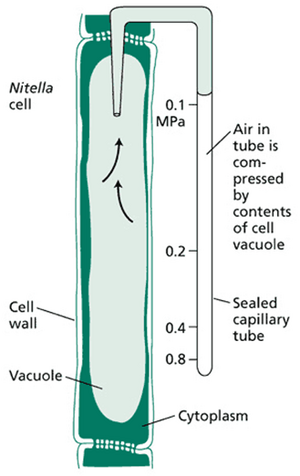
如果一个细胞像西瓜甚至葡萄一样大,测量其静水压将是一项相对容易的任务。然而,由于植物细胞尺寸微小,直接测量膨压的方法发展缓慢。宾夕法尼亚大学的Paul Green使用微压计,开发了首批直接测量植物细胞膨压的方法之一(Green和Stanton,1967)。在该技术中,将一端密封的充气玻璃管插入细胞中(网络图5.6.E)。细胞内的高压压缩了捕获的气体,根据体积变化,可以很容易地根据理想气体定律(压力 × 体积 = 常数)计算出细胞压力。这种方法仅适用于体积相对较大的细胞,例如丝状绿藻Nitella的巨型细胞。对于较小的细胞,细胞汁液流入玻璃管足以使细胞瘪塌,从而导致人为的低压测量结果。
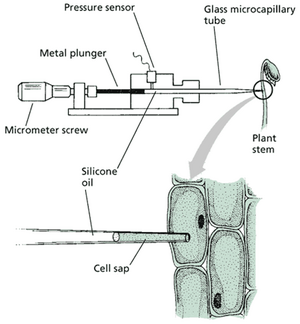
对于比Nitella体积小几个数量级的高等植物细胞,德国的Ernst Steudle、Ulrich Zimmermann及其同事开发了一种更精密的装置——压力探针(Hüsken等人,1978年)。该仪器类似于一个微型注射器(Web图5.6.F)。将一根玻璃微毛细管拉成细尖,然后插入细胞中。微毛细管内充满硅油,这是一种相对不可压缩的流体,在显微镜下可以很容易地与细胞液区分开来。当微毛细管尖端首次插入细胞时,由于该区域初始压力较低,细胞液开始流入毛细管。研究人员可以在显微镜下观察到这种汁液的移动,并通过推动装置的柱塞来抵消它,从而建立压力。通过这种方式,油和细胞液之间的边界可以被推回到微毛细管的尖端。当边界回到尖端并保持恒定位置时,细胞的初始体积得以恢复,并且细胞内的压力恰好与毛细管中的压力平衡。该压力由装置中的压力传感器测量。因此,可以直接测量单个细胞的静水压力。
该方法已被用于测量多种植物物种离体和完整组织细胞中的Ψp(压力势)和水关系其他参数(Steudle,1993)。此方法的主要局限在于,某些细胞太小而无法测量。此外,一些细胞在被毛细管刺穿后容易泄漏,另一些则会堵塞毛细管尖端,从而阻碍有效测量。压力探针经过改进,也可用于测量木质部中Ψp的正值和负值(Heydt和Steudle,1991)。然而,与空穴现象(参见教材第6章)相关的技术问题限制了用此技术测量负Ψp。
参考文献
Bearce, B. C., and Kohl, H. C., Jr. (1970) Measuring osmotic pressure of sap within live cells by means of a visual melting point apparatus. Plant Physiol. 46: 515–519.
Boyer , J.S. (1995) Measuring the Water Status of Plants and Soils. Academic Press, N.Y.
Boyer, J. S., and Knipling, E. B. (1965) Isopiestic technique for measuring leaf water potentials with thermocouple sychrometer. Proc. Natl. Acad. Sci. USA 54: 1044–1051.
Brown, R. W., and Van Haveren, B. P., eds. (1972) Psychrometry in Water Relations Research. Proceedings of the Symposium on Thermocouple Psychrometers. Utah Agricultural Experiment Station, Utah State University, Provo.
Green, P. B. (1968) Growth physics in Nitella: A method for continuous in vivo analysis of extensibility based on a micro-manometer technique for turgor pressure. Plant Physiol. 43: 1169–1184.
Green, P. B., and Stanton, F. W. (1967) Turgor pressure: Direct manometric measurement in single cells of Nitella. Science 155: 1675–1676.
Heydt, H., and Steudle, E. (1991) Measurement of negative pressure in the xylem of excised roots. Effects on water and solute relations. Planta 184: 389–396.
Hüsken, D., Steudle, E., and Zimmermann, U. (1978) Pressure probe technique for measuring water relations of cells in higher plants. Plant Physiol. 61: 158–163.
Malone, M., and Tomos, A. D. (1992) Measurement of gradients of water potential in elongating pea stem by pressure probe and picolitre osmometry. J. Exp. Bot. 43: 1325–1331.
Prager, D. J., and Bowman, R. L. (1963) Freezing-point depression: New method for measuring ultramicro quantities of fluids. Science 142: 237–239.
Scholander, P. F., Hammel, H. T., Bradstreer, E. D., and Hemmingsen, E. A. (1965) Sap pressure in vascular plants. Science 148: 339–346.
Slavik, B. (1974) Methods of Studying Plant Water Relations. Academia, Prague.
Steudle, E. (1993) Pressure probe techniques: Basic principles and application to studies of water and solute relations at the cell, tissue and organ level. In Water Deficits: Plant Responses from Cell to Community, J. A. C. Smith and H. Griffiths, eds., BIOS Scientific, Oxford, pp. 5–36.
Tyree, M. T., and Hammel, H. T. (1972) The measurement of the turgor pressure and the water relations of plants by the pressure-bomb technique. J. Exp. Bot. 23: 267–282.
Web 主题 5.7 基质势
在讨论土壤、种子和细胞壁时,常常会提到Ψ(水势)的另一个组分:基质势(Ψm)。基质势用于解释当水以一两分子厚的薄表面层形式吸附在相对干燥的土壤颗粒、细胞壁和其他材料表面时,其自由能的降低。基质势并不代表作用于水的新作用力,因为理论上表面相互作用的影响可以通过其对Ψs(溶质势)和Ψp(压力势)的影响来解释(见 Passioura 1980; Nobel 1999)。然而,在干燥材料中,表面相互作用通常不易区分为Ψp和Ψs组分,因此它们经常被归为一类,并指定为基质势。
将Ψm与独立测量的Ψs和Ψp相加以得到总水势,通常是不成立的。对于含水细胞和细胞壁内的水来说尤其如此,在这些情况下,基质效应要么可以忽略不计,要么已通过Ψp的降低来解释。例如,第5.4节讨论的叶片蒸发表面处由细胞壁微毛细管持有的水中的负压,有时被描述为细胞壁基质势。在Ψp、Ψs和Ψm的定义中解释这种物理效应时,需要注意避免不一致性(Passioura 1980)。
参考文献
Nobel, P. S. (1999). Physicochemical and Environmental Plant Physiology. Academic Press, San Diego.
Passioura, J. B. (1980) The meaning of matric potential. J. Exp. Bot. 31: 1161-1169.
Web 主题 5.8 萎蔫与质壁分离
质壁分离是指植物细胞质因失水而与细胞壁分离的现象。在实验室中,可以通过将植物细胞浸入高盐或高糖溶液中诱导质壁分离,从而使细胞通过渗透作用失水。
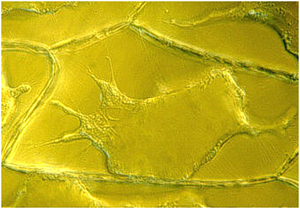
如果将洋葱表皮组织浸入硝酸钙溶液中,细胞会通过渗透作用迅速失水,细胞的原生质体收缩(网络图5.8.A)。发生这种情况是因为钙离子和硝酸根离子自由渗透细胞壁,遇到具有选择透过性的质膜。细胞中央的大液泡最初含有低浓度溶液,其渗透压远低于质膜另一侧的硝酸钙溶液。因此,液泡失水并缩小。细胞膜与细胞壁之间的空间增大,质膜及其内部的原生质体收缩至细胞中央。由于质膜与细胞壁的连接点,细胞质形成细丝延伸至细胞壁。发生质壁分离的细胞会死亡,除非将其迅速从盐溶液或糖溶液中转移到水中。
质壁分离在自然界中不太可能发生,因为体内细胞脱水通常是质外体Ψp降低的结果,而非Ψs降低。在这些条件下,只有当空气能够穿过细胞壁时,才会发生质壁分离(类似于空气可以被拉过木质部中的纹孔膜,如第6章所述)。
Web Topic 5.9 理解水力传导性
考虑一个初始水势为–0.2 MPa的细胞浸没在纯水中。根据此信息,我们知道水将流入细胞,驱动力为ΔΨ = 0.2 MPa,但初始移动速率是多少?速率取决于膜对水的通透性,该特性通常称为膜的水力传导性(参见教材图5.13)。
驱动力、膜通透性和流速由以下公式关联:
流速 = 驱动力 × 水力传导性
水力传导性表示水穿过膜的难易程度,其单位为单位膜面积、单位时间、单位驱动力下的水体积(例如,m³·m⁻²·s⁻¹·MPa⁻¹ 或 m·s⁻¹·MPa⁻¹)。水力传导性越大,流速越大。在教材图5.13中,膜的水力传导性为10⁻⁶ m·s⁻¹·MPa⁻¹。那么,传输(流动)速率(Jv)可由以下公式计算得出:
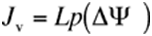
其中,Jv是单位膜面积、单位时间内穿过膜的水体积(m³·m⁻²·s⁻¹ 或等效为 m·s⁻¹)。注意,该公式假定膜是理想的——即溶质运输可忽略,且水运输对跨膜的ΔΨs和ΔΨp同等敏感。非理想膜则需要一个更复杂的公式,分别考虑由ΔΨs和ΔΨp引起的水流(Nobel 1999)。
在我们的例子中,Jv的值为0.2 × 10⁻⁶ m·s⁻¹。注意,Jv的物理含义是速度。我们可以将Jv乘以细胞的表面积,计算出体积意义上的流速(m³·s⁻¹)。
所得值是水运输的初始速率。随着水被吸收,细胞Ψ增加,驱动力(ΔΨ)减小。因此,水运输随时间推移而减慢。如第5.6节所述,该速率以指数方式趋近于零(参见Dainty 1976)。
参考文献
Dainty, J. (1976) Water relations of plant cells. In Transport in Plants II, Part A, Cells, U. Lüttge and M. G. Pitman, eds. Encyclopedia of Plant Physiology, New Series, Vol. 2. Springer-Verlag, Berlin, pp. 12–35.
Nobel, P. S. (1999) Physicochemical and Environmental Plant Physiology. Academic Press, San Diego.
