第十章Web Topic
Web Topic 10.1 CO₂ 泵
产氧光合作用始终利用 Rubisco 作为将无机碳整合到有机化合物骨架中的核心酶。然而,目前大气 CO₂ 浓度并未饱和其羧化酶活性,并且该酶的羧化酶活性被其加氧酶活性竞争性抑制是其固有特性。
因此,许多光合生物,特别是细菌和藻类,含有用于固定无机碳的 CO₂ 浓缩机制。这些机制主动转运 HCO₃⁻、CO₂ 和/或 H⁺,以提高 Rubisco 活性位点处的 CO₂ 浓度和 CO₂/O₂ 比率,从而促进羧化酶活性。在陆地植物中,CO₂ 浓缩机制通常是 C4 光合作用和景天酸代谢 (CAM)。或者,CO₂ 和 HCO₃⁻ 膜泵在原核蓝细菌和真核藻类中已被广泛研究,但也存在于一些水生植物中。
为响应水环境中无机碳浓度的变化,许多光合生物会诱导浓缩 CO₂ 的机制,从而促进 Rubisco 的羧化反应。虽然当用于给培养基充气的空气从 5% CO₂ 切换到 0.03% CO₂ 时,蓝细菌和藻类表现出光呼吸症状(生长受阻、早衰),但这些生物能迅速发展出浓缩无机碳的能力,以最小化 Rubisco 的加氧酶活性。
在蓝细菌中,两个细胞组分对无机碳的浓缩至关重要(网络图 10.1.A):
- 位于质膜和类囊体膜上的 CO₂ 和 HCO₃⁻ 转运蛋白,以及
- 羧酶体,这是一个蛋白质微区室,大部分 Rubisco 和碳酸酐酶位于其中。
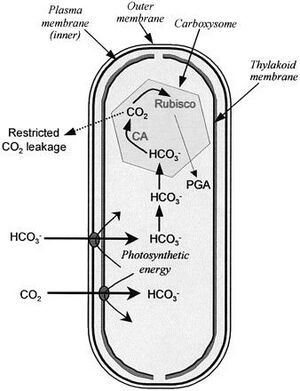
羧酶体是一种独特的微体,由蛋白质外壳包围,包含细胞中大部分的 Rubisco,并且与类囊体膜不同。在低大气 CO₂ 水平下,蓝细菌利用与质膜和类囊体膜相关的 HCO₃⁻ 和 CO₂ 泵在细胞质中积累无机碳。HCO₃⁻ 从细胞质扩散到羧酶体中,一旦进入该区室,碳酸酐酶就将 HCO₃⁻ 转化为 CO₂,用于 Rubisco 反应。
简而言之,无机碳从环境到 Rubisco 附近的过程需要:
- HCO₃⁻ 在细胞质中的积累
- 其向含 Rubisco 的羧酶体的转运
- 通过羧酶体碳酸酐酶将 HCO₃⁻ 转化为 CO₂ (Badger and Price 2003)
Rubisco 周围 CO₂ 的协同富集最终抑制了 1,5-二磷酸核酮糖的加氧作用,从而消除了对光呼吸的需求。
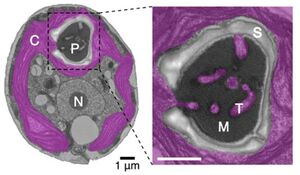
诸如衣藻属(Chlamydomonas)等藻类,也可利用一种诱导型碳浓缩机制来增加Rubisco周围的CO₂可用性(Wang等,2015)。这种碳浓缩机制通常通过将HCO₃⁻泵入细胞,穿过质膜,然后穿过叶绿体被膜进入叶绿体而运作。随后,HCO₃⁻在Rubisco周围被碳酸酐酶转化为CO₂,该区域被区隔在一个称为蛋白核的蛋白质体内(Web图10.1.B)。
参考文献
Badger, M. R., and Price, G. D. (2003) CO2 concentrating mechanisms in cyanobacteria: molecular components, their diversity and evolution, Journal of Experimental Botany 54(383): 609–622. https://doi.org/10.1093/jxb/erg076.
Meyer, M. T., Itakura, A., K, Patena, W., Wang, L., He, S., Emrich-Mills, T., Lau, C. S., Yates, G., Mackinder, L. C. M., and Jonikas, M. C. (2020) Assembly of the algal CO2-fixing organelle, the pyrenoid, is guided by a Rubisco-binding motif. Sci Adv. 6(46):eabd2408.
Wang, Y., Stessman, D. J., and Spalding, M. H. (2015) The CO2 concentrating mechanism and photosynthetic carbon assimilation in limiting CO2: how Chlamydomonas works against the gradient. Plant J, 82: 429–448. https://doi.org/10.1111/tpj.12829.
Web Topic 10.2 卡尔文-本森循环是如何被阐明的
卡尔文循环的阐明是梅尔文·卡尔文及其同事(安德鲁·本森和阿尔·巴萨姆;参见 Bassham 等人,1954)在20世纪50年代进行的一系列精妙实验的结果,他们因此在1961年获得了诺贝尔奖(Calvin,1964)。他们使用单细胞真核绿藻Chlorella的悬浮液来追踪碳的路径。卡尔文-本森循环也被称为还原戊糖磷酸循环,以区别于与其共享几种酶的氧化戊糖磷酸途径(见教科书第13章)。卡尔文-本森循环也被称为光合碳还原循环。
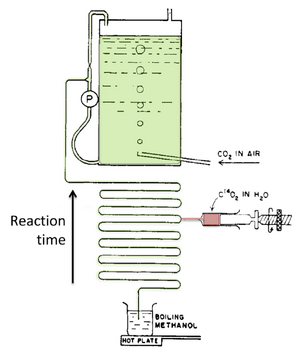
为了阐明这个循环,研究者首先将藻类细胞置于恒定的光照和CO₂条件下以建立稳态光合作用。接着,他们在短时间内添加放射性¹⁴CO₂以标记循环中的中间产物。然后,他们通过将悬浮液迅速浸入沸腾的酒精中来杀死细胞并使其酶失活(网络图 10.2.A)。
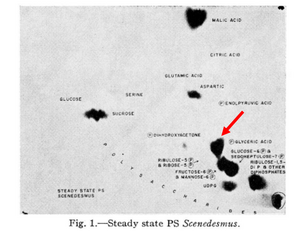
收集到的¹⁴C标记化合物被相互分离,并通过它们在二维纸色谱上的位置进行鉴定(网络图 10.2.B)。
通过这种方式,3-磷酸甘油酸和各种磷酸糖被鉴定为碳固定的中间产物。通过让细胞暴露于¹⁴CO₂的时间逐渐缩短,卡尔文的研究小组能够确定3-磷酸甘油酸是第一个稳定的中间产物。因此,其他标记的磷酸糖必然源自3-磷酸甘油酸的后续还原(Bassham,1954)。
为了推导碳的途径,有必要确定14C在每种标记糖中的分布情况。经过短暂的14CO2暴露后,分离出各个中间体并进行化学降解,从而可以测定每个碳原子中的14C含量。结果显示,3-磷酸甘油酸最初主要在羧基中被标记。这一发现表明,最初的CO2受体是一个二碳化合物,并促使人们对此类化合物进行了长期而无果的探索。
随后发现戊糖单磷酸盐和一种戊糖双磷酸盐(核酮糖)参与循环,这提出了最初CO2受体是五碳化合物的可能性。这一概念上的突破迅速导致了核酮糖-1,5-二磷酸被确认为CO2受体,并促成了完整循环的构建。该循环的运行解释了其他中间体的14C标记模式。
参考文献
Bassham, J. A., Shibata, K., Steenberg, K., Bourdon, J., Calvin, M. (1956) The Photosynthetic Cycle and Respiration: Light-dark Transients1. Journal of the American Chemical Society 78: 4120–4124.
Bassham, J. A., Benson, A. A., Kay, L. D., Harris, A. Z., Wilson, A. T., Calvin, M. (1954) The path of carbon in photosynthesis. XXI. The cyclic regeneration of carbon dioxide acceptor. J Am Chem Soc 76(7): 1760–1770. https://doi.org/10.1021/ja01636a012.
Calvin, M. (1964) The path of carbon in photosynthesis. In: Nobel lectures, chemistry 1942–1962. Elsivier, Amsterdam, pp. 618–644. https://doi.org/10.2172/928404.
Sharkey, T. D. (2019) Discovery of the canonical Calvin–Benson cycle. Photosynth Res 140: 235–252. https://doi.org/10.1007/s11120-018-0600-2.
Web Topic 10.3 Rubisco:研究结构与功能的模型酶
除了一些原核生物固定的碳之外,地球上大部分固定的碳都是由卡尔文循环处理的。Rubisco作为卡尔文循环的羧化酶,其浓度通常很高。例如,它占植物叶片总蛋白质的50%或更多,并且在叶绿体内的浓度极高(约0.2克/毫升)。
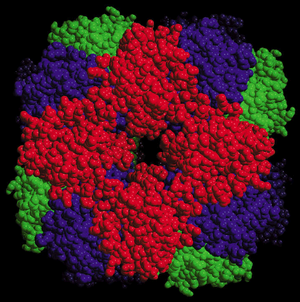
Rubisco存在三种功能类似但结构、分布和O2敏感性不同的形式。产氧光养生物(蓝细菌、高等植物的叶绿体)和许多光合细菌含有该酶的一种形式(形式I),由八个大(L)催化亚基(每个约55 kDa)和八个小(S)亚基(每个约14 kDa)组成,整个蛋白质(L8S8)的分子量约为560 kDa。形式I的8个L亚基排列成一个八聚体核心,周围环绕着两层各四个S亚基,每层位于分子的两侧(网络图 10.3.A)。
Rubisco的形式II和III缺乏小亚基,由两个L亚基组成,每个50 kDa。这些形式的Rubisco发现于一些光合紫色非硫细菌、变形菌、化能自养生物、甲藻和古菌中。最近在缺乏卡尔文循环的光合绿色硫细菌中发现了一种缺乏催化活性的类Rubisco酶。证据表明该酶可能在硫氧化中起作用,为光合电子传递链提供电子。基因组序列显示,这种类Rubisco蛋白也存在于某些异养细菌中。
酶特异性
除了其羧化反应外,Rubisco也与O2反应,这在许多光合生物中导致了光呼吸的需求——一种明显浪费的反应,降低了碳并入有机化合物的效率(参见教科书第10章)。由于CO2和O2是Rubisco的竞争性底物,核酮糖-1,5-二磷酸的2,3-烯二醇中间体的羧化(参见教科书图10.4)取决于环境CO2/O2比率(参见Web Topic 8.5)和酶的内在特性(即特异性因子φ [sigma])。
羧化反应和氧化反应的反应速率分别由网络方程 10.3.1 和 10.3.2 给出。
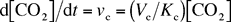
网络方程 10.3.1
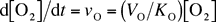
网络方程 10.3.2
其中 Kc:CO2的米氏常数;Ko:O2的米氏常数;Vc:羧化最大反应速度;Vo:氧化最大反应速度。
在此基础上,Rubisco催化的羧化与氧化反应之比为
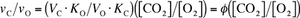
网络方程 10.3.3
其中特异性因子(φ)代表Rubisco对两种竞争底物的区分能力。显然,φ值高表明对CO2的特异性更强。
在Rubisco的形式I中,特异性因子φ的范围从50(蓝细菌)到80(C3和C4植物),但在形式II中降至约10(紫色光合细菌)。对Rubisco特性影响特异性因子的方式进行更详细的分析表明,Kc(羧化)是变异的主要原因,但也发现了Ko(氧化)和Vc/Vo的变化。
生物合成与组装
编码Rubisco小亚基(rbcS)和大亚基(rbcL)的基因对于自养细胞的功能至关重要。与原核生物不同,原核生物中基因表达和蛋白质生物合成发生在同一细胞区室(细胞质)中,而大多数真核生物的Rubisco的组装则依赖于可能需要多个细胞区室参与的多种生化过程的协调作用。在植物(metaphyte)和绿藻(chlorophyte)的细胞核中,光介导的对rbcS表达的调控在细胞质核糖体上产生一个前体多肽。穿过叶绿体被膜的转运会移除N端叶绿体靶向肽,并在叶绿体基质中释放成熟形式。另一方面,植物和绿藻的叶绿体基因组编码rbcL,因此大亚基的生物合成完全发生在叶绿体核糖体上。Rubisco从其组成亚基的组装发生在叶绿体内。
调节蛋白质折叠的特殊蛋白质在一个利用ATP的过程中协助形成L8S8型Rubisco。这些被称为分子伴侣的蛋白质,改变目标蛋白质的非共价相互作用,并使酶形成活性构象。几种不同的分子伴侣促进两个亚基的组装。
参考文献
Malkin, R., and Niyogi, K. K. (2000) Photosynthesis. In: Biochemistry and Molecular Biology of Plants, B Buchanan, W Gruissem, R Jones, eds (Rockville, MD: American Society of Plant Physiologists), pp. 568–628.
Web Topic 10.4 陆地植物光合作用的能量需求
卡尔文-本森循环对能量的有效利用
需要ATP和NADPH提供的持续能量输入,以维持卡尔文-本森循环运行来固定CO2。在卡尔文-本森循环的羧化和还原阶段形成磷酸丙糖,需要光下在叶绿体类囊体膜中产生的能量(ATP)和还原当量(NADPH)。

在稳态光合作用条件下,形成的磷酸丙糖中有六分之一离开卡尔文-本森循环,用于淀粉和蔗糖的净合成。其余六分之五则用于再生CO2受体1,5-二磷酸核酮糖。再生阶段需要额外的ATP,以利用5个磷酸丙糖形成3个分子的1,5-二磷酸核酮糖。

因此,卡尔文-本森循环完整运行一周,需要消耗9个ATP和6个NADPH,以将三个CO2固定为一个磷酸丙糖(网络图10.4.A)。总之,卡尔文-本森循环固定每个CO2分子消耗两个NADPH分子和三个ATP分子(即,每光同化一个CO2,ATP:NADPH的比例为3:2)。
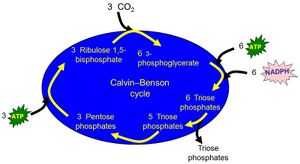
在此基础上,我们可以通过比较从CO2合成碳水化合物所消耗的能量与NADPH氧化和ATP水解所产生的能量,来计算卡尔文-本森循环的效率。为此,必须考虑以下几点:
- 一摩尔己糖完全氧化为CO2(燃烧)释放的能量为2,804 kJ [C6H12O6 + O2 → CO2 + H2O ΔG° = 2,804 kJ]。
- 从六摩尔CO2合成一摩尔己糖(例如果糖6-磷酸)消耗3,684 kJ。
- 12摩尔NADPH的氧化[NADPH + 1/2 O2 + H+ → NADP+ + H2O ΔG° = –217 kJ/摩尔]释放2604 kJ。
- 18摩尔ATP的水解[ATP + H2O → ADP + Pi ΔG° = –60 kJ/摩尔]释放1080 kJ(见网络附录1)。
- 12摩尔NADPH的氧化[NADPH + 1/2 O2 + H+ → NADP+ + H2O ΔG° = –217 kJ/摩尔]释放2604 kJ。
- 18摩尔ATP的水解[ATP + H2O → ADP + Pi ΔG° = –60 kJ/摩尔]释放1080 kJ(见网络附录1)。
因此,卡尔文-本森循环的热力学效率约为75% [(2,804/3,684 × 100%]。进一步分析这些计算可知,CO2转化为碳水化合物的过程主要是一个还原过程,因为所需的大部分能量来自NADPH。12摩尔NADPH的氧化释放2,604 kJ,而18摩尔ATP的水解提供1080 kJ;因此,卡尔文-本森循环中使用的总能量的71% [(2,604/3,684) × 100]来自还原剂NADPH。
只有光合有效辐射(波长范围在400到700纳米之间的光)能被植物利用。在此基础上,如果我们知道入射光的能量含量和光合作用过程的最小量子需求(每固定一摩尔CO2吸收的量子摩尔数;参见第9章),我们就可以计算光合作用的最大整体热力学效率。在卡尔文-本森循环中固定一摩尔CO2需要两摩尔NADPH和三摩尔ATP。通常计算的最小量子需求是每产生两摩尔NADPH和ATP需要八个光子(最小量子需求是每电子两个光量子,然后八个光量子用于驱动水的氧化:2 H2O → O2 + 4 H+ + 4 e–)。将需要一个额外的光量子来驱动循环电子流,以产生固定CO2所需的第三个ATP。波长为680 nm的红光每摩尔光子含有175 kJ。因此,将六摩尔CO2还原为一摩尔己糖所需的最小光能约为:6摩尔 CO2 × 9个680 nm光子/摩尔 CO2 × 175 kJ/680 nm光子 = 9,450 kJ。鉴于合成一摩尔己糖至少需要2,804 kJ,光合作用的最大整体热力学效率约为光合有效辐射的30% [(2,804/9,450) × 100]。
因此,当热力学估算依赖于底物提供的能量时,CO2光合同化的理论效率为90%,但当计算依赖于入射光能量时,效率降至近30%。这种差异表明,在光反应产生ATP和NADPH的过程中,大部分光能损失了,而不是在卡尔文-本森循环运行期间。
然而,在田间正常生长条件下,植物的实际表现远低于这些理论值。通常,植物的发育阶段和环境因素(如水、矿质养分、温度)共同作用往往会降低光合作用的产量。大多数作物(如马铃薯、大豆、小麦、水稻和玉米)的转换效率通常在 0.1% 到 0.4% 之间,与 C4 植物相比,C3 植物的效率通常较低。对于德克萨斯州和夏威夷的甘蔗而言,在最佳条件下几乎可以实现全年活跃生长,其效率值接近 2%。
C4 和 CAM 循环比卡尔文-本森循环具有更高的能量需求
C4 循环。 热力学告诉我们,建立和维持任何代谢物梯度都必须做功。这一原理同样适用于 C4 循环中 CO2 浓度梯度的运作。通过对相关反应进行总和(参见教材表 10.3),我们计算出,维管束鞘细胞中 NADP-苹果酸酶的作用 [苹果酸 + NADP+ → 丙酮酸 + NADPH + CO2](反应 4a)平衡了叶肉细胞中苹果酸脱氢酶用于还原草酰乙酸所消耗的 NADPH [草酰乙酸 + NADPH → 苹果酸 + NADP+](反应 2)。另一方面,叶肉细胞中初级 CO2 受体磷酸烯醇式丙酮酸的再生,需要消耗额外的两个 ATP 分子来驱动两个吸能反应——由丙酮酸-磷酸二激酶催化(网络图 10.4.B)。

这些反应辅以焦磷酸酶催化的焦磷酸放能水解为无机磷酸盐的过程 [焦磷酸 + H2O → 2 磷酸盐]。
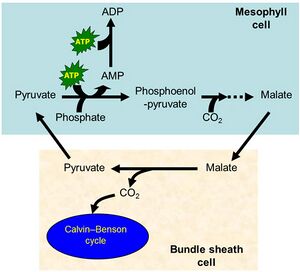
总之,C4 光合作用将每个 CO2 分子固定为碳水化合物,需要消耗两个 NADPH 分子和五个 ATP 分子(即,每同化一个 CO2,ATP:NADPH 的比例为 5:2)。
由于这种更高的能量需求,在低光呼吸条件下(高 CO2 和低温)进行光合作用的 C4 植物,每固定一个 CO2 所需的光量子数比 C3 叶片多。在正常空气中,C3 植物的量子需求会随影响光合作用和光呼吸平衡的因素(如温度)而变化。相比之下,由于存在避免光呼吸的机制,C4 植物的量子需求在不同环境条件下保持相对恒定(参见教材图 11.16)。
CAM 循环。 在夜间固定两个 CO2 分子还原草酰乙酸的过程中消耗了两个 NADH 分子,但在昼间释放两个 CO2 分子以运行卡尔文-本森循环的过程中又产生了两个 NADH 分子。也就是说,夜间 PEPCase 利用的两个还原型吡啶核苷酸分子,与昼间苹果酸酶产生的相似数量相匹配。
另一方面,需要额外的能量来从丙酮酸(由四碳化合物苹果酸在昼间脱羧形成)建立起足够的磷酸烯醇式丙酮酸水平(夜间 CO2 的初级受体)(参见图 10.13)。白天,两个丙酮酸分子通过糖异生途径用于将一个已糖部分掺入淀粉中(网络图 10.4.C)。将两个丙酮酸分子转化为淀粉的昼间过程消耗了两个 NADH 分子和七个当量的 ATP(网络表 10.4.A)。夜间,从一个已糖分子(来自淀粉)形成两个磷酸烯醇式丙酮酸分子,产生两个 NADH 分子和两个 ATP 分子,但在从淀粉形成果糖-1,6-二磷酸的过程中消耗了两个 ATP 分子。
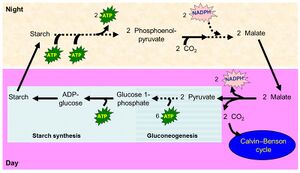

总之,在 CAM 光合作用中,除了通过卡尔文-本森循环将每个 CO2 分子同化为碳水化合物需要消耗两个 NADPH 分子和三个 ATP 分子外,还需要补充消耗 3.5 个 ATP 分子。
Web Topic 10.5 Rubisco 活化酶
Rubisco 催化 CO2 掺入到核酮糖-1,5-二磷酸烯二醇形式的 C-2 位,并随后切割不稳定的中间产物,生成两个 3-磷酸甘油酸分子(参见Web Topic 10.3 和教材图 10.4)。Rubisco 从非活性形式转变为活性状态是羧化反应和加氧反应所必需的,这需要特定赖氨酸残基(在菠菜中是 Lys-201)的氨基甲酰化。由于 CO2 分子与该赖氨酸残基结合,酶获得了一个由三个阴离子残基组成的三联体,为辅助因子 Mg2+ 提供了结合位点(在菠菜中,另外两个残基是 Asp-203 和 Glu-204)。在此阶段,核酮糖-1,5-二磷酸的掺入引起 Rubisco 构象变化,使酶能够将糖分子核酮糖-1,5-二磷酸从溶剂中隔离出来,并在结合 CO2 或 O2 分子后,启动催化循环。然而,核酮糖-1,5-二磷酸与未氨基甲酰化的酶分子紧密结合,会再生一个“死胡同”复合物,即 Rubisco-核酮糖-1,5-二磷酸,从而使 Rubisco 迅速失活。这个问题如何解决?(参见教材图 10.5)
遗传学、生理学和生物化学研究的结合,为解决长期存在的Rubisco激活之谜提供了答案。在体内,一些拟南芥(Arabidopsis thaliana)突变体缺乏光介导的Rubisco激活,只能在高浓度CO₂条件下生长。令人惊讶的是,该突变并未损害酶在体外对CO₂和Mg²⁺调节的响应。这些矛盾的结果导致了一种蛋白质——Rubisco激活酶——的发现,该酶能将核酮糖-1,5-二磷酸从去氨甲酰化的活性位点解离,并在此过程中促进CO₂和Mg²⁺进入以完成酶的氨甲酰化。这一过程的重要性在于,Rubisco激活酶增强Rubisco催化能力的速率与ATP的水解有关(每激活1个Rubisco位点水解50个ATP分子)。在多个物种中发现的两种Rubisco激活酶同工型(42 kDa和46 kDa)由于共同前体mRNA的差异剪接,导致其C端区域不同。两种同工型都能催化Rubisco的激活和ATP的水解,但较小的同工型在这两种活性上的能力均高于较大的同工型。研究表明,用胰蛋白酶消化天然Rubisco激活酶或通过定点诱变改变其一级结构,在刺激Rubisco和水解ATP方面不会引发相同的反应,这为这两个过程是独立的事实提供了证据(Esau等人,1996年;Kallis等人,2000年)。更重要的是,删除Rubisco激活酶C端区域的一些残基会使Rubisco激活速率加倍,而对ATP水解的影响微乎其微。
激活酶对Rubisco的激活需要两种蛋白质的相互识别。来自烟草(茄科,Solanaceae)的Rubisco激活酶无法激活来自菠菜或衣藻(非茄科)的Rubisco;同样,来自菠菜或衣藻的Rubisco激活酶也无法刺激来自烟草的Rubisco。然而,替换衣藻Rubisco大亚基表面的一些残基,能将特异性从非茄科Rubisco激活酶转变为茄科Rubisco激活酶(Ott等人,2000年)。这些实验强调了特定氨基酸对蛋白质-蛋白质相互作用的贡献,并为识别步骤与后续激活过程分离提供了实验证据。
参考文献
Esau, B. D., Snyder, G. W., and Portis, A. R., Jr. (1996) Differential effects of N- and C-terminal deletions on the two activities of Rubisco activase.Arch. Biochem. Biophys. 326: 100–105.
Kallis, R. P., Ewy, R. G., and Portis, A. R., Jr. (2000) Alteration of the adenine nucleotide response and increased Rubisco activation activity of Arabidopsis Rubisco activase by site-directed mutagenesis.Plant Physiol. 123: 1077–1086.
Ott, C. M., Smith, B. D., Portis, A. R., Jr.,and Spreitzer, R. J. (2000) Activase region on chloroplast ribulose-1,5-bisphosphate carboxylase/oxygenase.J. Biol. Chem. 275: 26241–26244.
Web Topic 10.6 光呼吸途径的运行
支持光呼吸途径的证据来自多种类型的实验。C. Somerville和W. L. Ogren利用缺乏磷酸乙醇酸磷酸酶(该酶催化教材图10.8,B部分中的反应2)的拟南芥(Arabidopsis)突变体植株证明,在有利于光呼吸的条件下(高浓度O₂、低浓度CO₂),来自¹⁴CO₂的放射性在2-磷酸乙醇酸中积累,但在非光呼吸条件下(低O₂、高CO₂)则不积累。此外,体内乙醇酸的合成依赖于O₂,并受CO₂以竞争性方式抑制,这与Rubisco在该循环中的主要作用预期相符。
多项研究表明,与卡尔文循环一样,光呼吸的酶在体外催化所有拟议反应的速度高于体内光呼吸速率。此外,参与酶定位于叶绿体(Rubisco、磷酸乙醇酸磷酸酶、甘油酸激酶)、过氧化物酶体(乙醇酸氧化酶、过氧化氢酶、羟基丙酮酸还原酶以及两种氨基转移酶)和线粒体(甘氨酸脱羧酶和丝氨酸羟甲基转移酶)(见教材图10.8,B部分)(Hatch和Osmond,1976年;Tolbert,1981年;Bauwe等人,2010年)。
参考文献
Bauwe, H., Hagemann, M.,and Fernie, A. R. (2010) Photorespiration: players, partners and origin.Trends Plant Sci. 15(6): 330–336. doi: 10.1016/j.tplants.2010.03.006. Epub 2010 Apr 18. PMID: 20403720.
Hatch, M. D., and Osmond, C. B. (1976)Compartmentation and transport in C4photosynthesis.InTransport in Plants(Encyclopedia of Plant Physiology, New Series, vol. 3), C. R. Stocking and U. Heber, eds., Springer, Berlin, pp. 144–184.
Tolbert, N. E. (1981) Metabolic pathways in peroxisomes and glyoxysomes.Annu Rev Biochem. 50: 133–157. doi: 10.1146/annurev.bi.50.070181.001025. PMID: 7023357.
Web Topic 10.7 蓝细菌与Rubisco的加氧反应
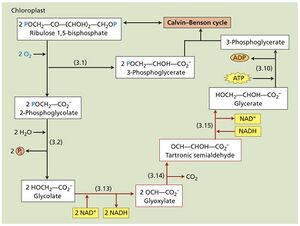
蓝细菌基因组编码植物C₂氧化光合碳循环的所有酶。光呼吸在第一批O₂生产者中的存在,表明这是一种与产氧光合作用密切相关的古老机制,是应对细胞内O₂的一种适应。尽管所有"类植物"光呼吸酶都存在,但现存的蓝细菌使用来自变形菌祖先的酶来回收在C₂氧化光合碳循环中损失的碳(网络图10.7.A和网络表10.7.A,反应1和2)。
最初,乙醇酸脱氢酶(网络表10.7.A,反应13)将光呼吸产生的乙醇酸转化为乙醛酸 [乙醇酸 + NAD⁺ → 乙醛酸 + NADH + H⁺]。
接下来,两种酶催化乙醛酸转化为甘油酸:
- 酒石酸半醛合酶 [乙醛酸 → 酒石酸半醛 + CO₂](见网络表10.7.A,反应14)
- 酒石酸半醛还原酶 [酒石酸半醛 + NADH + H⁺ → 甘油酸 + NAD⁺](见网络表10.7.A,反应15)
最后,蓝细菌的甘油酸激酶磷酸化甘油酸,产生重新进入卡尔文-本森循环的3-磷酸甘油酸 [甘油酸 + ATP → 3-磷酸甘油酸 + ADP](见网络表10.7.A,反应10)。
与陆地植物一样,蓝细菌的替代光呼吸循环释放一个碳原子(见网络表10.7.A,反应14),并将一个三碳骨架重新纳入卡尔文-本森循环(见网络表10.7.A,反应10)。该替代途径对ATP和还原剂的需求与陆地植物在C₂氧化光合碳循环中使用的不同,因为蓝细菌绕过了NH₄⁺的释放和再固定(比较教材图10.8C中的光呼吸净反应和网络表10.7.A)。

参考文献
Badger, M. R., and Price, G. D. (2003) CO2 concentrating mechanisms in cyanobacteria: Molecular components, their diversity and evolution. J. Exp. Bot. 54: 609–622.
Kaplan, A., Schwarz, R., Lieman-Hurwitz, J., and Reinhold, L. (1994) Physiological and molecular studies on the response of cyanobacteria to changes in the ambient inorganic carbon concentration. In The Molecular Biology of Cyanobacteria, D. Bryant, ed., Kluwer, Dordrecht, Netherlands, pp. 469–485.
Ogawa, T., and Kaplan, A. (1987) The stoichiometry between CO2 and H+ fluxes involved in the transport of inorganic carbon in cyanobacteria. Plant Physiol. 83: 888–891.
Web Topic 10.8 二氧化碳:一些重要的物理化学性质
理解 CO2 固定的机制需要了解 CO2 的物理和化学性质,特别是那些与其和水相互作用相关的性质。溶解在水中的任何气体量与其在溶液上方的分压 (P气体) 及其本生吸收系数 (α) 成正比。本生吸收系数是在 1 个大气压下,一体积水所吸收的气体体积,并且依赖于温度,温度升高时系数减小。
因此,气体的溶解度随着温度的升高而降低。于是,对于给定的温度,
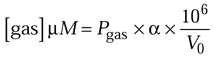
其中 V0 是标准温度和压力下理想气体的标准体积 (V0 = 22.4 L mol–1)。
我们可以通过将气体的摩尔分数乘以总压来计算气体的分压。气体的摩尔分数是其分体积除以所有存在气体的总体积。因此,空气中 CO2 和 O2 的摩尔分数分别为 0.0415%(参见教材图 11.18)和 20.95%。在海平面,大气压约为 0.1 MPa,因此 CO2 和 O2 的分压分别为 4.2 × 10–5 和 2.1 × 10–2 MPa。
根据这些数值以及 α 的数值,可以通过上面给出的方程计算出 CO2 和 O2 的相应溶液浓度。下表(网络表 10.8.A)给出了这些浓度在不同温度下的数值。
这些数值对羧化作用施加了相当大的限制。作为一种羧化酶,Rubisco 必须能够在即使 CO2 浓度相当低的情况下也能高效运行。Rubisco 在光呼吸中也起到加氧酶的作用,因此 O2 的溶液浓度也很重要。
由于本生吸收系数 α(CO2) 和 α(O2) 具有不同的温度依赖性,这两种气体的浓度随温度变化,使得 CO2 与 O2 的比率随着温度升高而降低。这种效应在生物学上很重要,因为随着温度升高,Rubisco 催化的羧化作用与加氧作用的比率降低,因此光呼吸与光合作用的比率增加。
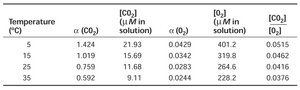
网络表 10.8.A CO2 和 O2 的溶解度作为温度的函数。
严格来说,大气 CO2 融入溶液包括两个反应:
溶解: CO2 (气体) → CO2 (水溶液)
和
水合: CO2 (水溶液) + H2O → H2CO3,K = 2 × 10–3。
相对于 CO2 (水溶液),H2CO3 的低比例以及实验上区分这些物种的困难,导致在亨利定律中将它们的浓度合并在一起。关于海洋和淡水中无机碳形态的进一步描述,可以参考 Lewis 和 Wallace(1998)开发的计算机程序。
参考文献
Lewis, E., and Wallace, D. (1998) Program developed for CO2 system calculations. ORNL/CDIAC-105. Carbon Dioxide Information Analysis Center, Oak Ridge National Laboratory, U.S. Department of Energy: Oak Ridge, TN.
Web Topic 10.9 C4 代谢的三种变体
历史上,已描述过基本 C4 生化途径的三种变体(网络图 10.10.A)。这些变体的主要区别在于运输到维管束鞘细胞的 C4 酸(苹果酸或天冬氨酸)以及脱羧方式。然而,最近的研究表明不同脱羧反应之间存在灵活性;因此,这三种亚型之间的区别可能不像曾经认为的那样分明(Wang 等,2014)。
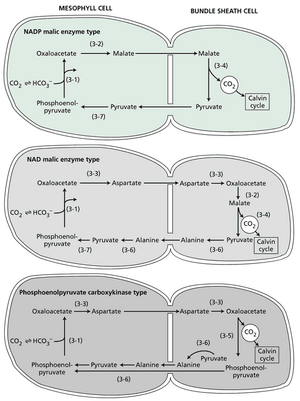
这些变体以催化各自脱羧反应的酶命名:叶绿体中发现的 NADP 依赖性苹果酸酶(NADP-ME);线粒体中的 NAD 依赖性苹果酸酶(NAD-ME);以及位于细胞质基质中的磷酸烯醇式丙酮酸羧激酶(PEP-CK)。文中讨论了NADP-ME类型(如甘蔗或玉米)的碳途径。
碳途径
所有C₄植物共有的初级羧化反应由PEP羧化酶催化,发生在叶肉细胞的细胞质基质中,并使用HCO₃⁻而非CO₂作为底物(见教材图10.10B,反应2)。在NADP-ME变体中,草酰乙酸在叶肉叶绿体中通过NADPH和NADP-苹果酸脱氢酶迅速被还原为苹果酸(见教材图10.10B,反应3)。形成的苹果酸进入维管束鞘细胞的叶绿体,并在那里进行氧化脱羧(见教材图10.10B,反应5),产生丙酮酸。在维管束鞘细胞内释放的CO₂通过卡尔文-本森循环转化为碳水化合物。
残留的C₃酸以丙酮酸形式运回叶肉,并在叶肉叶绿体中转化为磷酸烯醇式丙酮酸(见教材图10.10A和图10.10B,反应8)。该反应在所有三种C₄变体的叶肉叶绿体中发生。然后循环再次开始,磷酸烯醇式丙酮酸发生羧化产生草酰乙酸(Kanai and Edwards 2000)。
所有C₄植物中定位于叶肉叶绿体的另一个过程,是将3-磷酸甘油酸还原为磷酸丙糖,这在C₃植物叶绿体中是卡尔文-本森循环的固有部分。相反,所有C₄植物都将3-磷酸甘油酸从维管束鞘输出,以在叶肉叶绿体中进行还原。还原后,磷酸丙糖被运回维管束鞘叶绿体,用于那里的卡尔文-本森循环运作。
卡尔文-本森循环在维管束鞘和叶肉叶绿体之间如此显著分割的一个可能原因,是叶肉细胞具有更强的还原力,并有助于协调C₃和C₄循环之间的代谢活动。
参考文献
Kanai, R., and Edwards, G. E. (2000) The Biochemistry of C4 Photosynthesis, In: C4 Plant Biology, Eds: Rowan F. Sage, Russell K. Monson. Academic Press, pp. 49–87.
Wang, Y., Bräutigam, A., Weber, A. P., and Zhu, X. G. (2014) Three distinct biochemical subtypes of C4 photosynthesis? A modelling analysis. J Exp Bot. 65(13): 3567–3578. doi:10.1093/jxb/eru058.
Web主题 10.10 单细胞C4光合作用
在20世纪60年代阐明C4光合作用途径之后的许多年里,Kranz型叶片解剖结构一直是C4光合作用的代名词。21世纪初,在缺乏Kranz解剖结构的陆生植物中发现C4光合作用,揭示了C4碳固定机制的多样性远超之前的想象(Edwards等,2004)。有三个物种,一种生长在中亚(囊果碱蓬(Suaeda aralocaspica)),另外两种分布于从安纳托利亚向东至巴基斯坦地区(瘤果滨藜(Bienertia cycloptera)和波斯湾瘤果滨藜(B. sinuspersici)),能在单个绿色组织细胞内完成完整的C4光合作用(Sage,2002;Edwards等,2004)(见教材图10.11B)。此外,大量证据表明C4光合作用在被子植物之外也已演化出来。一些海洋大型藻类和重要的光能自养海洋原生生物(硅藻)也能在单个细胞内进行C4光合作用(Edwards等,2004)。
陆生单细胞C4光合作用
这些单细胞C4植物(均属藜科(Chenopodiaceae))能在单个绿色组织细胞内进行C4光合作用,是因为酶和叶绿体在同一细胞的两个区域分布不均。这一特性使细胞能够在Rubisco周围浓缩CO₂,从而最大限度地减少光呼吸(见教材图10.12B)。
在囊果碱蓬叶片中,叶绿素自发荧光的共聚焦显微镜观察显示,靠近维管束处有一层密集的叶绿体,而靠近与大气接触的叶片表面处叶绿体较少。此外,在囊果碱蓬子叶的绿色组织形成过程中,伴随着胞质酶PEPCase的合成以及在细胞两端二态性叶绿体的发育。靠近维管系统的叶绿体具有发育良好的基粒,含有Rubisco并储存淀粉;而位于远端的叶绿体基粒减少,含有丙酮酸-磷酸双激酶且缺乏淀粉。
大气CO₂的同化发生在绿色组织细胞中,胞质PEPCase催化HCO₃⁻掺入磷酸烯醇式丙酮酸形成草酰乙酸,后者是苹果酸的前体。四碳酸穿过一个无细胞器的胞质区域,扩散到靠近维管系统的细胞区域。在位于维管区域的线粒体中,NAD-苹果酸酶将苹果酸脱羧,释放CO₂和丙酮酸并生成NADH(见教材图10.10B,反应5)。CO₂被Rubisco和线粒体周围叶绿体中的卡尔文-本森循环捕获。形成的丙酮酸扩散回与大气接触的区域,在那里叶绿体丙酮酸-磷酸双激酶将丙酮酸转化为磷酸烯醇式丙酮酸。因此,这些细胞在细胞内模拟了经典的C4Kranz解剖结构的扩散路径,通过细胞器的定位作为适应性响应,以确保Rubisco周围有高浓度的CO₂。
参考文献
Edwards, G. E., Franceschi, V. R., and Voznesenskaya, E. V. (2004) Single-cell C4 photosynthesis versus the dual-cell (Kranz) paradigm. Annu. Rev. Plant Biol. 55: 173-196.
Sage, R. F. (2002) C4 photosynthesis in terrestrial plants does not require Kranz anatomy. Trends Biochem. Sci.7: 283-285.
Web主题 10.11 CAM植物的光呼吸
许多适应于炎热干旱、水资源稀缺地区的陆生植物,会受到强日照的严重影响,特别是干旱和高温。为了避免高水分散失率,这些物种的气孔在白天炎热时紧闭,而在夜间空气相对凉爽湿润时与周围大气进行大部分气体交换。另一方面,将CO₂固定到碳水化合物中的关键光合作用过程发生在白天。为了应对白天大气CO₂有效流入的不足,这些物种演化出一种不同的光合作用机制,称为"景天酸代谢"(CAM)。这个不寻常的过程发生在单个叶肉细胞内,其中大气CO₂的吸收和随后的同化涉及三个区室:细胞质、液泡和叶绿体(Bräutigam等,2017)。一般来说,CAM植物常见于暴露在白天高温和低相对湿度下的沙漠多肉植物(例如,仙人掌科(Cactaceae)),或因其气生生长习性而在湿润条件下暴露于生理性干旱的热带森林附生植物(凤梨科(Bromeliaceae))中。值得注意的是,CAM也出现在世界范围内沼泽和浅水栖息地、存在CO₂日间限制的水生植物(水韭科(Isoetaceae))中。
在凉爽的夜间,开放的气孔促进大气中的CO₂吸收,CO₂扩散进入细胞质中,生成HCO₃⁻(参见第8章)。在此阶段,磷酸烯醇式丙酮酸羧化酶(PEPCase)催化HCO₃⁻与磷酸烯醇式丙酮酸结合,生成草酰乙酸和相关的四碳有机酸(尤其是苹果酸),这些物质积累在液泡中。在白天的炎热时段,陆地CAM植物的气孔关闭特征减少了水分流失,但导致了内部CO₂短缺。为克服这一不足,液泡将苹果酸释放到细胞质中,在脱羧酶——NADP-苹果酸酶或PEP羧激酶的作用下,产生丙酮酸和CO₂。在叶绿体基质内部,Rubisco将释放的CO₂结合到3-磷酸甘油酸中,该过程与通过光合磷酸化在光下合成的ATP和NADPH协同,启动一系列卡尔文-本森循环反应,导致淀粉的积累。苹果酸的夜间形成与储存,以及白天的脱羧作用及随之而来的质体淀粉积累,在24小时的光周期内发生时间上的分离。基于这种时间性,CAM包含四个代谢阶段,涵盖了同一细胞环境中C₄(PEPCase)和C₃(Rubisco)羧化作用的调节。夜间通过PEPCase吸收大气CO₂形成C₄酸(阶段I)和白天苹果酸脱羧以引发内部CO₂浓度升高(阶段III),这两个阶段之间穿插着清晨(阶段II)和傍晚(阶段IV)的净CO₂吸收过渡期,此时PEPCase和Rubisco介导的羧化作用共同促进CO₂的同化。在这一昼夜节律中,夜间通过PEPCase或白天通过Rubisco吸收CO₂的比例受以下因素控制:
- 气孔功能
- 有机酸和储存碳水化合物含量的波动
- 参与初级(PEPCase)和次级(Rubisco)羧化作用以及有机酸脱羧作用(例如苹果酸酶或PEP羧激酶)的酶的活性
在白天的阶段III,关闭的气孔阻止了与外部大气的气体交换,但光合作用及其他生命过程仍在继续。此阶段,由于活跃的卡尔文-本森循环,内部CO₂水平急剧下降;然而,这种下降被线粒体呼吸作用所抵消。气孔的关闭也导致O₂在叶肉细胞中积累,因为光合作用产生O₂的速率高于线粒体呼吸及其他消耗O₂的反应。在此阶段,Rubisco的加氧酶活性激活了光呼吸循环,通过该循环,卡尔文-本森循环回收了75%转化为乙醇酸的碳,剩余的25%作为CO₂被线粒体甘氨酸脱羧酶复合体释放(参见第10章)。因此,关闭的气孔提供了一种适应性优势,通过蒸腾作用最大程度地减少叶片水分流失,并维持基质CO₂浓度足以进行碳同化。然而,O₂的随之积累是一个主要的不利后果,因为作为一种强氧化剂,O₂与其他分子反应并产生有害的自由基(例如超氧化物、氢氧根离子),这些自由基可能引发对DNA、蛋白质和脂质的不可控有害反应(参见第7、9、15章及Web Topic13.7)。
在此情况下,光呼吸通过消耗基质和过氧化物酶体中的O₂,有助于缓解O₂积累的不良后果。光呼吸循环单轮中释放1摩尔CO₂需要连续消耗:(a)叶绿体基质中Rubisco加氧酶活性消耗2摩尔O₂(参见教材图10.8,反应1),以及(b)过氧化物酶体中乙醛酸氧化酶和过氧化氢酶在小型氧循环中协同作用消耗1摩尔O₂(参见教材图10.8,反应3和4)。由核酮糖-1,5-二磷酸驱动的光呼吸循环 {2 Ribulose-1,5-bisphosphate + 3 O₂ + H₂O + ATP → 3 3-phosphoglycerate + CO₂ + 2 Pi + ADP} 比利用碳水化合物的线粒体呼吸 {C₆H₁₂O₆(例如葡萄糖)+ 6 O₂ → 6 CO₂ + 6 H₂O} 需要消耗更多的O₂。因此,每释放1摩尔CO₂,分别消耗3摩尔与1摩尔O₂。因此很明显,阶段III中CAM光呼吸的有益结果不仅包括避免因乙醛酸形成造成的碳损失,还包括通过清除活性氧减轻氧化应激。这种氧化应激的缓解被认为是CAM进化中的一个主要驱动力(Lüttge 2004)。
参考文献
Bräutigam, A., Schlüter, U., Eisenhut, M., and Gowik, U. (2017). On the Evolutionary Origin of CAM Photosynthesis. Plant Physiology 174(2): 473-477. https://doi.org/10.1104/pp.17.00195
Lüttge, U. (2004). Ecophysiology of Crassulacean Acid Metabolism (CAM). Annals of Botany 93(6): 629-652. https://doi.org/10.1093/aob/mch087
Web Topic 10.12 淀粉颗粒结构
Andreas Blennow, 植物与环境科学系,哥本哈根大学,丹麦哥本哈根(2021年9月)
植物中的淀粉是一种颗粒状、半晶质的多糖,储存于许多植物器官中,如叶片、籽粒、块茎和根。大量研究导致这样一种观点:这种多糖的结构最好在四个不同层面进行观察,即分子层、片层、块状层和颗粒层。尽管淀粉几乎完全由葡萄糖单元组成,但颗粒的组成、形状和大小取决于植物来源。
支链淀粉和直链淀粉紧密堆积在淀粉颗粒中
颗粒质量的主要部分,约98–99%,是一种复杂的同质多糖,由两种组分组成:主要是通过α-D-1,4糖苷键连接的线性链的直链淀粉,以及除此外还通过α-1,6糖苷键分支的支链淀粉。α-D-1,6糖苷键在总键数中的比例在直链淀粉中较低(低于1%),在支链淀粉中则较为广泛(约5–6%),分别形成了基本上是线性和分支的同质多糖。直链淀粉相对伸展且分子量较低(500–20,000个葡萄糖单元),而支链淀粉是自然界最大的分子之一(约10⁶个葡萄糖单元),形状更有序。
天然淀粉颗粒(网络图10.12.A)因其直链淀粉(10–30%)和支链淀粉(70–90%)的不同比例而在不同来源中差异很大。然而,更重要的是,直链淀粉与支链淀粉的比例定义了超分子的淀粉颗粒中支链淀粉规则半晶阵列的结构。在叶绿体(存在于光合组织中)和造粉体(存在于异养组织中,如种子、谷物、根和块茎)中,直链淀粉和支链淀粉被组织在相对致密的球状颗粒中,直径通常在1至50 μm范围内,形状和大小各异。在光学显微镜下观察时,大多数颗粒显示出同心层,这些层源自内部纳米尺寸的片层结构,构成了交替的半晶态和无定形层。据认为,生长环由交替的较小(更无定形或无序)层和较大(更结晶且有序)的砌块组成。扫描微聚焦X射线技术证据表明,这些结构可能以超螺旋实体的形式存在(Tang等人,2006年)。

淀粉颗粒中链序的骨架模型和砌块模型
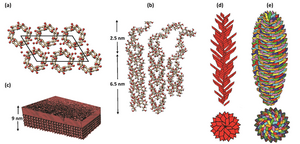
与许多蛋白质不同,对于淀粉等多糖,不存在精确的结构模型。然而,基于多年来收集的数据,一种关于淀粉颗粒中链如何组织的新模型正在出现,即所谓的“骨架模型backbone model”(网络图10.12.B)。该模型在分子和纳米水平上描述了淀粉颗粒内的分子和组装结构,并涵盖了目前观察到的所有已知结构和物理现象,包括其在热水中的溶胀。淀粉颗粒的这种表示包括存在长链形成的骨架,构成长链骨架的二维片层,较短的成晶片段(crystal-forming segments)从这些片层伸出(网络图10.12.B)。这些片段彼此随机分布,可以形成平行的双螺旋并结晶。一个这样的骨架/双螺旋层构成一个9纳米厚的片层,这些片层在淀粉颗粒中构建出同心结构。
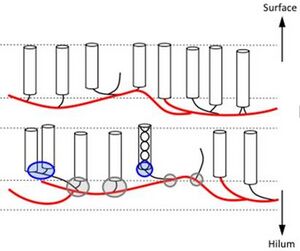
在颗粒和亚颗粒水平上,Karl Wilhelm von Nägeli于1858年提出,淀粉的有组织单元被组织程度较低的材料包围并结合在一起,而在1937年,Nicolaas P. Badenhuizen首次描述了由嵌入无定形材料中的晶态单元构成的结构。这些易受部分酶水解的淀粉单元导致了当前的“砌块(blocklet)”概念(最初称为“blöckchen Strüktur”;Buléon等人,1998年)。砌块是介于大分子和大型淀粉颗粒组织之间的超分子结构(网络图10.12.B)。
对切片淀粉的透射电子显微镜图像的重建揭示了直径约20至500纳米的近似椭球区域。这些结构是由砌块内交替的半晶态和无定形支链淀粉片层叠加形成的。一个砌块由几个半晶态片层组成(如上文骨架模型所述)。这些片层的支化、无定形部分也包含直链淀粉分子和脂质。通常,一些支链淀粉分子松散组装,干扰半晶态阵列并在无定形环中引起“缺陷”。这两类砌块群,“正常”和“缺陷”,在淀粉颗粒的径向生长中规律地交替出现,产生两种不同的形成物:异质层和均质层。因此,支链淀粉在砌块的结构中起着主要作用,而包括直链淀粉、脂质和蛋白质在内的其他组分调节整个淀粉颗粒的强度和柔韧性(Tang等人,2006年)。已发现结晶度较低的部分比较结晶的部分更容易被淀粉酶消化。淀粉对酶攻击的差异反应清楚地表明,半晶层的结构调节了水解酶的催化能力。
一个最近的模型(网络图10.12.C)试图解释淀粉颗粒所有层次的层级结构,并提出了一些控制这些结构形态发生的一般规则。有趣的是,所谓的“叶序样”特征(灵感来源于植物器官围绕中心轴的排列)出现在淀粉颗粒从纳米到微米级的尺度上。这种结构遵循斐波那契黄金角,形成几个所谓的“黄金螺旋”。一个黄金螺旋椭球体可以用由平行链葡聚糖双螺旋组成的元素构建,显示出形状、大小和高致密性,让人联想到上述描述的砌块(网络图10.12.C)。
为明日世界利用淀粉
淀粉是自然界和人类社会最重要的植物产品之一。其生物合成在作物器官(如植物块茎(例如,马铃薯)和种子胚乳(例如,玉米、小麦、水稻))中已得到极大提高。淀粉目前是人类热量摄入的最大来源,也是工业生产过程(如粘合剂和可生物降解塑料)的重要资源。
由于紧密堆积和结晶性,淀粉颗粒不允许过多水分进入,因此不溶于冷水。然而,当温度升高时,结晶区域开始分离成溶胀的无定形形式,这一过程称为糊化(Damager 等人,2010)。这个过程指的是水和热的协同作用使淀粉分子的分子间键水合,驱动氢键位点(羟基氢和氧)结合更多的水,特别是在结晶区域,同时导致整个颗粒结构的无序性增加。糊化能力以及随后的胶凝作用是食品和材料加工及质地控制中的重要现象,包括烘焙糕点、白酱汁和蛋奶冻,以及为生物塑料、化学、制药和纺织工业生产原材料。
因此,要改善这些活动,必须实现两个方面:充足的产量以养活世界,以及满足特定用途的独特品质。前者依赖于育种工作以实现稳定高产和高效耕作,但两者的责任都落在整个加工链上,这同样体现在食品和化学工业中。因此,未来的挑战将是培育改良品种,以可持续的方式养活世界。新的育种技术,特别是利用Crispr-Cas9精确基因编辑技术(Bennett 等人,2020),目前正在迅速发展。预计这些策略将对提高产量、增强稳健性以及开发用于各种淀粉应用的新型淀粉类型产生重大影响。
参考文献
Bennett, E. P., Petersen, B. L., Johansen, I. E., Niu, Y., Yang, Z., Chamberlain, C. A., Met, Ö., Wandall, H. H., and Frödin, M. (2020) INDEL detection, the ‘Achilles heel’ of precise genome editing: a survey of methods for accurate profiling of gene editing induced indels. Nucleic Acids Research 48(21): 11958–11981.
Bertoft, E. (2017) Understanding starch structure; recent progress. Agronomy 7: 56.
Spinozzi, F., Ferrero, C., and Perez, S. (2020) The architecture of starch blocklets follows phyllotaxic rules. Scientific Reports 10: 20093. https://doi.org/10.1038/s41598-020-72218-w
Tang, H., Mitsunaga, T., and Kawamura, Y. (2006) Molecular arrangement in blocklets and starch granule architecture. Carbohydrate Polymers 63(4): 555–560.
