第二章Web Topic
Web Topic 2.1 多糖化学术语
多糖根据其含有的主要糖来命名。例如,葡聚糖(glucan)是由葡萄糖组成的聚合物;木聚糖(xylan)是由木糖组成的聚合物;半乳聚糖(galactan)是由半乳糖组成的聚合物。
对于支链多糖,多糖的主链通常由名称的最后部分给出。因此,木葡聚糖(xyloglucan)具有一个葡聚糖主链(一条葡萄糖残基的线性链),木糖作为侧链连接其上;阿拉伯木聚糖(arabinoxylan)具有一个木聚糖主链(由木糖单体组成),带有阿拉伯糖侧链。然而,复合名称不一定意味着支链结构。例如,“葡甘露聚糖(glucomannan)”是指主链中同时含有葡萄糖和甘露糖的聚合物名称。由于糖可以呈现多种形式并以多种方式连接,糖的命名法并不简单,在此简要总结。
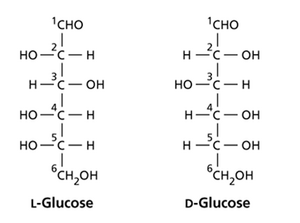
单糖是具有经验式(CH2O)n的多羟基醛或酮。它们通常含有一个不对称碳原子,因此可以作为两种立体异构体存在,被指定为D或L对映异构体(网络图2.1.A)。
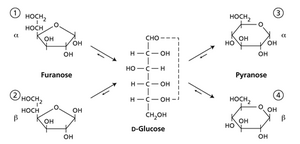
单糖通常形成环状结构,而不是线性结构,因为羰基氧可以与羟基反应,通常形成五元环(呋喃糖环)或六元环(吡喃糖环)。这些环有一个新的手性中心,可能呈现两种形式,指定为α或β异头物。因此,β-D-吡喃葡萄糖是D-葡萄糖以β构型形成的六元环形式(网络图2.1.B)。在溶液中,单糖自由变旋(在α或β异头物之间转换);当在聚合物中连接时,异头构型是稳定的。
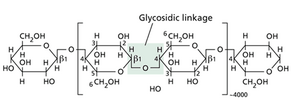
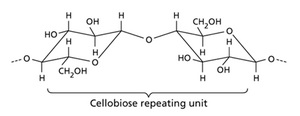
多糖中的糖通过O-糖苷键连接在一起。我们通过指定糖苷键连接的碳原子来指示连接模式。例如,在纤维素中,碳原子1与相邻葡萄糖残基中的碳原子4连接。因此,纤维素被指定为(→4)β-D-葡聚糖,因为它是由β-D-葡萄糖分子通过碳1和碳4连接而成的链(网络图2.1.C)。它也可以被称为(→4)连接的β-D-吡喃葡萄糖的聚合物。
Web Topic 2.2 细胞壁的基质成分
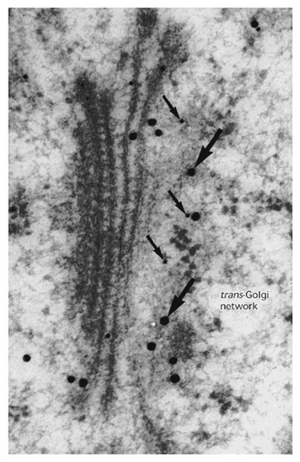
Web Topic 2.3 细胞壁的力学特性:以丽藻属(Nitella)进行的研究
典型植物细胞的小尺寸(20 至 100 µm)一直是研究细胞壁力学特性的严重障碍。为了测量高等植物离体细胞壁的伸展性,研究人员必须将整个冷冻和解冻的器官或组织置于伸长仪中,如教科书图 14.18 和 14.19 所示。虽然此类测量可以提供定性答案,但所测得的伸展性无法以定量方式与活细胞的生长相关联,因为施加的应力是单轴的(单向的),而由膨压引起的体内应力是多轴的(多方向的)。

淡水绿藻丽藻属(Nitella)和轮藻属(Chara)的巨大节间细胞在离子运输、水渗透性和细胞质流动的经典研究中占有突出地位(Hope and Walker 1975)。这些藻类的特征是具有直立的、分枝的合胞体(多核)丝状体,分化为节和节间,每个节上生有一轮特化的侧生节间(网络图 2.3.A)。
节间细胞起始于长 20 mm 的短圆盘,成熟时伸长成约 6 cm 长、0.5 mm 宽的细长圆柱体。细胞通过以纵向为主的弥散性生长进行扩展。由于单个节间细胞体积巨大,可以分离其细胞壁,并测量其力学特性。甚至可以使用多轴应力来模拟体内膨压,从而研究单个细胞壁的各向异性(不等同的)力学特性。
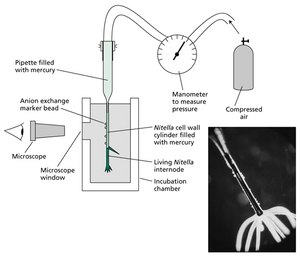
网络图 2.3.B 展示了研究丽藻属(Nitella)节间细胞多轴伸展性的实验装置。将空的细胞壁圆筒粘到移液管上,并在压力下用汞进行充胀。液态汞在这些条件下不溶解,因此是惰性的。为了响应加压汞引起的多轴应力,细胞壁圆筒发生膨胀,研究人员可以通过水平显微镜观察该过程(网络图 2.3.C),监测其长度和宽度的扩展情况(Metraux 等人,1980)。
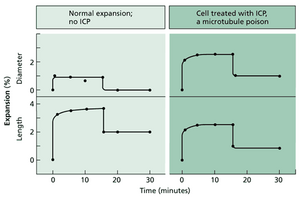
利用丽藻属(Nitella)节间的多轴应力程序,可以使用微管抑制剂改变纤维素微纤维的排列方向,并验证微纤维排列方向决定细胞壁力学各向异性的假说。如网络图 2.3.C 所示,对照细胞的多轴伸展是高度各向异性的。不仅长度伸展是直径伸展的四倍,而且长度伸展的大部分是不可逆的,而直径的伸展则几乎是完全可逆的。
这些结果与细胞的各向异性生长模式一致。网络图 2.3.C 还显示了用微管毒剂异丙基 N-苯基氨基甲酸酯(IPC)预处理细胞的效果,该物质与秋水仙素类似,能诱导纤维素微纤维在细胞壁中的随机沉积。结果是细胞壁在长度和直径上的伸展大致相等,这与该抑制剂诱导的等轴生长模式一致。
丽藻属也被证明可用于研究体内(in vivo)细胞壁特性。应用于当代细胞膨胀生物物理控制研究的许多概念,都源于斯坦福大学的保罗·格林(Paul Green)及其同事对活体丽藻属细胞的开拓性实验(Green 1968)。此类研究得出的一个重要见解是,细胞壁内层 25% 的部分决定了细胞膨胀的极性。
利用纤维素微纤维是晶体结构、在偏振光下表现出双折射的特性,加州太平洋大学的保罗·里士满(Paul Richmond)设计了一种光学技术,可以同时测量细胞的长度膨胀和直径膨胀以及细胞壁中纤维素微纤维的排列方向(Richmond 1983)。该技术使得确定微纤维角度与细胞膨胀方向之间的关系成为可能。
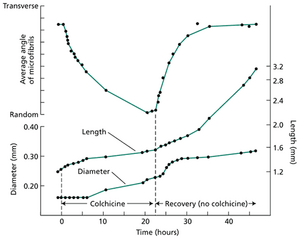
如网络图 2.3.D 所示,将秋水仙素加入生长培养基后,微纤维角度几乎立即开始从横向变为随机。然而,生长的各向异性直到大约 8 小时后才开始改变。从各向异性生长向等轴生长的转变,在细胞表面积相对增加约 25% 后完成。
由于在此期间持续的细胞壁合成使壁厚保持恒定,我们可以推断,当细胞壁内侧25%的部分被替换时,细胞膨胀的方向性发生了改变。因此,细胞壁内侧25%的部分似乎代表了细胞壁的承重部分。这意味着,外侧75%的细胞壁因拉伸而变得过于脆弱,从而无法限制细胞膨胀。
参考文献
Green, P. B. (1968) Cell morphogenesis.Annu. Rev. Plant Physiol. 20: 365–394.
Hope, A. B., and Walker, N. A. (1975)The Physiology of Giant Algal Cells. Cambridge University Press, London.
Metraux, J-P., Richmond, P., and Taiz, L. (1980) Control of cell elongation inNitellaby endogenous cell wall pH gradients. Multiaxial extensibility and growth studies.Plant Physiol.65: 204–210.
Richmond, P. A. (1983) Patterns of cellulose deposition and rearrangement inNitella: In vivo analysis by birefringence index.J. Appl. Polym. Sci. 37: 107–122.
Taiz, L., Metraux, J.-P., Richmond, P. A. (1981) Control of cell expansion in theNitellainternode.Cytomorphogenesis in Plants, ed. O. Kiermeyer, pp. 231-264. Vienna: Springer-Verlag.
