氨基酸的化学反应
氨基酸的化学反应
一、α-NH2参与的反应
1. 伯胺特征的反应:黄色反应
Cα-NH2 + HNO2 → Cα-OH + H2O + N2↑
每分子N2中有一个原子来自α-NH2,此反应是Van-Slyke[定氮]法测量氨基酸含量的基础。Lys和AECys的伯胺基也可发生此反应,但相对较慢。
2. 酰基化反应:去质子化的—NH2与酰氯或酸酐反应
机理:氨基氮对亲电的羰基碳的进攻。
a. 与丹磺酰氯(DNS-Cl)反应
产物DNS-aa是强烈的荧光分子。若使用DNS-Cl代替DNFB进行Sanger反应,则为DNS-Cl-Sanger法,仅需微量样品即可测定肽链的N端aa残基。
b. 其他
常见的还有苄氧酰氯酯(Z-酯)、邻苯二甲酸酐等。保护剂Boc-酯(酸性下脱去)、Fmoc酯(碱脱)用于肽的固相合成。
3. 烃基化反应
机理:氨基氮对亲电的C—X进攻,取代反应。
a. 与DNFB/FDNB(2, 4-二硝基氟苯)
与DNFB/FDNB(2, 4-二硝基氟苯)即Sanger试剂反应,生成黄色的DNP-aa。做正相层析分离,然后和标准DNP-aa做对比,可知N端aa。
b. 与PITC(苯异硫氰酸酯)反应
与PITC在pH = 8.3形成PTC-aa,然后在无水强酸中环化为PTH-aa。PTH-aa即可分析。
如果肽链的N端氨基参与了PITC反应,生成PTH-肽,那么它可以在无水HF中进行环化断裂,生成PTH-aa和N端少一个氨基酸的肽链。抽提PTH-aa后可重复反应,即为Edman降解法。
已有自动化的Edman降解法测序仪,速率约40 min/aa,每轮转化率可达99.9%,约能测50个aa残基。
4. 与醛类的加成
---CHO + H2N--- → ---CH=N---
a. 与甲醛的反应
---NH3+ → ---NH2 + H+ HCHO→ ---NHCH2OH HCHO→ ---N(CH2OH)2
氨基酸的α-COOH和α-NH2的pK值偏离常见指示剂太远,不容易滴定。当加入过量甲醛时,平衡右移,n(H+) = n(---NH3+)0,此时的α-NH2表观pK值刚好落在酚酞的指示范围内,可以通过滴定H+测量原游离氨基的浓度,进而判读肽链水解或合成的速度。
b. 与PLP反应:转氨基反应的重要原理
5. 脱氨基反应
反应形成α-酮酸,是aa分解的一个重要步骤。
6. 与荧光胺反应
生成产物具有强烈荧光性质,可分析ng级别的aa。
二、α-COOH参与的反应
1. 成酯/成盐反应
当---COOH与钠、钾成盐或成短脂肪酸酯时,其反应活性降低而α-氨基活性升高,用于羧基的保护和氨基的活化。(因此,涉及α-NH2的反应大多在碱性下进行,一方面是因为碱性环境下氨基的亲核性能变好,另一方面则出于此乎)
2. 成酰氯/叠氮化反应
当氨基被保护,羧基可与PCl5或二氯亚砜等反应生成酰氯,或者通过其他方式被叠氮化,即被活化,可用于肽的固相合成等。
三、α-COOH和α-NH2共同参与的反应
1. 与水合茚三酮反应
水合茚三酮 + +H3NCHRCOO- Δ→ NH3↑ + CO2↑ + RCHO + H+ + 还原茚三酮
NH3 + 还原茚三酮 + 水合茚三酮 → 紫色共振复合物
可测量570 nm处的吸收峰检验aa含量。Pro&Hyp在第一步即生成黄色化合物,并无法进行第二步。
2. 成肽
a. 2Gly 热乙二醇→二酮吡嗪
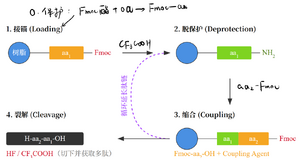
b. 肽的固相合成
如图(包括作者手写文本和AI生成的.svg文件截出的位图)。常用的保护基就是Fmoc基、Boc基等。
四、R基参与的反应
1. Tyr:酚基
a. 邻位亲电取代
碘化、硝化,如形成甲腺原氨酸。
b. Pauly反应
邻位上和对氨基苯磺酸的重氮盐形成橘黄色化合物。(His也行)
c. Millon反应
与热的Hg(NO3)2的亚硝酸溶液反应,生成红色化合物。
d. Ehrlich反应
与对二甲基氨基苯醛的盐酸溶液反应,生成蓝色化合物。
e. Salkowski黄蛋白反应
与沸浓硝酸形成黄色化合物。(Phe也可)
2. His:咪唑基
a. Pauly反应
与重氮苯磺酸形成红色化合物。*(Tyr也行)
*:据杨荣武老师的数字资源,这反应的产物是樱红色的,不过某老师讲义认为是棕红色的。但大约没有神经病会在这种地方设题。
b. 配位
组氨酸的咪唑氮具有孤对电子,可与空电子轨道配位,例如Ni+(此即固定化金属阳离子层析的原理),或其他某些过渡金属离子。
3. Arg:胍基
a. Sakaguchi(坂口)反应
与α-萘酚和次氯酸钠/次溴酸钠生成桃红色物质。
b. 与环己二酮反应
与环己二酮可逆缩合。
4. Met:甲硫基
a. 与一碘甲烷反应
---S-CH3 + CH3I → ---S+(CH3)2 + I- (可逆地生成锍盐。若用标记的CH3I进行此反应,则一轮可逆反应后标记的C有50%的可能留在Met中,可以用于标记Met)
5. Trp/Tyr:Floin-Ciocalteu反应/Folin-酚反应
还原磷钨酸盐和磷钼酸盐,产生蓝色的钨蓝和钼蓝。
6. Trp:吲哚基
a. 水合乙醛酸反应/Hopkins-Cole反应
与水合乙醛酸的硫酸溶液反应,生成紫色物质。
b. 与对二甲基氨基苯甲醛反应
生成蓝色物质。
7. Phe
a. Salkowski黄蛋白反应
与沸浓硝酸形成黄色化合物。
8. Cys:巯基
a. 电离:活化
b. 硫醇-二硫化物交换
c. 与氮丙啶(乙撑亚胺)反应
生成AECys,具有ε-氨基,可被胰蛋白酶切割。
d. 配位
例如一些R-Hg+型一价有机汞试剂,可使一些Cys硫蛋白变性。
e. 氧化
i. 空气氧化:—SH + —SH → —S—S—
ii. 强氧化剂氧化:—SH or —S—S— → —SO3—(磺基丙氨酸)
f. 烃基化:与卤代烃及其衍生物反应
例:---S- + ICH2CH3 → ---SCH2CH3 + I-。
本文主要参考了作者的大脑(这很不靠谱)、王镜岩等的《生物化学》上册第三版、杨荣武主编的《生物化学原理》第四版。
P.S. 由于作者非常菜,并且化学非常不好,机理之类属实无能为力,有问题在所难免,麻烦大家纠正。
图片使用了Times New Roman和Google和Adobe开发的思源宋体。
