其他受体及其信号转导:修订间差异
小无编辑摘要 |
无编辑摘要 |
||
| 第74行: | 第74行: | ||
Wnt 信号也参与调节胰岛素敏感性。胰岛素通过促进细胞膜上葡萄糖转运蛋白的表达,增强细胞对血糖的摄取。该过程部分依赖 Wnt/β-连环蛋白信号。特别是 Wnt10b,可提高骨骼肌细胞的胰岛素敏感性。 | Wnt 信号也参与调节胰岛素敏感性。胰岛素通过促进细胞膜上葡萄糖转运蛋白的表达,增强细胞对血糖的摄取。该过程部分依赖 Wnt/β-连环蛋白信号。特别是 Wnt10b,可提高骨骼肌细胞的胰岛素敏感性。 | ||
= Hedgehog 信号通路 = | |||
[[Image:Denticlebands.png|thumb|right|正常幼虫与 Hedgehog 图片幼虫。]] | |||
Hedgehog 信号通路负责向胚胎细胞传递其正常细胞分化所需的信息,存在于所有两侧对称动物中。胚胎的不同部位具有不同浓度的 Hedgehog 信号蛋白。该通路在成体中也发挥作用。 | |||
该通路得名于其多肽配体,即一种在果蝇属果蝇中发现、名为 Hedgehog(Hh)的细胞间信号分子;缺失 Hh 基因的果蝇幼虫据称形似刺猬。Hh 是果蝇体节极性基因产物之一,参与建立果蝇身体蓝图的基础。该分子在胚胎发生后期以及变态发育过程中仍然十分重要。 | |||
哺乳动物具有三种 Hedgehog 同源物,即 Desert hedgehog(DHH)、Indian hedgehog(IHH)和 Sonic hedgehog(SHH),其中 Sonic hedgehog 研究最为充分。在缺失该通路组成成分的基因敲除小鼠中,脑、骨骼、肌肉系统、胃肠道和肺均不能正常发育。近期研究指出,Hedgehog 信号在调控成体干细胞方面发挥作用,而这些干细胞参与成体组织的维持与再生。 | |||
== 果蝇 == | |||
=== 机制 === | |||
[[File:HedgehogCiR.svg|thumb|left|'''图1'''. 当 Hh 未与 Patched (PTCH)结合时,CiR 转录抑制因子的产生。]] | |||
[[File:HedgehogActive.svg|thumb|right|'''图2'''. 当 Hh 与 Patched (PTCH) 结合时,Ci 蛋白能够在细胞核内作为转录因子发挥作用。]] | |||
昆虫细胞表达一种全长锌指转录因子 Cubitus interruptus(Ci)。Ci 可与类驱动蛋白 Costal-2(Cos2)形成复合体,并与细胞微管结合,定位于细胞质中(图 1)。包括 PKA、GSK3β 和 CK1等激酶将 Ci 磷酸化,使其结合 SCF 复合体(果蝇蛋白 Slimb)。155 kDa 的全长 Ci 蛋白被靶向至依赖蛋白酶体的裂解过程,从而生成一个 75 kDa 的片段,即 CiR。CiR 在细胞内积累,并扩散进入细胞核,在那里作为 Hedgehog(Hh)靶基因的共抑制因子发挥作用。 | |||
在没有 Hh 的情况下(图 1),一种名为 Patched(PTCH)的细胞表面跨膜蛋白会阻止一种七次跨膜受体 Smoothened(SMO)的高水平表达和活性。当细胞外存在 Hh 时(图 2),Hh 会与 Patched 结合并抑制 Patched,从而使 Smoothened 得以积累,并抑制 Ci 蛋白的蛋白水解性裂解。 | |||
在具有 Hh 作用后的 Patched 的细胞中,完整的 Ci 蛋白会在细胞质中积累,而 CiR 水平下降,从而允许某些基因发生转录,例如 decapentaplegic,即 dpp,BMP 生长因子家族的成员。对于另一些受 Hh 调控的基因而言,其表达不仅需要 CiR 的消失,还需要未被裂解的 Ci 发挥积极作用,作为转录激活因子参与调控。 | |||
[[File:Wingless and Hedgehog reciprocal signaling during segmentation of Drosophila embryos.svg|thumb|right|[[#Wnt 信号通路|Wingless]] 和 Hedgehog之间的相互作用]] | |||
=== 作用 === | |||
Hedgehog 在果蝇发育中主要参与幼虫体节形成和成体附肢发育。在胚胎体节形成过程中,表达转录因子 engrailed 的细胞同时表达 Hedgehog(图中绿色所示)。当 Hedgehog 以这种局部方式发挥作用时,它是一种旁分泌因子。只有位于 engrailed 表达细胞一侧的细胞,才具备在 Hh 与受体蛋白 Patched 相互作用后对 Hedgehog 作出反应的能力(图中蓝色所示)。 | |||
邻近细胞在接收到 Hedgehog 信号后,会通过受体 Patched 被激活,并进一步诱导 Wingless 蛋白的表达(图中红色所示)。Wingless 属于 Wnt 家族信号蛋白,能够通过其受体 Frizzled 作用于相邻细胞,稳定 engrailed 的表达条带。Hedgehog 与 Wingless 之间形成相互调控,共同维持副体节边界(图上部),并建立体节前后轴上的位置编码,从而决定不同部位的解剖学特征。 | |||
在变态发育过程中,Hedgehog 与 Wingless 协同调控翅的形成。Hedgehog 还参与眼、脑、性腺、肠道和气管等器官的发育。其表达下降可能与某些动物眼部发育减弱有关。 | |||
2026年5月16日 (六) 17:31的版本
前言
本篇是信号转导系列的第三篇,也是末篇——其他受体及其信号转导。
- 前篇:酶联受体及其信号转导
Wnt 信号通路

Wnt 信号通路既可通过邻近细胞之间的通信发挥作用,即旁分泌,也可通过同一细胞内部的通信发挥作用,即自分泌。
目前已鉴定出三种 Wnt 信号通路:经典 Wnt 通路、非经典平面细胞极性通路,以及非经典 Wnt/钙通路。这三种通路均由 Wnt 蛋白配体与 Frizzled 家族受体(Fz)结合而激活,随后该受体将生物信号传递给细胞内的 Dishevelled 蛋白(Dsh)。经典 Wnt 通路主要导致基因转录的调控。非经典平面细胞极性通路调控细胞骨架,而细胞骨架负责维持和改变细胞形态。非经典 Wnt/钙通路则调控细胞内的钙水平。
Wnt 信号最早因其在癌发生中的作用而被识别,随后又因其在胚胎发育中的功能而受到关注。它所控制的胚胎发育过程包括体轴模式形成、细胞命运决定、细胞增殖和细胞迁移。这些过程对于骨、心脏和肌肉等重要组织的正常形成是必需的。Wnt 信号还调控成年骨髓、皮肤和肠道中的组织再生。
蛋白
Wnt 由一类多样化的分泌型、经脂质修饰的信号糖蛋白组成,其长度为 350–400 个氨基酸。所有 Wnt 蛋白的脂质修饰形式,都是对一个完全保守的半胱氨酸残基进行棕榈油酸化修饰。棕榈油酸化是必需的,因为 Wnt 需要借此与其载体蛋白 Wntless(WLS)结合,从而被运输至质膜并完成分泌;同时,这一修饰也使 Wnt 蛋白能够与其受体 Frizzled 结合。Wnt 蛋白还会发生糖基化,即连接糖类基团,以确保其正常分泌。
信号转导
共用的上游通路
信号传导始于 Wnt 蛋白与 Frizzled(Fz)家族受体 N 端胞外富含半胱氨酸结构域的结合。Fz 受体七次跨膜,构成一类独特的 GPCRs。结合往往还需要共受体的参与。例如,低密度脂蛋白受体相关蛋白 5/6(LRP5/6)、受体酪氨酸激酶(RTK)以及 ROR2 等,均可作为相关共受体。
受体被激活后,信号通过 Fz 与 Dsh 之间的直接相互作用,传递至细胞质中的磷蛋白 Dishevelled(Dsh)。Dsh 蛋白具有以下高度保守的蛋白结构域:N 端 DIX 结构域、中央 PDZ 结构域,以及 C 端 DEP 结构域。
经典通路与非经典通路
三条 Wnt 信号通路:经典 Wnt 通路、非经典平面细胞极性通路,非经典 Wnt/钙通路。经典通路与非经典通路的区别在于,经典通路 依赖 β-连环蛋白(β-catenin),而非经典通路则不依赖 β-连环蛋白发挥作用。

经典通路
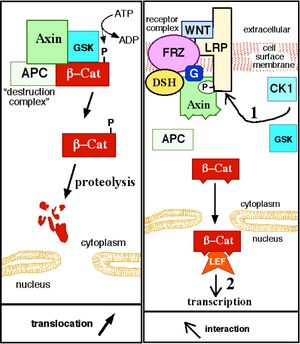
经典 Wnt 通路,即 Wnt/β-catenin 通路,机制为使 β-catenin 在细胞质中积累,并最终转位进入细胞核的 Wnt 通路。进入细胞核后,β-连环蛋白作为转录共激活因子,与 TCF/LEF 家族转录因子共同发挥作用。
在没有 Wnt 信号时,β-catenin 被“降解复合体”靶向泛素化而促使其降解。该降解复合体包括:Axin、腺苷酸酰化酶(APC)、蛋白磷酸酶 2A(PP2A)、糖原合酶激酶 3(GSK3)以及酪蛋白激酶 1α(CK1α)。
Wnt 与 Fz 及 LRP5/6 结合后,Axin 以及降解复合体转位至质膜。随后,降解复合体中的其他蛋白通过磷酸化作用,使 Axin 与 LRP5/6 的细胞质尾部结合。Axin 随后发生去磷酸化,其稳定性和水平下降。此后,Dsh 通过磷酸化而被激活,其 DIX 和 PDZ 结构域抑制降解复合体中 GSK3 的活性。
这一过程使 β-连环蛋白得以积累并定位至细胞核,随后与 TCF/LEF,即 T 细胞因子/淋巴增强因子转录因子共同作用,经由基因表达调控诱导细胞反应。β-连环蛋白还会招募其他转录共激活因子,例如 BCL9、Pygopus以及 Parafibromin/Hyrax。
非经典通路
非经典平面细胞极性(PCP)通路并不使用 LRP5/6 作为共受体,而被认为可能使用 NRH1、Ryk、PTK7 或 ROR2。PCP 通路通过 Wnt 与 Fz 及其共受体结合而被激活。随后,受体招募 Dsh;Dsh 利用其 PDZ 和 DIX 结构域,与 Dishevelled 相关形态发生激活因子 1(DAAM1)形成复合体。
DAAM1 随后通过 GEF 激活小 G 蛋白 Rho。Rho 激活 Rho 相关激酶(ROCK),而 ROCK 是细胞骨架的主要调控因子之一。Dsh 还会与 Rac1 形成复合体,并介导 profilin 与肌动蛋白结合。Rac1 激活 JNK,并且也可导致肌动蛋白聚合。Profilin 与肌动蛋白结合后,可引起细胞骨架重构和原肠胚形成。
非经典 Wnt/钙通路的作用是帮助调控内质网中的钙释放,从而控制细胞内钙水平。与其他 Wnt 通路类似,当配体结合后,被激活的 Fz 受体会直接与 Dsh 相互作用,并激活特定的 Dsh 蛋白结构域。参与 Wnt/钙信号传导的结构域是 PDZ 和 DEP 结构域。
与其他 Wnt 通路不同的是,Fz 受体会直接与三聚体 G 蛋白发生作用。Dsh 与 G 蛋白的这种共同刺激,可导致 PLC 或 cGMP 特异性 PDE 的激活。
如果 PLC 被激活(见PLC信号通路),最终导致钙和 DAG 浓度升高。可通过 PKC 激活 Cdc42。Cdc42 是腹侧模式形成的重要调控因子。还会激活钙调神经磷酸酶和 CaMKII。前者诱导转录因子 NFAT 的激活,调控细胞黏附、迁移和组织分离。后者可激活 TAK1 和 NLK 激酶,干扰经典 Wnt 通路中 TCF/β-catenin信号传导。
然而,如果 PDE 被激活,则会抑制内质网中的钙释放。PDE 通过抑制 PKG 来介导这一过程,而 PKG 受到抑制后,进一步导致钙释放受到抑制。
调控
1. 分泌前:Wnt 蛋白会发生棕榈酰化。Porcupine 蛋白介导这一过程,通过决定 Wnt 配体何时完全成熟,来帮助调控 Wnt 配体何时被分泌。
2. 分泌后:某些蛋白结合 Wnt 使其无法到达其受体。例如,Dally 和 GPC3 等稳定因子可与 Wnt 结合并抑制其扩散。
3. Fz 受体层面:Wnt 以外的蛋白与受体结合也可拮抗信号传导。特异性拮抗因子包括 Dickkopf(Dkk)、Wnt 抑制因子 1(WIF-1)、分泌型 Frizzled 相关蛋白(SFRP)等构成 Wnt 信号传导的抑制因子。
4. 信号通路相互作用:Wnt/钙通路可以抑制 TCF/β-连环蛋白,从而阻止经典 Wnt 通路信号传导。前列腺素 E2(PGE2)是经典 Wnt 信号通路的一个必要激活因子。通过 cAMP/PKA 介导的磷酸化稳定 β-连环蛋白。
诱导的细胞反应
胚胎发育
1. 轴向模式形成:在哺乳动物中,Wnt 与 BMP、FGF、Nodal、视黄酸等形态发生因子共同形成浓度梯度,以区分前部和后部区域。在鱼类和蛙类中,经典 Wnt 信号通过 β-连环蛋白诱导组织中心形成,并参与后部结构和背侧区域的建立。
2. 细胞命运决定:Wnt 信号可诱导多能干细胞分化为中胚层和内胚层祖细胞,并进一步形成内皮、心肌、血管平滑肌等细胞谱系。但在心脏形成中,Wnt 信号具有拮抗作用,因此抑制 Wnt 是诱导心脏组织形成和体外生成心肌细胞的重要手段。
3. 细胞增殖:经典 Wnt 信号通过提高细胞质和细胞核中的 β-连环蛋白水平,激活 cyclin D1、c-myc 等基因,从而推动细胞周期由 G1 期进入 S 期,促进 DNA 复制和细胞分裂。
4. 细胞迁移:原肠胚形成期间,经典 Wnt 通路和 Wnt/PCP 通路共同参与会聚延伸;而 Wnt/钙通路在激活时可抑制会聚延伸。
胰岛素敏感性
Wnt 信号也参与调节胰岛素敏感性。胰岛素通过促进细胞膜上葡萄糖转运蛋白的表达,增强细胞对血糖的摄取。该过程部分依赖 Wnt/β-连环蛋白信号。特别是 Wnt10b,可提高骨骼肌细胞的胰岛素敏感性。
Hedgehog 信号通路
Hedgehog 信号通路负责向胚胎细胞传递其正常细胞分化所需的信息,存在于所有两侧对称动物中。胚胎的不同部位具有不同浓度的 Hedgehog 信号蛋白。该通路在成体中也发挥作用。
该通路得名于其多肽配体,即一种在果蝇属果蝇中发现、名为 Hedgehog(Hh)的细胞间信号分子;缺失 Hh 基因的果蝇幼虫据称形似刺猬。Hh 是果蝇体节极性基因产物之一,参与建立果蝇身体蓝图的基础。该分子在胚胎发生后期以及变态发育过程中仍然十分重要。
哺乳动物具有三种 Hedgehog 同源物,即 Desert hedgehog(DHH)、Indian hedgehog(IHH)和 Sonic hedgehog(SHH),其中 Sonic hedgehog 研究最为充分。在缺失该通路组成成分的基因敲除小鼠中,脑、骨骼、肌肉系统、胃肠道和肺均不能正常发育。近期研究指出,Hedgehog 信号在调控成体干细胞方面发挥作用,而这些干细胞参与成体组织的维持与再生。
果蝇
机制
昆虫细胞表达一种全长锌指转录因子 Cubitus interruptus(Ci)。Ci 可与类驱动蛋白 Costal-2(Cos2)形成复合体,并与细胞微管结合,定位于细胞质中(图 1)。包括 PKA、GSK3β 和 CK1等激酶将 Ci 磷酸化,使其结合 SCF 复合体(果蝇蛋白 Slimb)。155 kDa 的全长 Ci 蛋白被靶向至依赖蛋白酶体的裂解过程,从而生成一个 75 kDa 的片段,即 CiR。CiR 在细胞内积累,并扩散进入细胞核,在那里作为 Hedgehog(Hh)靶基因的共抑制因子发挥作用。
在没有 Hh 的情况下(图 1),一种名为 Patched(PTCH)的细胞表面跨膜蛋白会阻止一种七次跨膜受体 Smoothened(SMO)的高水平表达和活性。当细胞外存在 Hh 时(图 2),Hh 会与 Patched 结合并抑制 Patched,从而使 Smoothened 得以积累,并抑制 Ci 蛋白的蛋白水解性裂解。
在具有 Hh 作用后的 Patched 的细胞中,完整的 Ci 蛋白会在细胞质中积累,而 CiR 水平下降,从而允许某些基因发生转录,例如 decapentaplegic,即 dpp,BMP 生长因子家族的成员。对于另一些受 Hh 调控的基因而言,其表达不仅需要 CiR 的消失,还需要未被裂解的 Ci 发挥积极作用,作为转录激活因子参与调控。

作用
Hedgehog 在果蝇发育中主要参与幼虫体节形成和成体附肢发育。在胚胎体节形成过程中,表达转录因子 engrailed 的细胞同时表达 Hedgehog(图中绿色所示)。当 Hedgehog 以这种局部方式发挥作用时,它是一种旁分泌因子。只有位于 engrailed 表达细胞一侧的细胞,才具备在 Hh 与受体蛋白 Patched 相互作用后对 Hedgehog 作出反应的能力(图中蓝色所示)。
邻近细胞在接收到 Hedgehog 信号后,会通过受体 Patched 被激活,并进一步诱导 Wingless 蛋白的表达(图中红色所示)。Wingless 属于 Wnt 家族信号蛋白,能够通过其受体 Frizzled 作用于相邻细胞,稳定 engrailed 的表达条带。Hedgehog 与 Wingless 之间形成相互调控,共同维持副体节边界(图上部),并建立体节前后轴上的位置编码,从而决定不同部位的解剖学特征。
在变态发育过程中,Hedgehog 与 Wingless 协同调控翅的形成。Hedgehog 还参与眼、脑、性腺、肠道和气管等器官的发育。其表达下降可能与某些动物眼部发育减弱有关。
