第五章 分生组织和分化:修订间差异
自动添加 Sofia 模板和分类 |
无编辑摘要 |
||
| 第1行: | 第1行: | ||
{{:Esau's Plant Anatomy}} | == ❙ 分生组织 (Meristems) == | ||
从合子分裂开始,维管植物产生新细胞并发育出新器官,通常直到其死亡。在早期胚胎发育过程中,细胞繁殖发生在整个生物体中,但随着胚胎发育成为独立的植物体,新细胞的增加逐渐局限于某些区域。这些现在局部化的生长组织(growing tissues)仍然保持胚胎特征,并在植物的整个生命周期中持续存在,因此其植物体是成体(adult)和幼体(juvenile)组织的复合体。这些主要参与新细胞形成的胚胎组织区域就是'''分生组织(meristems)'''(图5.1; McManus和Veit, 2002)。 | |||
细胞繁殖局限于植物的某些部位是进化特化(evolutionary specialization)的结果。在最原始的植物中,所有细胞基本上都是相似的,并且都参与细胞增殖、光合作用、分泌、储存和运输等重要活动。随着细胞和组织的逐步特化,细胞繁殖的功能主要局限于分生组织及其直接衍生物。 | |||
术语"分生组织"(源自希腊语''merismos'',意为分裂)强调了细胞分裂活动作为分生组织(meristematic tissue)的特征。除了分生组织之外,其他活组织也可能被诱导产生新细胞,但分生组织无限期地保持这种活动,因为它们不仅向植物体添加细胞,而且还自我延续(self-perpetuate);也就是说,分生组织中细胞分裂的一些产物不会发育成成体细胞,而是保持分生状态。那些维持分生组织作为新细胞持续来源的细胞被称为'''起始细胞(initiating cells)'''、'''分生组织起始细胞(meristematic initials)''',或简称为'''initials'''。它们的产物在经过不定次数的细胞分裂后产生'''体细胞(body cells)''',这些产物就是起始细胞的'''衍生物(derivatives)'''。也可以说,一个分裂细胞是衍生物的前体(precursor)。分生组织中的某个起始细胞是两个衍生物的前体,其中一个衍生物是新的起始细胞,另一个是体细胞的前体。 | |||
起始细胞和衍生物的概念应包括一个限定条件,'''即起始细胞与其衍生物没有本质上的区别。'''起始细胞和衍生物的概念将从不同角度考虑,与维管形成层(vascular cambium)(第12章)以及茎和根顶端分生组织(apical meristems)的描述相关(第6章)。这里只需指出,根据一种普遍观点,分生组织中的某些细胞之所以充当起始细胞,主要是因为它们占据了进行这种活动的适当位置。 | |||
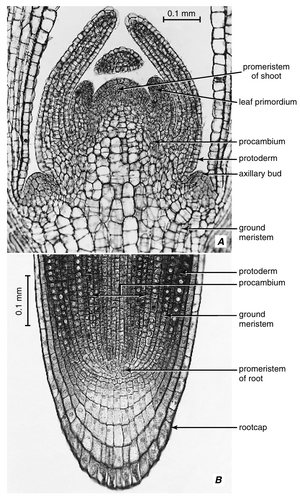
[[文件:E-5.1.png|缩略图|亚麻(Linum usitatissimum)幼苗茎尖(A)和根尖(B)的纵切面。两者都展示了顶端分生组织(apical meristems)和衍生的初生分生组织(primary meristematic tissues),包括原表皮(protoderm)、基本分生组织(ground meristem)和原形成层(procambium),其中最少确定的部分称为原分生组织(promeristem)。A中可见叶原基(primordia of leaves)和腋芽(axillary buds)。B中根冠覆盖了顶端分生组织。注意根顶端分生组织后面的细胞列(cell files)或细胞谱系(cell lineages)。(A,来自Sass, 1958. © Blackwell Publishing; B,来自Esau, 1977。)]] | |||
保留分生组织和产生新器官的能力将高等植物与高等动物区分开来。在后者中,胚胎发育过程中产生固定数量的器官,尽管完全发育的动物体内的成体组织和器官在整个生命周期中由存在于组织或器官内的细胞群维持。这些细胞被称为干细胞(stem cell)(Weissman, 2000; Fuchs, E., and Segre, 2000; Weissman et al., 2001; Lanza et al., 2004a, b),已被比作植物分生组织的原始细胞,并且术语"干细胞"已被许多植物生物学家采用。本书未采用"干细胞"这一术语。 | |||
尽管动物干细胞可能与植物分生组织的原始细胞类似,但它们并不等同于原始细胞。原始细胞是'''全能的(totipotent)'''(来自拉丁语totus,意为"全部");也就是说,它们有能力产生所有类型的细胞,甚至发育成完整的植物。在大多数动物中,只有受精卵或受精卵(fertilized egg)是真正全能的。胚胎干细胞(embryonic stem cell)几乎全能,但在个体发育(ontogeny)早期(囊胚期(blastocyst stage)后不久),它们会产生成体干细胞(adult stem cell),这些干细胞是多能的(pluripotent),并且能够产生的细胞类型数量有限——通常是它们所在的成体组织和器官中的那些细胞类型(Lanza et al., 2004a, b)。据报道,一些成体干细胞能够从其原始生态位迁移(原始细胞不具备这一特性),并呈现出新环境的典型形态和功能(Blau et al., 2001)。 | |||
成熟植物部分中的许多活细胞在发育上仍然是全能的。因此,植物的发育和组织可以被描述为具有可塑性(plasticity)(Pigliucci, 1998),这一特性被解释为对固着生活形式的进化反应。由于植物是静止的,它无法逃离其生长的环境,必须通过不经历不可逆的变化来适应不利的环境条件和捕食(Trewavas, 1980)。 | |||
=== 分生组织的分类 === | |||
分生组织的常见分类基于它们在植物体内的位置。有'''顶端分生组织(apical meristem)''',即位于主茎和侧枝以及根尖的分生组织(图5.1),和'''侧生分生组织(lateral meristem)''',即与轴(通常是茎和根)的侧面平行排列的分生组织。维管形成层(vascular cambium)和木栓形成层(cork cambium)是侧生分生组织。 | |||
基于分生组织位置的第三个术语是'''居间分生组织(intercalary meristem)'''。该术语指的是源自顶端分生组织并继续在距该分生组织一定距离处保持分生组织活性的分生组织。<u>居间(intercalary)一词意味着分生组织被插入(intercalated)在不再具有分生组织活性的组织之间</u>。最著名的居间分生组织例子是单子叶植物,特别是禾本科植物节间(internode)和叶鞘(leaf sheath)中的分生组织(图5.2)。这些类型的生长区域包含分化的传导组织元素,并最终转化为成熟组织,尽管它们的薄壁组织细胞长期保持恢复生长的能力(第7章)。作为分生组织,<u>居间分生组织与顶端分生组织和侧生分生组织不属于同一等级,'''因为它们不包含可以称为原始细胞的细胞'''</u>。 | |||
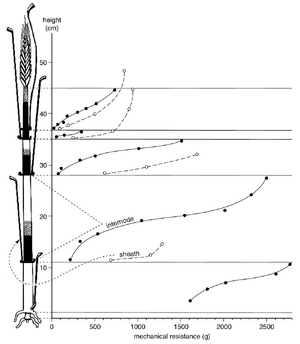
[[文件:E-5.2.png|缩略图|图5.2 黑麦植物茎秆中生长区域的分布。该植物有五个节间和一个穗。叶鞘从每个节向上延伸,并在叶片(仅部分显示)从叶鞘分叉处终止。节间中最年轻的组织(居间分生组织)用黑色表示,稍老的组织用斜线表示,最成熟的组织则留白。右侧的曲线表示在不同茎段水平上节间组织(实线)和叶鞘(虚线)的机械阻力。阻力等同于以克为单位表示的压力,即横向切割节间或叶鞘所需的压力。(根据Prat, 1935. © Masson, Paris.)]] | |||
在描述茎尖和根尖的初级分化时,初始细胞及其最近的衍生物经常与部分分化但仍具分生能力的下方组织区分开来,称为原分生组织(promeristem或protomeristem;Jackson, 1953)。下方的分生组织根据它们衍生的组织系统进行分类,即'''原表皮(protoderm)''',分化为表皮;'''原形成层(procambium,也称为provascular tissue*)''',产生初生维管组织;以及'''基本分生组织(ground meristem)''',是基本组织系统的前体。如果广泛使用分生组织这一术语,原表皮层、原形成层和基本分生组织被称为初生分生组织(Haberlandt, 1914)。在更狭义的分生组织定义(初始细胞及其直接衍生物的组合)中,这三种组织构成了部分确定的初生分生组织。 | |||
<nowiki>*</nowiki>一些研究人员区分provascular cells和 procam bial cells,provascular cells被认为是uncommitted but vascular-competent cells,而procambial cells是开始已经向木质部和韧皮部分化的细胞。 | |||
术语原表皮层、原形成层和基本分生组织非常适合描述植物器官中组织分化的模式,并且它们与成熟组织同样简单且方便的分类相对应,即表皮、维管和基本组织系统,这些在第一章中已经讨论过。只要理解这些组织的未来发育至少部分确定,原表皮层、原形成层和基本分生组织被称为分生组织或分生组织似乎并不重要。 | |||
分生组织也可以根据产生其初始细胞的细胞性质进行分类。如果初始细胞是胚胎细胞的直接后代,这些胚胎细胞从未停止与分生活动相关,那么由此产生的分生组织称为初生分生组织。然而,如果初始细胞来自已经分化后又恢复分生活动的细胞,那么由此产生的分生组织称为次生分生组织。 | |||
木栓形成层(phellogen)是次生分生组织(secondary meristem)的一个很好的例子,因为它起源于表皮或皮层和树皮深层中的各种薄壁组织(parenchymatous tissues)。维管形成层(vascular cambium)的起源更为多样,与初生维管系统(primary vascular system)的组织有关。该系统从原形成层(procambium)分化而来,而原形成层最终来源于顶端分生组织(apical meristem)。通常,原形成层和由其产生的初生维管组织以束(fascicles)的形式存在,或多或少已经被束间薄壁组织(interfascicular parenchyma)分隔开(图5.3A)。在初生生长结束时,初生木质部(primary xylem)和初生韧皮部(primary phloem)之间的剩余原形成层成为形成层的束内部分(fascicular part)。这种形成层由束间薄壁组织中产生的束间形成层(interfascicular cambium)补充(图5.3B)。因此,形成了一个连续的圆柱形形成层(横切面呈环状),部分起源于束内,部分起源于束间。根据初生和次生分生组织的定义,束内形成层是初生分生组织——通过原形成层从顶端分生组织衍生而来——而束间形成层是次生分生组织——从薄壁组织衍生而来,其次恢复了分生组织的活性。 | |||
在许多木本植物中,起源于这两个部位的形成层部分在随后的次生生长中变得难以区分。此外,鉴于从组织培养工作中获得的证据表明,活的植物细胞长期保持其生长潜力(Street, 1977),束间薄壁组织中形成层分裂的出现并不表明所涉及细胞的特征发生了重大变化。因此,将维管形成层部分归为初生分生组织,部分归为次生分生组织纯粹是理论上的。然而,这一结论并不影响将成熟组织分为初生和次生的分类价值,如第1章所述。 | |||
分生组织细胞的特征 | |||
分生组织细胞基本上与年轻的薄壁细胞相似。在细胞分裂期间,茎尖的细胞壁相对较薄,储存物质较少,其质体处于前质体(proplastid)阶段。内质网(endoplasmic reticulum)数量较少,线粒体(mitochondria)的嵴(cristae)较少。高尔基体(Golgi bodies)和微管(microtubules)存在,这是具有生长细胞壁的细胞的特征。液泡(vacuoles)小而分散。 | |||
顶端分生组织的深层可能具有更高的液泡化程度并含有淀粉(Steeves et al., 1969)。在一些分类群中,特别是蕨类植物、针叶树和银杏,在顶端圆顶(apical dome)的最高位置出现明显液泡化的细胞(第6章)。在种子萌发之前,胚胎的分生组织含有储存物质。 | |||
在细胞分裂期间,维管形成层细胞高度液泡化,一个或两个大液泡将致密的细胞质限制在薄壁层(parietal layer)中(第12章),其中含有粗糙内质网(rough endoplasmic reticulum)和其他细胞成分。在休眠期间,液泡系统呈现为许多相互连接的液泡。冬季液泡有时含有多酚(polyphenols)和蛋白质体(protein bodies)。此时,内质网是光滑的,核糖体(ribosomes)游离在细胞质中。 | |||
分生组织细胞通常被描述为具有较大的细胞核。但细胞大小与核大小的比率——细胞核比率(cytonuclear ratio)——变化很大(Trombetta, 1942)。一般来说,较大的分生组织细胞的细胞核相对于细胞大小来说较小。 | |||
在有丝分裂活性变化期间,细胞核显示出特征性的结构变化(Cottignies, 1977)。例如,在休眠的形成层中,当细胞核被阻滞在有丝分裂周期的$\mathbf{G}_{1}$期时,RNA合成缺失,核仁小、致密,且主要由纤维状结构组成。当细胞活跃且RNA合成进行时,核仁较大,具有明显的液泡和广泛的颗粒区,与纤维区交织在一起。 | |||
前面的综述表明,分生组织细胞在大小、形状和细胞质特征上存在差异。为了认识到这种变异性,术语eumeristem(真分生组织)被建议用于指定由小的、近似等径的、壁薄且富含细胞质的细胞组成的分生组织(Kaplan, R., 1937)。出于描述目的,这个术语通常使用起来很方便,但它不应暗示某些细胞比其他细胞更典型地具有分生组织特性。 | |||
分生组织中的生长模式 | |||
分生组织和分生组织组织显示出由于细胞分裂和扩大模式的差异而产生的细胞排列的多样性。仅有一个起始细胞占据顶端的顶端分生组织(木贼属和许多蕨类植物)具有最近形成的、仍然是分生组织的细胞的有序分布(第6章)。在种子植物中,细胞分裂的模式似乎不那么精确。然而,它并不是随机的,因为顶端分生组织作为一个有组织的整体生长,单个细胞的分裂和扩大与生长的内部分布和顶端的外部形式有关。这些相关影响导致分生组织中独特区域的分化。在分生组织的某些部分,细胞可能分裂缓慢并达到相当大的尺寸;在其他部分,它们可能频繁分裂并保持较小。一些细胞复合体在各个平面上分裂(体积生长),而其他细胞仅在与分生组织表面成直角的壁上分裂(垂周分裂,表面生长)。 | |||
侧生分生组织特别以与器官最近表面平行的分裂为特征(图5.4A;平周分裂),这导致与轴半径平行的细胞行的建立(径向序列或排列)和器官厚度的增加。在圆柱体(如茎和根)中,术语切向分裂(或切向纵向)通常用于代替平周分裂。如果垂周分裂与圆柱体的半径平行发生,则称为径向垂周(或径向纵向)分裂(图5.4B)。如果新壁与... | |||
图5.4 | |||
展示圆柱形植物结构分裂面的示意图。A,平周分裂(与表面平行)。B,径向垂周分裂(与半径平行)。C,横向分裂(与长轴成直角的垂周分裂)。 | |||
在圆柱体的纵轴上,垂周分裂是横向的(图5.4C)。 | |||
来自同一顶端分生组织(apical meristem)的器官可能呈现出不同的形态,因为顶端分生组织的仍具分生能力的衍生物(初生分生组织,primary meristems)通常表现出不同的生长模式。其中一些模式非常典型,以至于表现出这些模式的分生组织获得了特殊的名称。这些名称包括块状分生组织(mass meristem或block meristem)、肋状分生组织(rib meristem或file meristem)和板状分生组织(plate meristem)(Schiepp, 1926)。块状分生组织通过所有平面的分裂生长,产生等径的、球形的或没有明确形状的体。例如,在孢子、精子(在无种子维管植物中)和胚乳的形成过程中会发生这种生长。在许多被子植物胚胎发育的某个阶段,不同平面的分裂与球形形状相关。肋状分生组织通过垂直于细胞行纵轴的分裂产生一系列平行的纵向细胞列(“肋”)。这种生长模式发生在伸长的圆柱形植物部分中,如根的皮层以及茎的髓和皮层(图5.1)。板状分生组织主要表现出垂周分裂,因此最初在幼嫩器官中建立的层数不会进一步增加,从而产生板状结构。被子植物叶片的扁平叶片是板状分生组织生长的结果(图5.5)。板状分生组织和肋状分生组织是主要发生在基本分生组织(ground meristem)中的生长形式。它们与植物体的两种基本形式相关,即叶状器官的薄片状扩展叶片(lamina或blade)和根、茎、叶柄等伸长的圆柱形植物部分。 | |||
分生组织活动与植物生长 | |||
分生组织及其分生衍生物与广义上的生长有关,即体积和表面积的不可逆增加。在多细胞植物中,生长基于两个过程:细胞分裂(cell division)和细胞扩大(cell enlargement)。分生组织初始细胞的最近衍生物通过细胞分裂产生其他衍生物,并且连续的衍生物世代会增大体积。细胞扩大逐渐取代细胞分裂,最终完全取代它。当离分生组织初始细胞最远的衍生物停止分裂和扩大时,它们获得了所在组织的特征;也就是说,细胞分化并最终成熟。 | |||
尽管细胞分裂本身并不增加生长实体的体积(Green, 1969, 1976),但细胞的增加是多细胞生物生长的基本要求。细胞分裂和细胞扩大是生长过程的不同阶段,其中细胞扩大决定了植物的最终大小。 | |||
图5.5 | |||
图示两种大小的*Lupinus*小叶边缘的分生组织活动:A、B,$600\upmu\mathrm{m}$长;C、D,$8500\upmu\mathrm{m}$长。短线表示分裂细胞的赤道面或细胞板。分裂图通过连续切片记录并组装,A和C中为垂周分裂(anticlinal division),B和D中为平周分裂(periclinal division)。边缘的平周分裂建立了叶片的层数。垂周分裂扩展了各层(板状分生组织活动)。(来自Esau, 1977;重绘自Fuchs, 1968。) | |||
及其部分。作为细胞个体发育(development of an individual entity)的一个完整步骤,细胞的扩大(expansion)是分裂和成熟阶段之间的过渡(Hanson and Trewavas, 1982)。 | |||
细胞分裂很少不伴随细胞扩大,至少在一定程度上,分裂细胞群中维持了原始细胞的大小。一些被子植物胚胎在这方面是个例外。在合子发育成胚胎的前两到三个细胞分裂周期中,几乎检测不到细胞扩大(Dyer, 1976)。在无实体大小增加的情况下发生的细胞分裂也出现在小孢子(花粉粒)内雄配子体的形成过程中。同样,当多核胚乳转化为细胞组织时,细胞分裂也不伴随细胞扩大。然而,通常生长可以大致分为两个阶段:通过细胞分裂和有限的细胞扩大进行的生长,以及没有细胞分裂但伴随大量细胞扩大的生长。 | |||
图5.6 | |||
木本被子植物示意图,展示了茎和根的分枝,通过次生生长(secondary growth)增加茎和根的厚度,以及在增厚的轴上形成周皮(periderm)和树皮(bark)。主茎和侧枝(腋生)的顶端带有不同大小的叶原基(leaf primordia)。根毛出现在主根(直根)和侧根顶端的一定距离处。(来自Esau, 1977;改编自Rauh, 1950。) | |||
由于顶端分生组织(apical meristem)存在于所有茎和根的顶端,无论是主茎还是侧枝,因此在一株植物中其数量相对较多。经历茎和根次生增厚的维管植物(图5.6)还拥有广泛的分生组织,即维管形成层(vascular cambium)和木栓形成层(cork cambium)。植物在顶端分生组织中启动的初生生长(primary growth)扩展了植物体,决定了其高度,并通过增加其表面积,扩大了与空气和土壤的接触面积。最终,初生生长还产生了生殖器官。由形成层活动引起的次生生长增加了传导组织的体积,并形成了支持和保护组织。 | |||
通常,植物上存在的所有顶端分生组织不会同时活跃。在顶芽活跃生长时抑制侧芽生长(顶端优势(apical dominance);Cline, 1997, 2000;Napoli et al., 1999;Shimizu-Sato and Mori, 2001)是一种常见现象。然后,形成层的活动强度会有所不同,顶端和侧生分生组织的分生组织活动可能会表现出季节性波动,在温带地区冬季细胞分裂会减慢或完全停止。 | |||
❙ 分化(DIFFERENTIATION) | |||
术语和概念 | |||
植物的发育包括紧密相关的生长( growth )、分化( differentiation )和形态发生( morphogenesis )现象。分化是指分生组织衍生物的后代在形态、结构和功能上的一系列变化,以及它们组织成组织和器官的过程。我们可以谈论单个细胞的分化、组织( histogenesis )的分化、器官( organogenesis )的分化以及整个植物的分化。分化也指受精卵细胞产生后代细胞的过程,这些细胞表现出越来越明显的异质性、特化和模式化组织。这个术语并不精确,尤其是当它被用来对比分化细胞和未分化细胞时。分生细胞和卵细胞在细胞学上是复杂的,它们本身就是分化的产物。将这些细胞描述为未分化只是一种惯例(Harris, 1974)。 | |||
分化的程度和伴随的特化(对特定功能的结构适应)差异很大(图5.7)。一些细胞与其分生前体相比变化相对较小,并保留了分裂的能力(各种薄壁细胞)。其他细胞则发生了更深刻的改变,失去了大部分或全部分生潜力(筛管分子、乳汁管、管状分子、各种石细胞)。因此,在多细胞体中分化的细胞不仅与其分生前体不同,也与同一植物其他组织中的细胞不同。 | |||
从某种意义上说,各种分化的细胞可以被称为成熟细胞,因为它们已经达到了某种特化和生理稳定性,这通常是成年植物某些组织组成部分的特征。这种成熟的定义必须包括一个限定条件,即具有完整原生质体的成熟细胞在适当刺激下可能会重新恢复分生活动。这种刺激可能是由意外伤害、寄生虫入侵或病原体感染引起的(Beers and McDowell, 2001)。正常的内应力导致组织的选择性分解可能会引发类似于“修复反应”的生长反应。这种反应在轴次生增粗过程中的树皮中以及叶片或其他器官通常从植物上脱落的离区中很常见。通过将细胞从植物中分离出来并在体外培养以刺激其恢复生长,已成为研究成熟细胞分生潜力的特别有用的实验方法(Street, 1977)。 | |||
在研究非分生细胞恢复分生活动的过程中,术语去分化( dedifferentiation )——失去先前获得的特征——和再分化( redifferentiation )——获得新特征——经常被使用。整个过程被称为转分化( transdifferentiation )。与分化一样,去分化也不是一个精确的术语。去分化的细胞不会恢复到受精卵的状态,甚至不会恢复到胚胎细胞的状态,但它们可能会失去一些特化特征,并增加与DNA和蛋白质合成相关的亚细胞成分的数量。 | |||
关于分化(differentiation)的讨论可能会涉及到决定(determination)的概念(McDaniel, 1984a, b; Lyndon, 1998),这一现象可以被视为分化的一个方面。决定意味着对特定发育过程的渐进性承诺,导致恢复生长能力的减弱或丧失。一些细胞比其他细胞更早、更完全地决定,而一些细胞在分化后仍保持其全能性(totipotency)。分化与生长相关,这两种现象都发生在从亚细胞结构到整个植物的所有形态学水平上。在没有分化的情况下生长见于异常结构,如肿瘤。愈伤组织(callus tissue)也可能被诱导在几乎没有分化的情况下生长。 | |||
术语"能力(competence)"经常出现在分化的讨论中。正如McDaniel (1984a, b)所定义的,能力指的是细胞响应特定信号(如光)发育的能力。它意味着有能力的细胞能够识别信号并将其转化为反应。 | |||
在发育过程中,植物呈现出特定的形态。因此,植物经历形态发生(morphogenesis)(来自希腊语中表示形状和起源的单词)。该术语通常用于指代外部形态和内部组织,就像分化一样,形态发生在从细胞成分到整个植物的所有组织水平上都有体现。然而,D. R. Kaplan和W. Hagemann (1991)强调,尽管 | |||
图5.7 | |||
图示了一些可能起源于原形成层(procambium)或维管形成层(vascular cambium)分生组织细胞(meristematic cell)的细胞类型。这里描绘的分生组织细胞(中心)具有单个大液泡,是维管形成层分生组织细胞的典型特征。原形成层细胞通常含有几个小液泡。所有这些细胞的分生组织细胞或前体都具有相同的基因组。不同的细胞类型之所以彼此不同,是因为它们表达其他细胞类型不表达的基因集。在描绘的四种细胞类型中,薄壁组织细胞(parenchyma cell)是最不特化的。成熟的导管分子(vessel element)(专门用于水分传导)和成熟的纤维(fiber)(专门用于支持)都缺乏原生质体(protoplast)。成熟的筛管分子(sieve-tube element)(专门用于糖类和其他同化物的运输)保留了活的原生质体,但没有细胞核和液泡。它依赖其姐妹细胞——伴胞(companion cell)来维持生命。(来自Raven等,2005年。) | |||
植物解剖学和形态学的某些方面是相关的,但细胞和组织分化遵循器官发生(organogenesis)或形态发生。注意到一些植物生物学家在解释植物发育机制时倾向于混淆解剖学特征和形态学特征,D. R. Kaplan (2001)进一步强调"虽然解剖学可能由形态学决定...,但解剖学并不决定形态学。" | |||
衰老(程序性细胞死亡)(Senescence, Programmed Cell Death) | |||
植物因衰老而自然终止生命可以被视为植物发育的一个正常阶段,是分化和成熟事件的后续(Leopold, 1978; Noodén和Leopold, | |||
1988; Greenberg, 1996)。术语衰老(senescence)特指导致生物体死亡的一系列变化(Noodén and Thompson, 1985; Greenberg, 1996; Pennell and Lamb, 1997)。衰老可能影响整个生物体或其某些器官、组织或细胞。一年生植物(monocarpy: 仅结果一次)在其生命周期中仅开花一次,在一个季节内衰老。在落叶树中,叶子通常在季节性生长结束时衰老。果实在几周内成熟和衰老,离体的叶子和花朵在几天内衰老。衰老的单个细胞是根冠细胞,它们不断从生长的根上脱落。由于衰老在植物生命中有序发生,并且是一个活跃的退化过程,因此被认为是由基因控制的或程序化的——一个程序性细胞死亡(programmed cell death)的过程(Buchanan-Wollaston, 1997; Noodén et al., 1997; Dangl et al., 2000; Kuriyama and Fukuda, 2002)。 | |||
衰老可以由化学物质(包括生长物质)和环境条件控制(Dangl et al., 2000)。例如,用生长素(auxin)和细胞分裂素(cytokinins)处理大豆叶片,可以防止通常由种子发育引起的衰老(Thimann, 1978)。处理过的叶片保持了光合作用和氮同化能力,而不是将储备物质释放到生殖结构中并变得衰老。相反,乙烯(ethylene)可以诱导衰老(Grbic and Bleecker, 1995),它刺激了一系列衰老相关基因(senescence-associated genes, SAGs)的表达(Lohman et al., 1994)。 | |||
尽管衰老(senescence)一词源自拉丁语senesco,意为变老,但它并不被认为是与老化(aging)同义的(Leopold, 1978; Noodén and Thompson, 1985; Noodén, 1988)。与衰老一样,老化是个体生物生命周期的一个组成部分,并且不容易与衰老区分开来。老化被定义为降低生物体活力但不致命的累积变化。然而,老化可能导致衰老。老化一词的模糊性因其在实验工作中的使用而增强,用于表示在刺激代谢活动增加的条件下培养贮藏组织切片的做法。这种"老化"应称为复壮(rejuvenation)(Beevers, 1976)。 | |||
叶片衰老细胞中常见的变化包括叶绿素含量下降、红色(花青素)和黄色(类胡萝卜素)色素含量增加、蛋白质降解和核酸含量减少,以及细胞通透性增加(Leopold, 1978; Huang et al., 1997; Fink, 1999; Jing et al., 2003)。通透性的增加与膜脂质(membrane lipids)的紊乱有关(Simon, 1977; Thompson et al., 1997)。在自然衰老的小麦叶片中,叶绿体以质体小球(plastoglobuli)的形式积累脂质,基粒(grana)和基粒间片层(intergrana lamellae)膨胀并破裂成囊泡,基质(stroma)解体,最终叶绿体被膜破裂并释放细胞器内容物(Hurkman, 1979)。在衰老过程中,细胞的大部分生化过程都用于回收和重新分配代谢物和结构物质,特别是氮和磷的储备。过氧化物酶体(peroxisomes)转化为乙醛酸循环体(glyoxysomes),将脂质转化为糖类。在绿色细胞中,大部分蛋白质由位于叶绿体基质相中的Rubisco(核酮糖-1,5-二磷酸羧化酶/加氧酶)组成。迄今为止,已在多种植物物种中鉴定出100多个所谓的衰老相关基因(senescence-associated genes),这些基因的表达水平在叶片衰老期间上调(参见Jing et al., 2003引用的文献)。 | |||
植物中程序性细胞死亡(programmed cell death)的其他例子包括: - 导管分子(tracheary elements)的成熟(第10章;Fukuda, 1997); - 根部通气组织(aerenchyma tissue)的形成(第7章),以应对由洪水引起的缺氧(hypoxia)(Drew et al., 2000); - 胚胎发生过程中胚柄(suspensor)的破坏(Wredle et al., 2001); - 大孢子发生(megagametogenesis)期间四个大孢子中三个的死亡; - 谷物糊粉层细胞(aleurone cells)在产生大量$\upalpha$-淀粉酶后的死亡,这些酶是分解和动员淀粉以提供幼苗发育所需能量的关键(Fath et al., 2000; Richards et al., 2001); - 叶片形状的发育重塑(Gunawardena et al., 2004)。 | |||
程序性细胞死亡还在抵抗病原体(pathogens)中发挥重要作用(Mittler et al., 1997)。由病原体攻击引发的快速细胞死亡——称为超敏反应(hypersensitive response, HR)——与主动抗性密切相关(Greenberg, 1997; Pontier et al., 1998; Lam et al., 2001; Loake, 2001)。HR抵抗病原体的确切机制仍存在争议。有观点认为,HR通过直接杀死病原体和/或干扰其营养获取来限制其生长(Heath, 2000)。 | |||
植物中的程序性细胞死亡(programmed cell death)由激素信号触发,涉及胞质$\mathrm{Ca}^{2+}$浓度的变化(He et al., 1996; Huang et al., 1997),以及液泡中隔离的水解酶的激活。随着液泡的崩溃,酶被释放出来,使其能够攻击原生质体的细胞核和细胞质成分。乙烯(ethylene)在缺氧后诱导根部的程序性细胞死亡和通气组织(aerenchyma)的形成,并且如前所述,促进叶片衰老(He et al., 1996; Drew et al., 2000)。当添加到刚刚完成S期的烟草TBY-2细胞时,乙烯在细胞周期的${\bf G}_{2}/{\bf M}$检查点导致了一个显著的死亡高峰,这支持了程序性细胞死亡可能与细胞周期检查点紧密相关的假设(Herbert et al., 2001)。糊粉层细胞(aleurone cells)中的程序性细胞死亡由赤霉酸(gibberellic acid)启动(Fath et al., 2000),而油菜素内酯(brassinosteroids)已被证明可以诱导管状分子(tracheary elements)中的程序性细胞死亡(Yamamoto et al., 2001)。 | |||
术语程序性细胞死亡和细胞凋亡(apoptosis)经常互换使用。然而,细胞凋亡最初用于指代动物细胞中程序性细胞死亡的特定特征(第2章; Kerr et al., 1972; Kerr and Harmon, 1991)。这些特征包括核收缩、染色体凝聚、DNA断裂、细胞收缩、膜泡化以及形成被邻近细胞吞噬和降解的膜结合“凋亡小体(apoptotic bodies)”。迄今为止,植物细胞中记录的程序性细胞死亡均不具备细胞凋亡的所有特征(Lee and Chen, 2002; Watanabe et al., 2002; 以及其中引用的文献)。 | |||
分化过程中的细胞变化 | |||
在分化过程中,组织多样性源于单个细胞特征的变化以及细胞间关系的改变。或多或少分化细胞的共同特征,包括单个细胞组分的结构和功能,将在第2章和第3章中描述。细胞分化过程中细胞壁结构的变化将在第4章中讨论。初生和次生细胞壁厚度的差异增加、细胞壁质地和化学性质的变化以及特殊雕刻图案的发育引入了细胞之间的差异。 | |||
被子植物分化细胞中常见的细胞学现象是内多倍性 | |||
内多倍性(Endopolyploidy)是指在核膜内发生DNA复制周期而不形成纺锤体的情况。因此,新形成的DNA链保留在同一核内,使核成为多倍体。这种类型的DNA复制周期称为内周期(Endocycle)(Nagl, 1978, 1981)。在一些内周期中,会发生类似于有丝分裂的结构变化,复制的DNA链成为独立的染色体(内周期有丝分裂周期)。植物中最常见的内周期是内复制(Endoreduplication)或内复制(Endoreplication)周期,其中不发生类似有丝分裂的结构变化(D’Amato, 1998; Traas et al., 1998; Joubès and Chevalier, 2000; Edgar and Orr-Weaver, 2001)。在内复制过程中,会形成多线染色体(Polytene chromosomes)。这些染色体包含许多以电缆形式并排连接的DNA链。因此,多线性是由于DNA复制而不分离姐妹染色体,因此染色体数量不变的结果。 | |||
内周期有时被解释为没有功能意义的异常现象。根据另一种观点,涉及内周期的生长具有重要的优势,因为它提供了一种增加基因表达水平的机制(Nagl, 1981; Larkins et al., 2001)。此外,在内周期期间,RNA合成不会像在有丝分裂周期中那样中断。因此,细胞具有持续高水平的RNA和蛋白质合成,这些活动促进了快速生长和早期进入功能状态。相比之下,正在进行有丝分裂活动的生长组织在承担成熟生理活动方面表现出延迟。例如,当Phaseolus的胚体仍然表现出分生组织活动时,含有多线染色体的胚柄是一种代谢高度活跃的结构,为生长的胚胎提供营养。 | |||
越来越多的证据表明,倍性水平与细胞大小之间存在正相关关系(Kondorosi et al., 2000; Kudo and Kimura, 2002; Sugimoto-Shirasu et al., 2002)。因此,内复制可能是细胞生长的重要策略(Edgar and Orr-Weaver, 2001)。它也可能是特定细胞类型分化所必需的。例如,在拟南芥(Arabidopsis)中,毛状体(Trichome)的起始与内复制的开始密切相关(第9章; Hülskamp et al., 1994)。 | |||
正如Nagl(1978)所指出的,内周期可以被理解为一种进化策略。在整个物种中具有较低基本核DNA含量的门总是表现出内多倍性,而那些主要具有高DNA值的物种则缺乏内多倍性。正如Mizukami(2001)所提出的,“内复制可能已经作为一种发育手段进化,以在具有小基因组的物种中提供差异基因表达。” | |||
在分化组织中最先可见的变化之一是细胞大小的不均等增加。一些细胞继续分裂,但大小增加不大,而另一些细胞停止分裂并显著增大(图5.8)。细胞大小差异生长的例子包括:原形成层细胞的伸长与相邻髓和皮层薄壁细胞缺乏类似伸长;根中初生韧皮部(最早形成的)筛管分子的伸长,与相邻的周缘细胞继续横向分裂形成对比(图5.8A);导管分子的加宽与周围细胞保持狭窄形成对比(图5.8E)。两个相邻细胞之间的大小差异也可能源于不对称或不等分裂,这些分裂产生具有不同命运的细胞(Gallagher and Smith, 1997; Scheres and Benfey, 1999)。例如,在花粉形成过程中,不对称细胞分裂产生一个较大的管细胞或营养细胞和一个较小的生殖细胞(Twell et al., 1998)。在一些植物中,根毛从原表皮细胞不对称分裂形成的两个姐妹细胞中较小的细胞发育而来(图5.8B, C;第9章)。不等分裂也发生在气孔的形成过程中(第9章;Larkin et al., 1997; Gallagher and Smith, 2000)。 | |||
细胞大小的增加可能沿所有直径相对均匀,但细胞经常在一个方向上比其他方向增大更多。这样的细胞可能与其分生组织前体在形状上显著不同(长的初生韧皮部纤维、分支的石细胞)。然而,许多细胞通过增加细胞面数但保留多面体形状以更温和的方式发生改变(Hulbary, 1944)。 | |||
组织中主要的细胞排列可能由其分生组织的生长形式决定(肋状分生组织、板状分生组织)。连续细胞行中壁的相对位置也赋予组织独特的外观(Sinnott, 1960)。与细胞行成直角的壁可能在相邻行中交替出现,或者可能出现在同一平面上。 | |||
图5.8 | |||
组织分化过程中的细胞间调整。A,烟草根尖的一系列细胞。薄壁细胞继续分裂;韧皮部细胞停止分裂并开始伸长。B, C,根毛从原表皮细胞横向分裂形成的两个姐妹细胞中较小的细胞发育而来。C,根毛细胞在与根成直角的方向上延伸,但不在根的伸长方向上延伸。显然,在根毛相邻的细胞中,壁部分$^a$和$c$继续伸长,而部分$^b$在根毛原基形成后停止伸长。D, E,形成层和由此类形成层发育的木质部,均为切向切面。E,展示了形成层衍生物发育变化的结果:此类衍生物的横向分裂形成薄壁细胞,导管分子横向扩展,纤维通过顶端侵入性生长伸长。 | |||
分化组织中的细胞间调节涉及协调和侵入性生长 | |||
分化组织中细胞的扩大和形状改变伴随着细胞间空间关系的或多或少深刻的变化。一个熟悉的现象是沿着三个或更多细胞结合线出现的细胞间隙(intercellular spaces)(第4章)。在某些组织中,细胞间隙的形成不会改变细胞的总体排列;而在其他组织中,它深刻地改变了组织的外观(Hulbary, 1944)。细胞骨架,特别是微管(microtubules)和纤维素微纤维(cellulose microfibrils)的定向在细胞形状形成中的作用将在第4章中讨论。 | |||
关于组织分化过程中细胞壁的生长,可以设想两种细胞间调节方式:(1) 属于两个相邻细胞的相邻生长壁层不分离,而是共同扩展;(2) 相邻壁层分离,生长细胞侵入由此产生的空间。第一种生长方式最初被称为共质生长(symplastic growth)(Priestley, 1930),在器官的初生生长过程中扩展时很常见。无论复合体中的所有细胞是否都在分裂,或者某些细胞已经停止分裂并在长度和宽度上增加,相邻细胞的壁似乎在没有分离或弯曲的情况下同步生长。在这种协调生长中,两个细胞之间的共同壁的一部分可能在扩展,而另一部分则没有。 | |||
涉及细胞侵入其他细胞之间的细胞间调节被称为侵入性生长(intrusive growth)(Sinnott和Bloch, 1939)或插入生长(interpositional growth)(Schoch-Bodmer, 1945)。这种生长的证据基于光学显微镜观察(Bailey, 1944; Bannan, 1956; Bannan和Whalley, 1950; Schoch-Bodmer和Huber, 1951, 1952)。它在延长的形成层初始细胞、维管组织中的初生和次生纤维、管胞(tracheids)、乳汁管(laticifers)和一些石细胞(sclereids)中很常见。侵入性生长可能异常强烈,如在某些木本百合科植物中,次生管胞比其分生组织对应物长15到40倍(Cheadle, 1937)。延长的细胞在其顶端生长(顶端侵入性生长(apical intrusive growth)),通常在两端。特定扩展基因表达在分化中的Zinnia木质部细胞末端的定位表明,扩展蛋白(expansins)可能参与了这些细胞初生细胞壁通过侵入性生长的延长(Im等, 2000)。延长的细胞侵入的细胞间物质可能在前进的尖端前水解,相邻细胞的初生壁以与细胞间隙形成期间相同的方式彼此分离(第4章)。 | |||
如果存在胞间连丝(plasmodesmata),它们可能会被生长细胞的侵入而破裂。报道的初生纹孔对(pit-pairs)成员的分离(Neeff, 1914)表明这种破裂的发生。纹孔对后来出现在通过侵入性生长接触的细胞对之间(Bannan, 1950; Bannan和Whalley, 1950)。这种纹孔对的特征是存在次生胞间连丝(secondary plasmodesmata)(第4章)。侵入性生长还与细胞的横向扩展有关,这些细胞获得了相当大的宽度,例如木质部中的导管分子(vessel elements)(第10章)。 | |||
早期的植物学家推测,滑动生长(gliding growth)发生在细胞侵入其他细胞之间的差异伸长或侧向扩张过程中。在滑动生长中,生长细胞的一部分壁被认为会分离并在相邻细胞的壁上滑动(Krabbe, 1886; Neeff, 1914)。这一概念后来被侵入生长(intrusive growth)所取代。这种局部细胞延伸是否涉及新壁部分在与旧壁接触时的滑动(Bannan, 1951),或者新壁是否沿着分离细胞的自由表面并置(插入生长; Schoch-Bodmer, 1945),目前仍不确定。 | |||
❙ 分化中的因果因素 | |||
关于分化和形态发生的研究包括对正常发育的植物和发育受到实验操作的植物的观察。实验处理的例子包括使用生长调节化学物质、外科手术、暴露于辐射、限制在受控温度和光照下、干扰正常重力效应以及在选定的日长条件下生长。已经收集了大量关于机械扰动对植物影响的证据。轻微的摩擦或弯曲茎会导致所有测试物种的长度生长明显延迟和径向生长增加。对机械干扰的反应被称为接触形态发生(thigmomorphogenesis)(Jaffe, 1980; Giridhar and Jaffe, 1988),thigm在希腊语中意为触摸。在自然界中,风显然是导致接触形态发生的最主要环境因素。分子遗传学方法在研究分化和形态发生中的应用,包括识别干扰感兴趣过程的突变,极大地促进了我们对调节植物发育各个方面因素的理解(Žárský and Cvrckova, 1999)。 | |||
组织培养技术对确定生长和分化需求非常有用 | |||
对完整植物和实验处理植物的研究清楚地表明,高等植物的有组织模式发育依赖于内部控制机制,其作用在一定程度上受到环境因素的影响(Steward et al., 1981)。 | |||
植物中模式分化(patterned differentiation)的需求对细胞的分生潜能(meristematic potentialities)施加了限制。当这种限制因从植物的有组织体中切除而中断时,活细胞能够恢复生长。在体外组织培养(tissue culture in vitro)的研究中,利用完整植物中控制机制的释放来探索有利于分生活动(meristematic activity)的条件,或者相反,诱导分化和形态发生(morphogenesis)(Gautheret, 1977; Street, 1977; Williams and Maheswaran, 1986; Vasil, 1991)。由于细胞在组织培养中对刺激的生长反应能力并不一定可预测(Halperin, 1969),许多组织培养研究涉及测试来自不同分类群和植物不同部位的外植体(explant)的分生潜能。这项研究的另一个目的是研究培养基的各种成分,特别是生长调节物质(growth-regulating substances)对外植体的影响。最初,植物组织培养主要用于专门的植物学研究。后来,该技术被广泛用于经济重要植物的繁殖、获得无病植物,以及培养细胞和组织作为药用和其他植物成分的来源(Murashige, 1979; Withers and Anderson, 1986; Jain et al., 1995; Ma et al., 2003)。对分离的*Zinnia*叶肉细胞(mesophyll cells)的培养研究为植物细胞分化和程序性细胞死亡(programmed cell death)提供了宝贵信息(第10章)。 | |||
在早期的组织培养工作中,胡萝卜根的次生韧皮部组织(secondary phloem tissue)是流行的实验材料(图5.9; Steward et al., 1964)。在含有椰子胚乳(coconut endosperm)的液体培养基中以解离状态培养时,外植体首先发育成随机增殖的愈伤组织(callus tissue),然后产生一种更有序的生长类型:具有中央木质部和木质部外韧皮部的结节(nodule)(Esau, 1965, p. 97)。结节最终产生根,然后在根的对面产生芽。由此产生的小植株呈现出年轻胡萝卜植物的形态,当转移到土壤中时,形成典型的直根(tap root)并开花。分离的胡萝卜细胞可以通过其他方式而不是通过愈伤组织进行形态发生(Jones, 1974)。通常,小的、液泡稀少的细胞从原始外植体中脱离,并呈现出胚状体(embryoid)的形态,这些胚状体在发育成植物时类似于合子胚(zygotic embryo)。从植物体细胞(somatic cells)启动和发育胚状体的过程称为体细胞胚胎发生(somatic embryogenesis)(Griga, 1999)。 | |||
技术的改进使得通过酶法去除单细胞的细胞壁来分离原生质体(protoplast)成为可能。这样的原生质体使得质膜(plasma membrane) | |||
图5.9 | |||
从组织培养中的细胞发育成胡萝卜植物。培养的细胞来自胡萝卜直根的韧皮部。(经许可改编自F. C. Steward, M. O. Mapes, A. E. Kent, 和 R. D. Holsten. 1964. 培养植物细胞的生长和发育. Science 143, 20–27. © 1964 AAAS.) | |||
膜可用于广泛的实验。分离的原生质体可以被诱导融合并产生体细胞杂种,这种技术对于植物育种方法成功率有限的植物尤其有价值,例如马铃薯植物 (Shepard et al., 1980)。分离的原生质体最终会再生细胞壁,并可能经历分裂并产生完整的植物 (Power and Cocking, 1971; Lörz et al., 1979)。如今,基因工程——重组DNA技术的应用——允许将单个基因以精确且简单的方式插入植物细胞中,无论是否去除细胞壁 (Slater et al., 2003; Peña, 2004; Poupin and Arce-Johnson, 2005; Vasil, 2005)。此外,参与基因转移的物种不必能够相互杂交。 | |||
许多细胞培养研究基于花药和花粉粒的使用 (Raghavan, 1976, 1986; Bárány et al., 2005; Chanana et al., 2005; Maraschin et al., 2005)。在适当的培养条件下,包裹在花药中的花粉粒可以产生胚状体,当花药打开时,这些胚状体被释放出来。对于分离的花粉培养,花药或整个花蕾在液体培养基中研磨,悬浮液经过过滤以分离花粉,然后在悬浮液或琼脂上进行培养。 | |||
在成功的培养中,花粉粒从正常的配子体发育转向营养孢子体发育,直接或通过愈伤组织生长形成胚状体 (Geier and Kohlenbach, 1973)。这个过程被称为雄核发育 (androgenesis)。常见的途径是通过营养细胞 (Sunderland and Dunwell, 1977; Street, 1977 第9章)。 | |||
由于花粉粒只含有一个基因组,因此可以获得单倍体植物。这些单倍体植物在植物育种中有许多用途,并且在突变研究中尤为重要。诱导的突变会立即在单倍体表型中表现出来,而在二倍体高等植物中,通常的隐性突变只有在诱变植物的后代中才会显现。 | |||
遗传嵌合体分析可以揭示发育植物中的细胞分裂和细胞命运模式 | |||
遗传嵌合体 (genetic mosaic) 一词指的是由不同基因型的细胞组成的植物。在开花植物中,遗传嵌合体,也称为嵌合体 (chimeras),出现在茎尖分生组织 (shoot apical meristem) 中 (图5.10) (Tilney-Bassett, 1986; Poethig, 1987; Szymkowiak and Sussex, 1996; Marcotrigiano, 1997, 2001)。在一些茎尖分生组织中,发现了整个平行的细胞层,这些细胞层在基因上彼此不同。这种嵌合体被称为周缘嵌合体 (periclinal chimeras)。在其他情况下,只有部分层(或几层)在基因上不同(部分周缘嵌合体,mericlinal chimeras);还有一些情况下,基因不同的细胞的清晰边界延伸穿过所有层(扇形嵌合体,sectorial chimeras)。这些差异可以作为标记,通过连续的细胞谱系追踪到茎尖分生组织细胞层中的类似差异。一些嵌合体具有二倍体和多倍体核的细胞层组合(细胞嵌合体,cytochimeras)。多倍化 | |||
图5.10 | |||
嵌合体茎尖。A,周缘嵌合体;B,部分周缘嵌合体;C,扇形嵌合体。右侧显示横切面;左侧显示由线指示的平面上的纵切面。 | |||
通过用秋水仙素(colchicine)处理茎尖(图5.11),可以诱导细胞核的多倍化。结果,顶端分生组织(apical meristem)中的某一层会被多倍体(polyploid)细胞核占据,这种变化会通过该层的后代细胞传递到分化中的植物体(Dermen, 1953)。在具有缺陷、无色质体(plastid)的突变体中,也可以发现周缘嵌合体(periclinal chimera)。与核嵌合体(nuclear chimera)一样,这种异常特征——在这里是有缺陷的质体——可以通过顶端分生组织到成熟组织的细胞谱系来追踪(Stewart et al., 1974)。花青素(anthocyanin)色素沉着是另一个常见的标记。 | |||
另一种类型的遗传嵌合体(genetic mosaic)是遗传上不同的细胞克隆(clone)散布在植物体中(图5.12)。这种克隆通常简称为遗传嵌合体,可以通过电离辐射(ionizing radiation)实验产生。由此产生的染色体重排(chromosomal rearrangement)使得隐性细胞自主突变(recessive cell-autonomous mutation)得以表型表达。来自这些细胞的细胞谱系或克隆被永久标记,对这些克隆的分析可以用来生成植物体任何区域细胞的命运图谱(fate map)。正如Poethig(1987)所指出的,他通过克隆分析研究了叶片发育(Poethig, 1984a; Poethig and Sussex, 1985; Poethig et al., 1986),然而,这种技术并不能替代植物发育的组织学研究。为了准确解释克隆模式,"必须对所研究系统的发育组织学和形态学有清晰的理解"(Poethig, 1987)。 | |||
基因技术极大地提高了我们对植物发育的理解 | |||
最终决定植物特征的是基因。DNA测序技术的进步使得对整个基因组进行测序成为可能,并催生了基因组学(genomics)这一新科学。基因组学涵盖了对整个基因组的内容、组织和功能的研究(Grotewold, 2004)。第一个被完整测序的植物基因组是拟南芥(Arabidopsis thaliana)(Arabidopsis Genome Initiative, 2000)。最近,水稻(Oryza sativa)基因组的高精度测序也已完成(International Rice Genome Sequencing Project, 2005)。 | |||
基因组学的一个广泛目标是识别基因,确定哪些基因被表达(以及在什么条件下),并确定它们的功能或其蛋白质产物的功能。如何确定一个基因的功能?一个非常成功的方法是揭示对植物发育有可见或表型影响的突变。已经筛选了大量经诱变剂处理的拟南芥植株,寻找此类突变。通过插入一段DNA片段使基因失活的突变体集合,可以用于研究基因功能。 | |||
图5.11 | |||
来自二倍体植物(左上)和几个周缘细胞嵌合体(periclinal cytochimeras)的*Datura*茎尖。染色体组合由每张图下方的数值表示。每组三个数值中的第一个数值代表第一层表皮原(tunica layer);第二个数值代表第二层表皮原;第三个数值代表原体层(corpus)的初始层。这三层通常被命名为L1、L2和L3。八倍体细胞最大,其细胞核用黑色表示以强调;四倍体细胞稍小,其细胞核用点状表示;二倍体细胞最小,其细胞核用圆圈表示。表皮原层的染色体特征仅在这些层及其衍生物中得以延续(表皮原中的垂周分裂);原体初始层的染色体特征会立即传递到其下方的层(不同平面的分裂)。(引自Satina等人,1940年。) | |||
大片段DNA,如*Agrobacterium tumefaciens*的T-DNA,也被开发用于大量基因的研究(Bevan, 2002)。这些所谓的敲除突变体(knockout mutants),每个突变体都有一个不同的基因失活,然后通过筛选它们在特定环境中的表型变化或功能变化。任何被识别的变化都可以追溯到特定的突变序列。关于*Arabidopsis*,已经识别出负责胚胎发生(embryogenesis)主要事件的基因(Laux和Jürgens, 1994),负责茎尖分生组织(shoot apical meristem)形成和维持的基因(Bowman和Eshed, 2000; Doerner, 2000b; Haecker和Laux, 2001),以及控制花形成和花器官发育的基因(Theißen和Saedler, 1999)。 | |||
图5.12 | |||
在叶片开始形成之前,烟草(*Nicotiana tabacum*)叶片的表皮下层(subepidermal layer)中的克隆(clones)被照射($\mathbf{axis}=100\upmu\mathbf{m}$)。在这个阶段,克隆通常仅限于上表皮下层(黑色)或下表皮下层(灰色)。没有一个克隆从边缘延伸到中脉。(重绘自Poethig, 1984b。引自:*Pattern Formation*。Macmillan。© 1984。经McGraw-Hill Companies许可复制。) | |||
在基因的初级作用与其最终表达之间有一系列的过程。基因对分化的初始影响的解释是在分子水平上进行的。它涉及基因激活和抑制、转录(从双链DNA螺旋的一条链的一部分合成信使RNA)和翻译(由mRNA的核苷酸序列指导的多肽合成)。多细胞生物中许多细胞类型之间的差异是选择性基因表达的结果——即只有某些基因被表达并转录成mRNA。因此,介导细胞分化的蛋白质被选择性地合成。在给定的细胞中,一些基因持续表达,另一些基因仅在需要其产物时表达,还有一些基因根本不表达。控制基因表达的机制——即“开启”和“关闭”基因——统称为基因调控(gene regulation)。 | |||
极性是生物模式形成的关键组成部分,并与梯度现象相关 | |||
极性(polarity)指的是空间中的活动方向。它是生物模式形成(biological pattern formation)的重要组成部分(Sachs, 1991)。极性在植物生命早期就显现出来。它表现在卵细胞中,细胞核位于合点端(chalazal end),而大液泡位于珠孔端(micropylar end),也表现在合子发育成胚胎的双极(bipolar)发育过程中。随后,极性表现在植物组织成根和茎的过程中,在细胞水平的各种现象中也很明显(Grebe et al., 2001)。移植研究(Gulline, 1960)和组织培养研究(Wetmore and Sorokin, 1955)表明,不仅整个植物表现出极性,其各个部分也表现出极性,即使这些部分与植物分离。茎的极性是一个常见的现象。例如,在用茎插条繁殖的植物中,根会在茎的下端形成,叶和芽会在上端形成。此外,通过将茎插条倒置种植,无法改变极性。 | |||
极性的稳定性在分化蕨类孢子(fern spores)的离心实验中得到了清晰的证明(Bassel and Miller, 1982)。在*Onoclea sensibilis*中,孢子的正常第一次分裂之前,细胞核从椭圆形孢子的中心迁移到其一端。随后发生高度不对称的分裂。大细胞形成原丝体(protonema),小细胞发育成假根(rhizoid)。孢子的离心作用不会改变这种分裂模式,即使孢子的内容物发生位移和分层。只有当离心作用发生在有丝分裂(mitosis)或胞质分裂(cytokinesis)之前或期间时,不对称分裂才会被阻止。 | |||
完整植物中单个细胞的极性行为通过不等分裂(unequal division)表现出来,这种分裂会产生生理上、通常也是形态上不同的子细胞(Gallagher and Smith, 1997)。在一些根的表皮(epidermis)中,发生不等分裂后,两个分裂产物中较小的一个形成根毛(root hair)。在分裂之前,富含细胞器的细胞质大部分积累在细胞的近端(proximal end)(朝向根尖的一端)或远端(distal end)。细胞核向同一方向迁移,然后分裂。细胞板(cell-plate)的形成将未来的小根毛细胞与不产生根毛的较长表皮细胞分开(Sinnott, 1960)。两种细胞之间的生化差异也变得明显(Avers and Grimm, 1959)。通常的假设是,不等分裂依赖于细胞质的极化(polarization),因为没有证据表明染色体物质(chromosomal material)的不等分布(Stebbins and Jain, 1960)。 | |||
极性(polarity)与梯度现象(gradients)相关,因为植物轴两极之间的差异以梯度系列的形式出现。存在生理梯度(physiological gradients),例如表现在代谢过程速率、生长素(auxins)浓度和传导系统中糖浓度的梯度;也存在解剖分化(anatomical differentiation)和外部特征发育的梯度(Prat, 1948, 1951)。植物轴在根和茎之间的过渡区域显示出过渡性的解剖学和组织学特征。分生组织(meristems)衍生细胞的分化通常以梯度系列的形式发生,相邻但不同的组织可能表现出不同的梯度。外部形态上,沿轴的连续叶片形态的变化显示出梯度发育,从通常较小且简单的幼态形式逐渐过渡到较大且更复杂的成体形式(图5.13)。随后,在诱导生殖状态后,逐渐产生较小的叶片,最终以支持花序(inflorescence)分支或单个花的花序苞片(inflorescence bracts)完成这一系列变化。 | |||
植物细胞根据位置分化 | |||
尽管细胞分化(cellular differentiation)依赖于基因表达的控制,但植物细胞的命运——即它将成为何种类型的细胞——是由其在发育器官中的最终位置决定的。即使建立了不同的细胞谱系(cell lineages),例如根中的细胞谱系,决定细胞命运的是位置而非谱系。多细胞生物中细胞的功能由其在该生物体中的位置早期决定的概念可以追溯到19世纪下半叶(Vöchting, 1878, p. 241)。然而,直到20世纪70年代初,嵌合体(chimeras)中偶尔观察到的细胞位移才提供了证据,表明茎和叶中的细胞命运是由位置而非谱系决定的,即使在发育的晚期阶段也是如此(Stewart and Burk, 1970)。此后,通过对遗传嵌合体(genetic mosaics)的分析,积累了确凿的证据,表明细胞的位置而非其克隆起源决定了其命运(Irish, 1991; Szymkowiak and Sussex, 1996; Kidner et al., 2000)。如果一个未分化的细胞从其原始位置位移,它将分化成适合其新位置的细胞类型,而不会对植物的组织结构产生任何影响(Tilney-Bassett, 1986)。对拟南芥(Arabidopsis)根尖的激光消融实验(van den Berg et al., 1995)也表明,消融的细胞可以被其他谱系的细胞替代,这些“替代细胞”根据其新位置进行分化。 | |||
图5.13 | |||
马铃薯(Solanum tuberosum)主茎上的前10片叶片。叶片经历了从单叶到羽状复叶的过渡。$(\times0.1$ 。引自McCauley and Evert, 1988。) | |||
鉴于植物细胞的命运取决于它们在植物体内的位置,显然细胞之间必须能够相互通信,即交换位置信息。位置信息已被证明在玉米叶片光合作用细胞类型的分化(differentiation)中起作用(Langdale et al., 1989),在拟南芥叶片表皮毛(trichome)的间距中起作用(Larkin et al., 1996),并在维持拟南芥茎尖和根尖分生组织(apical meristem)细胞类型平衡中起作用(Scheres and Wolkenfelt, 1998; Fletcher and Meyerowitz, 2000; Irish and Jenik, 2001)。植物细胞间信号传导的机制基础仍有待阐明。植物中的一些信号传导过程似乎由跨膜受体样激酶(transmembrane receptor-like kinases)介导(Irish and Jenik, 2001);其他则利用胞间连丝(plasmodesmata)(第4章; Zambryski and Crawford, 2000)。 | |||
❙ 植物激素(PLANT HORMONES) | |||
植物激素(phytohormones)是化学信号,在调节生长和发育中起主要作用,因此在此简要讨论(Davies, P. J., 2004; Taiz and Zeiger, 2002; Crozier et al., 2000; Weyers and Paterson, 2001)。激素(hormone)一词(来自希腊语horman,意思是启动)是从动物生理学中借用的。动物激素的基本特征——它们在远离其合成部位的地方起作用——并不完全适用于植物激素。虽然一些植物激素在一个组织中产生并运输到另一个组织,在那里产生特定的生理反应,但其他植物激素在产生它们的同一组织内起作用。在这两种情况下,它们都通过作为细胞之间的化学信使或信号来帮助协调生长和发育。 | |||
植物激素具有多种活性。一些激素不是作为刺激物,而是具有抑制作用。对特定激素的反应不仅取决于其化学结构,还取决于其靶组织如何"解读"它。一种给定的激素可以在不同的组织中或在同一组织的不同发育阶段引起不同的反应。一些植物激素能够影响另一种激素的生物合成或干扰另一种激素的信号转导。组织可能需要不同量的激素。这种差异被称为敏感性(sensitivity)的差异。因此,植物系统可以通过改变激素浓度或改变对已经存在的激素的敏感性来调节激素信号的强度。 | |||
传统上,植物激素的五大类受到了最多的关注:生长素(auxins)、细胞分裂素(cytokinins)、乙烯(ethylene)、脱落酸(abscisic acid)和赤霉素(gibberellins) (Kende and Zeevaart, 1997)。然而,越来越清楚的是,植物还使用了其他化学信号(Creelman and Mullet, 1997),包括油菜素内酯(brassinosteroids)——一类天然存在的多羟基类固醇,已在许多植物中被鉴定,并且似乎是大多数植物组织正常生长所必需的;水杨酸(salicylic acid)——一种结构与阿司匹林相似的酚类化合物,其产生与抗病性相关,并与过敏反应有关;茉莉酸类(jasmonates)——一类被称为氧脂素(oxylipins)的化合物——在种子萌发、根生长、贮藏蛋白积累和防御蛋白合成的调节中发挥作用;系统素(systemin)——一种18个氨基酸的多肽——由受伤细胞分泌,然后通过韧皮部运输到上部未受伤的叶片,以激活对食草动物的化学防御,这种现象称为系统获得性抗性(systemic acquired resistance) (Hammond-Kosack and Jones, 2000);多胺(polyamines)——低分子量、强碱性的分子——对生长和发育至关重要,并影响有丝分裂和减数分裂过程;以及气体一氧化氮(nitric oxide, NO),已被发现作为激素和防御反应中的信号。据报道,NO抑制拟南芥(Arabidopsis)的花期转变(He, Y., et al., 2004)。在它们的多种活动中,激素之间相互作用;实际上,生长物质之间的相互作用和平衡,而不是单一物质的活动,调节正常的生长和发育。 | |||
在接下来的段落中,将考虑传统植物激素类群的一些显著特征。 | |||
生长素(Auxins) | |||
主要的天然生长素是吲哚-3-乙酸(indole-3-acetic acid, IAA)。IAA主要在叶原基和幼叶中合成,并涉及植物发育的许多方面,包括植物根-茎轴的整体极性,这是在胚胎发生期间建立的。这种结构极性可追溯到IAA在植物中的极性或单向运输。极性生长素运输通过特定膜结合流入(AUX1)和流出(PIN)载体的作用以细胞到细胞的方式进行(Steinmann et al., 1999; Friml et al., 2002; Marchant et al., 2002; Friml, 2003; Volger and Kuhlemeier, 2003)。从叶片向下到茎的生长素稳定流动导致生长素沿狭窄的细胞列流动,并导致连续维管组织束的形成(Aloni, 1995; Berleth and Mattsson, 2000; Berleth et al., 2000)——Sachs (1981)的管道化假说(canalization hypothesis)。 | |||
在茎和根中,极性运输(polar transport)始终是向基的(basipetal)——从茎尖和叶片向下运输到茎部,以及从根尖向根部基部(根-茎连接处)运输。极性生长素运输(auxin transport)的速度——每小时5到20厘米——比被动扩散(passive diffusion)的速度要快。除了生长素的极性运输外,最近还发现,成熟叶片中合成的大部分IAA显然是通过韧皮部以非极性的方式长距离运输到整个植物中,其速度远高于极性运输。在*Ricinus communis*的韧皮部(筛管)汁液中检测到相对较高浓度的游离IAA,表明生长素可能通过韧皮部长距离运输(Baker, 2000)。进一步的研究表明,在*Arabidopsis*中,生长素流入载体AUX1参与了叶片中的韧皮部装载(phloem loading)和根中的韧皮部卸载(phloem unloading)(Swarup et al., 2001; Marchant et al., 2002),这进一步支持了生长素在韧皮部中的运输。在具有次生生长的植物中,生长素运输也发生在维管形成层(vascular cambium)区域(Sundberg et al., 2000)。 | |||
在一项巧妙的研究中,Aloni及其同事(2003)结合分子和定位程序,展示了发育中的*Arabidopsis*叶片中游离生长素(IAA)产生的模式(图5.14)。托叶(stipules)是第一个主要的游离生长素高产部位。在发育中的叶片中,排水器(hydathodes)是游离生长素高产的主要部位,首先是叶尖的排水器,然后沿着边缘向基部推进。毛状体(trichomes)和叶肉细胞(mesophyll cells)是游离生长素产生的次要部位。在叶片发育过程中,游离生长素产生的部位和浓度从伸长的叶尖向扩展的边缘向基部转移,最后转移到叶片的中央区域。游离生长素产生部位和浓度的有序变化可能控制了叶片中脉序模式的形成和维管分化(vascular differentiation),排水器中生长素的大量产生诱导了中脉和次生维管束的分化,而叶片中——特别是与毛状体相关的区域——低游离生长素的产生诱导了三级和四级脉及脉端的分化。这项研究的结果与Aloni(2001)提出的叶脉假说(leaf-venation hypothesis)一致,该假说解释了真双子叶植物叶片中维管分化的激素控制。 | |||
一个名为VASCULAR HIGHWAY1 (VH1)的基因,其表达是原维管/原形成层细胞特异性的,已在*Arabidopsis*的发育叶片中被鉴定出来(Clay and Nelson, 2002)。VH1的表达模式与发育叶片中脉的形成模式相对应,并且正如Clay和Nelson(2002)所指出的,这与基于生长素产生和分布的模式化维管分化的管道化假说(canalization hypothesis)一致(Sachs, 1981)。 | |||
图5.14 | |||
在拟南芥(*Arabidopsis*)叶原基发育过程中,自由IAA(生长素)产生的位点(由点表示)和浓度(由点的大小表示)逐渐变化。IAA的初始产生发生在托叶(s)中(A)。箭头表示在叶片中,从分化的排水器(hydathodes)向下的基向极性IAA运动方向(B-D);箭头表示叶片中次级自由生长素产生位点的位置(D, E)。实验证据表明,尽管中脉向顶发育(B),但它是由基向极性IAA流诱导的。(引自Aloni, 2004, 图1。© 2004,经Springer Science and Business Media友好许可。) | |||
实验证据还表明,极性生长素运输在水稻(*Oryza sativa*)叶片的维管模式中起作用(Scarpella et al., 2002)。有研究提出,水稻的*Oshox1*基因在原形成层细胞中表达(Scarpella et al., 2000),通过增加其生长素传导特性促进原形成层细胞的命运决定(Scarpella et al., 2002)。 | |||
生长素提供了协调植物体内多个发育过程的信号(Berleth and Sachs, 2001)。生长素被认为在调节细胞分裂、伸长和分化的模式中起作用(Chen, 2001; Ljung et al., 2001; Friml, 2003)。在拟南芥叶片中,高水平的IAA与高细胞分裂率密切相关。分裂的叶肉组织中的IAA水平是仅通过伸长生长的组织的十倍。尽管最年轻的叶片表现出最高的IAA合成能力,但拟南芥幼苗的其他部分(包括子叶、扩展中的叶片和根)也显示出从头合成IAA的能力(Ljung et al., 2001)。由极性运动引起的生长素梯度在胚胎发生(Hobbie et al., 2000; Berleth, 2001; Hamann, 2001)、叶片维管模式(Mattsson et al., 1999; Aloni et al., 2003)以及茎和根的侧器官形成(Reinhardt et al., 2000; Casimiro et al., 2001; Paquette and Benfey, 2001; Scarpella et al., 2002; Bhalerao et al., 2002)中提供了重要的发育信号。生长素被认为在向重性和向光性(Marchant et al., 1999; Rashotte et al., 2001; Muday, 2001; Parry et al., 2001)以及茎和根顶端分生组织的组织和维持(Sachs, 1993; Sabatini et al., 1999; Doerner, 2000a, b; Kerk et al., 2000)中起作用。与乙烯一起,生长素在拟南芥根毛的发育中起重要作用(Rahman et al., 2002)。生长素的其他一些活性包括作为顶端优势现象的一部分抑制腋芽发育以及延缓脱落。 | |||
细胞分裂素(Cytokinins) | |||
细胞分裂素(cytokinins)之所以得名,是因为它们与生长素(auxin)共同作用,促进细胞分裂。根部是细胞分裂素的丰富来源,它们通过木质部从根部运输到茎部(Letham, 1994)。关于根部合成的细胞分裂素的调节功能之一,是触发侧芽从休眠状态中释放,与生长素的作用相反,后者抑制侧芽的生长。然而,通过转基因植物的实验结果表明,释放芽从休眠状态需要的是局部合成的细胞分裂素,而非根部来源的细胞分裂素(Schmülling, 2002)。根部来源的细胞分裂素更可能的作用是传递关于营养状态的信息,特别是氮营养,在根和茎之间(Sakakibara et al., 1998; Yong et al., 2000)。根冠(rootcap)中产生的细胞分裂素与拟南芥(Arabidopsis)根部对重力的早期反应有关(Aloni et al., 2004)。细胞分裂素在胚胎发生过程中原维管组织(provascular tissue)的形成(Mähönen et al., 2000)以及胚胎后发育过程中分生组织(meristem)活性和器官生长的控制中起着重要作用(Coenen and Lomax, 1997)。尽管它们是茎部发育的促进者,细胞分裂素却是根部发育的抑制剂(Werner et al., 2001)。 | |||
乙烯(Ethylene) | |||
乙烯(ethylene),一种简单的碳氢化合物 $\left(\mathrm{{H}}_{2}\mathrm{{C}}{=}\mathrm{{CH}}_{2}\right)$,几乎可以由种子植物的所有部分产生(Mattoo and Suttle, 1991)。作为一种气体,它通过扩散从其合成部位移动。乙烯的产生速率在植物组织之间有所不同,并取决于发育阶段。幼苗的茎尖是乙烯产生的重要部位,茎的节区域也是如此,它们产生的乙烯比节间多得多(在相同组织重量的基础上)。 | |||
乙烯的产生在叶片脱落和一些果实成熟期间增加。在鳄梨、番茄和苹果、梨等核果类果实的成熟过程中,细胞呼吸显著增加。这一阶段被称为呼吸跃变期(climacteric),这些果实被称为呼吸跃变型果实(climacteric fruits)。在呼吸跃变型果实中,乙烯合成的增加先于许多成熟过程,并对其负责。乙烯产生的增加也发生在大多数组织中,以响应生物(疾病、昆虫损害)和非生物(洪水、温度、干旱)胁迫(Lynch and Brown, 1997)。如前所述,溶生通气组织(lysigenous aerenchyma)的形成是乙烯介导的对洪水的响应(Grichko and Glick, 2001)。 | |||
乙烯的作用通常与生长素相反。生长素阻止叶片脱落,而乙烯促进叶片脱落。脱落区(abscission zone)中的乙烯产生受生长素调节。在大多数植物物种中,乙烯对细胞伸长有抑制作用(Abeles et al., 1992);而生长素促进细胞伸长。然而,在一些半水生植物(Ranunculus sceleratus, Callitriche platycarpa, Nymphoides peltata, 深水稻)中,乙烯引发茎的快速生长。 | |||
脱落酸(Abscisic Acid) | |||
脱落酸(Abscisic Acid, ABA)这个化合物的名称其实是个误称。之所以这样命名,是因为最初人们认为它与脱落(abscission)有关,而现在已经知道脱落是由乙烯(ethylene)触发的。ABA几乎在所有含有淀粉体(amyloplast)或叶绿体(chloroplast)的细胞中合成,因此可以在从根尖到茎尖的活体组织中检测到(Milborrow, 1984)。ABA在木质部和韧皮部中都有运输,尽管在韧皮部中通常含量更高。根部响应水分胁迫合成的ABA通过木质部向上运输到叶片,在那里可以诱导气孔关闭(第9章;Davies和Zhang, 1991)。 | |||
在许多植物物种中,ABA水平在种子发育早期增加,刺激种子贮藏蛋白(seed storage proteins)的产生(Koornneef等, 1989)并防止过早萌发。许多种子的休眠打破与种子中ABA水平的下降有关。 | |||
赤霉素(Gibberellins) | |||
赤霉素(Gibberellins, GAs)是四环二萜类化合物(tetracyclic diterpenoids)。已经鉴定出125多种GAs,但只有少数已知具有生物活性。发育中的种子和果实表现出最高的GA水平。豌豆幼苗中正在活跃生长的幼芽、叶片和上部节间已被确定为GA合成的部位(Coolbaugh, 1985; Sherriff等, 1994)。茎中合成的GAs可以通过韧皮部运输到整个植株。 | |||
GAs通过刺激细胞分裂和细胞伸长对茎和叶的伸长有显著影响。它们在茎生长中的作用在应用于许多矮化植物时最为明显。在GA处理下,这些植物与正常的非突变植物无法区分,表明突变体无法合成GA,而生长需要GA。拟南芥gal-3矮化突变体(Zeevaart和Talon, 1992)说明了GA缺乏的多重影响。除了矮化外,这些植物更浓密,叶片颜色更深。此外,gal-3开花延迟,gal-3花雄性不育,gal-3种子无法萌发。添加GA后,突变体的所有野生型特征都得以恢复。对烟草和豌豆的研究表明,茎中正常的$\mathbf{GA}_{1}$生物合成需要来自顶芽的IAA(Ross等, 2002)。$\mathbf{GA}_{1}$可能是控制茎伸长的唯一GA。$\mathbf{GA}_{1}$诱导的伸长通常伴随着IAA含量的增加。 | |||
GAs控制着广泛的植物发育过程(Richards等, 2001)。它们对豌豆的正常根伸长(Yaxley等, 2001)、种子发育和拟南芥的花粉管生长(Singh等, 2002)很重要,并且对许多植物物种的种子萌发至关重要(Yamaguchi和Kamiya, 2002)。在许多种子植物中,GAs可以替代种子萌发所需的打破休眠的低温或光照。如前所述,在谷物中,GAs调节酶($\upalpha$-淀粉酶)的产生和分泌,导致胚乳中储存的淀粉水解。GAs也可能作为长日照开花信号(King等, 2001)。对长日照植物和二年生植物施用GAs可能会导致抽薹和开花,而无需适当的低温或长日照暴露。{{:Esau's Plant Anatomy}} | |||
{{学科分类}} | {{学科分类}} | ||
[[Category:植物学]] | [[Category:植物学]] | ||
2026年3月2日 (一) 10:13的最新版本
❙ 分生组织 (Meristems)
从合子分裂开始,维管植物产生新细胞并发育出新器官,通常直到其死亡。在早期胚胎发育过程中,细胞繁殖发生在整个生物体中,但随着胚胎发育成为独立的植物体,新细胞的增加逐渐局限于某些区域。这些现在局部化的生长组织(growing tissues)仍然保持胚胎特征,并在植物的整个生命周期中持续存在,因此其植物体是成体(adult)和幼体(juvenile)组织的复合体。这些主要参与新细胞形成的胚胎组织区域就是分生组织(meristems)(图5.1; McManus和Veit, 2002)。
细胞繁殖局限于植物的某些部位是进化特化(evolutionary specialization)的结果。在最原始的植物中,所有细胞基本上都是相似的,并且都参与细胞增殖、光合作用、分泌、储存和运输等重要活动。随着细胞和组织的逐步特化,细胞繁殖的功能主要局限于分生组织及其直接衍生物。
术语"分生组织"(源自希腊语merismos,意为分裂)强调了细胞分裂活动作为分生组织(meristematic tissue)的特征。除了分生组织之外,其他活组织也可能被诱导产生新细胞,但分生组织无限期地保持这种活动,因为它们不仅向植物体添加细胞,而且还自我延续(self-perpetuate);也就是说,分生组织中细胞分裂的一些产物不会发育成成体细胞,而是保持分生状态。那些维持分生组织作为新细胞持续来源的细胞被称为起始细胞(initiating cells)、分生组织起始细胞(meristematic initials),或简称为initials。它们的产物在经过不定次数的细胞分裂后产生体细胞(body cells),这些产物就是起始细胞的衍生物(derivatives)。也可以说,一个分裂细胞是衍生物的前体(precursor)。分生组织中的某个起始细胞是两个衍生物的前体,其中一个衍生物是新的起始细胞,另一个是体细胞的前体。
起始细胞和衍生物的概念应包括一个限定条件,即起始细胞与其衍生物没有本质上的区别。起始细胞和衍生物的概念将从不同角度考虑,与维管形成层(vascular cambium)(第12章)以及茎和根顶端分生组织(apical meristems)的描述相关(第6章)。这里只需指出,根据一种普遍观点,分生组织中的某些细胞之所以充当起始细胞,主要是因为它们占据了进行这种活动的适当位置。
保留分生组织和产生新器官的能力将高等植物与高等动物区分开来。在后者中,胚胎发育过程中产生固定数量的器官,尽管完全发育的动物体内的成体组织和器官在整个生命周期中由存在于组织或器官内的细胞群维持。这些细胞被称为干细胞(stem cell)(Weissman, 2000; Fuchs, E., and Segre, 2000; Weissman et al., 2001; Lanza et al., 2004a, b),已被比作植物分生组织的原始细胞,并且术语"干细胞"已被许多植物生物学家采用。本书未采用"干细胞"这一术语。
尽管动物干细胞可能与植物分生组织的原始细胞类似,但它们并不等同于原始细胞。原始细胞是全能的(totipotent)(来自拉丁语totus,意为"全部");也就是说,它们有能力产生所有类型的细胞,甚至发育成完整的植物。在大多数动物中,只有受精卵或受精卵(fertilized egg)是真正全能的。胚胎干细胞(embryonic stem cell)几乎全能,但在个体发育(ontogeny)早期(囊胚期(blastocyst stage)后不久),它们会产生成体干细胞(adult stem cell),这些干细胞是多能的(pluripotent),并且能够产生的细胞类型数量有限——通常是它们所在的成体组织和器官中的那些细胞类型(Lanza et al., 2004a, b)。据报道,一些成体干细胞能够从其原始生态位迁移(原始细胞不具备这一特性),并呈现出新环境的典型形态和功能(Blau et al., 2001)。
成熟植物部分中的许多活细胞在发育上仍然是全能的。因此,植物的发育和组织可以被描述为具有可塑性(plasticity)(Pigliucci, 1998),这一特性被解释为对固着生活形式的进化反应。由于植物是静止的,它无法逃离其生长的环境,必须通过不经历不可逆的变化来适应不利的环境条件和捕食(Trewavas, 1980)。
分生组织的分类
分生组织的常见分类基于它们在植物体内的位置。有顶端分生组织(apical meristem),即位于主茎和侧枝以及根尖的分生组织(图5.1),和侧生分生组织(lateral meristem),即与轴(通常是茎和根)的侧面平行排列的分生组织。维管形成层(vascular cambium)和木栓形成层(cork cambium)是侧生分生组织。
基于分生组织位置的第三个术语是居间分生组织(intercalary meristem)。该术语指的是源自顶端分生组织并继续在距该分生组织一定距离处保持分生组织活性的分生组织。居间(intercalary)一词意味着分生组织被插入(intercalated)在不再具有分生组织活性的组织之间。最著名的居间分生组织例子是单子叶植物,特别是禾本科植物节间(internode)和叶鞘(leaf sheath)中的分生组织(图5.2)。这些类型的生长区域包含分化的传导组织元素,并最终转化为成熟组织,尽管它们的薄壁组织细胞长期保持恢复生长的能力(第7章)。作为分生组织,居间分生组织与顶端分生组织和侧生分生组织不属于同一等级,因为它们不包含可以称为原始细胞的细胞。
在描述茎尖和根尖的初级分化时,初始细胞及其最近的衍生物经常与部分分化但仍具分生能力的下方组织区分开来,称为原分生组织(promeristem或protomeristem;Jackson, 1953)。下方的分生组织根据它们衍生的组织系统进行分类,即原表皮(protoderm),分化为表皮;原形成层(procambium,也称为provascular tissue*),产生初生维管组织;以及基本分生组织(ground meristem),是基本组织系统的前体。如果广泛使用分生组织这一术语,原表皮层、原形成层和基本分生组织被称为初生分生组织(Haberlandt, 1914)。在更狭义的分生组织定义(初始细胞及其直接衍生物的组合)中,这三种组织构成了部分确定的初生分生组织。
*一些研究人员区分provascular cells和 procam bial cells,provascular cells被认为是uncommitted but vascular-competent cells,而procambial cells是开始已经向木质部和韧皮部分化的细胞。
术语原表皮层、原形成层和基本分生组织非常适合描述植物器官中组织分化的模式,并且它们与成熟组织同样简单且方便的分类相对应,即表皮、维管和基本组织系统,这些在第一章中已经讨论过。只要理解这些组织的未来发育至少部分确定,原表皮层、原形成层和基本分生组织被称为分生组织或分生组织似乎并不重要。
分生组织也可以根据产生其初始细胞的细胞性质进行分类。如果初始细胞是胚胎细胞的直接后代,这些胚胎细胞从未停止与分生活动相关,那么由此产生的分生组织称为初生分生组织。然而,如果初始细胞来自已经分化后又恢复分生活动的细胞,那么由此产生的分生组织称为次生分生组织。
木栓形成层(phellogen)是次生分生组织(secondary meristem)的一个很好的例子,因为它起源于表皮或皮层和树皮深层中的各种薄壁组织(parenchymatous tissues)。维管形成层(vascular cambium)的起源更为多样,与初生维管系统(primary vascular system)的组织有关。该系统从原形成层(procambium)分化而来,而原形成层最终来源于顶端分生组织(apical meristem)。通常,原形成层和由其产生的初生维管组织以束(fascicles)的形式存在,或多或少已经被束间薄壁组织(interfascicular parenchyma)分隔开(图5.3A)。在初生生长结束时,初生木质部(primary xylem)和初生韧皮部(primary phloem)之间的剩余原形成层成为形成层的束内部分(fascicular part)。这种形成层由束间薄壁组织中产生的束间形成层(interfascicular cambium)补充(图5.3B)。因此,形成了一个连续的圆柱形形成层(横切面呈环状),部分起源于束内,部分起源于束间。根据初生和次生分生组织的定义,束内形成层是初生分生组织——通过原形成层从顶端分生组织衍生而来——而束间形成层是次生分生组织——从薄壁组织衍生而来,其次恢复了分生组织的活性。
在许多木本植物中,起源于这两个部位的形成层部分在随后的次生生长中变得难以区分。此外,鉴于从组织培养工作中获得的证据表明,活的植物细胞长期保持其生长潜力(Street, 1977),束间薄壁组织中形成层分裂的出现并不表明所涉及细胞的特征发生了重大变化。因此,将维管形成层部分归为初生分生组织,部分归为次生分生组织纯粹是理论上的。然而,这一结论并不影响将成熟组织分为初生和次生的分类价值,如第1章所述。
分生组织细胞的特征
分生组织细胞基本上与年轻的薄壁细胞相似。在细胞分裂期间,茎尖的细胞壁相对较薄,储存物质较少,其质体处于前质体(proplastid)阶段。内质网(endoplasmic reticulum)数量较少,线粒体(mitochondria)的嵴(cristae)较少。高尔基体(Golgi bodies)和微管(microtubules)存在,这是具有生长细胞壁的细胞的特征。液泡(vacuoles)小而分散。
顶端分生组织的深层可能具有更高的液泡化程度并含有淀粉(Steeves et al., 1969)。在一些分类群中,特别是蕨类植物、针叶树和银杏,在顶端圆顶(apical dome)的最高位置出现明显液泡化的细胞(第6章)。在种子萌发之前,胚胎的分生组织含有储存物质。
在细胞分裂期间,维管形成层细胞高度液泡化,一个或两个大液泡将致密的细胞质限制在薄壁层(parietal layer)中(第12章),其中含有粗糙内质网(rough endoplasmic reticulum)和其他细胞成分。在休眠期间,液泡系统呈现为许多相互连接的液泡。冬季液泡有时含有多酚(polyphenols)和蛋白质体(protein bodies)。此时,内质网是光滑的,核糖体(ribosomes)游离在细胞质中。
分生组织细胞通常被描述为具有较大的细胞核。但细胞大小与核大小的比率——细胞核比率(cytonuclear ratio)——变化很大(Trombetta, 1942)。一般来说,较大的分生组织细胞的细胞核相对于细胞大小来说较小。
在有丝分裂活性变化期间,细胞核显示出特征性的结构变化(Cottignies, 1977)。例如,在休眠的形成层中,当细胞核被阻滞在有丝分裂周期的$\mathbf{G}_{1}$期时,RNA合成缺失,核仁小、致密,且主要由纤维状结构组成。当细胞活跃且RNA合成进行时,核仁较大,具有明显的液泡和广泛的颗粒区,与纤维区交织在一起。
前面的综述表明,分生组织细胞在大小、形状和细胞质特征上存在差异。为了认识到这种变异性,术语eumeristem(真分生组织)被建议用于指定由小的、近似等径的、壁薄且富含细胞质的细胞组成的分生组织(Kaplan, R., 1937)。出于描述目的,这个术语通常使用起来很方便,但它不应暗示某些细胞比其他细胞更典型地具有分生组织特性。
分生组织中的生长模式
分生组织和分生组织组织显示出由于细胞分裂和扩大模式的差异而产生的细胞排列的多样性。仅有一个起始细胞占据顶端的顶端分生组织(木贼属和许多蕨类植物)具有最近形成的、仍然是分生组织的细胞的有序分布(第6章)。在种子植物中,细胞分裂的模式似乎不那么精确。然而,它并不是随机的,因为顶端分生组织作为一个有组织的整体生长,单个细胞的分裂和扩大与生长的内部分布和顶端的外部形式有关。这些相关影响导致分生组织中独特区域的分化。在分生组织的某些部分,细胞可能分裂缓慢并达到相当大的尺寸;在其他部分,它们可能频繁分裂并保持较小。一些细胞复合体在各个平面上分裂(体积生长),而其他细胞仅在与分生组织表面成直角的壁上分裂(垂周分裂,表面生长)。
侧生分生组织特别以与器官最近表面平行的分裂为特征(图5.4A;平周分裂),这导致与轴半径平行的细胞行的建立(径向序列或排列)和器官厚度的增加。在圆柱体(如茎和根)中,术语切向分裂(或切向纵向)通常用于代替平周分裂。如果垂周分裂与圆柱体的半径平行发生,则称为径向垂周(或径向纵向)分裂(图5.4B)。如果新壁与...
图5.4
展示圆柱形植物结构分裂面的示意图。A,平周分裂(与表面平行)。B,径向垂周分裂(与半径平行)。C,横向分裂(与长轴成直角的垂周分裂)。
在圆柱体的纵轴上,垂周分裂是横向的(图5.4C)。
来自同一顶端分生组织(apical meristem)的器官可能呈现出不同的形态,因为顶端分生组织的仍具分生能力的衍生物(初生分生组织,primary meristems)通常表现出不同的生长模式。其中一些模式非常典型,以至于表现出这些模式的分生组织获得了特殊的名称。这些名称包括块状分生组织(mass meristem或block meristem)、肋状分生组织(rib meristem或file meristem)和板状分生组织(plate meristem)(Schiepp, 1926)。块状分生组织通过所有平面的分裂生长,产生等径的、球形的或没有明确形状的体。例如,在孢子、精子(在无种子维管植物中)和胚乳的形成过程中会发生这种生长。在许多被子植物胚胎发育的某个阶段,不同平面的分裂与球形形状相关。肋状分生组织通过垂直于细胞行纵轴的分裂产生一系列平行的纵向细胞列(“肋”)。这种生长模式发生在伸长的圆柱形植物部分中,如根的皮层以及茎的髓和皮层(图5.1)。板状分生组织主要表现出垂周分裂,因此最初在幼嫩器官中建立的层数不会进一步增加,从而产生板状结构。被子植物叶片的扁平叶片是板状分生组织生长的结果(图5.5)。板状分生组织和肋状分生组织是主要发生在基本分生组织(ground meristem)中的生长形式。它们与植物体的两种基本形式相关,即叶状器官的薄片状扩展叶片(lamina或blade)和根、茎、叶柄等伸长的圆柱形植物部分。
分生组织活动与植物生长
分生组织及其分生衍生物与广义上的生长有关,即体积和表面积的不可逆增加。在多细胞植物中,生长基于两个过程:细胞分裂(cell division)和细胞扩大(cell enlargement)。分生组织初始细胞的最近衍生物通过细胞分裂产生其他衍生物,并且连续的衍生物世代会增大体积。细胞扩大逐渐取代细胞分裂,最终完全取代它。当离分生组织初始细胞最远的衍生物停止分裂和扩大时,它们获得了所在组织的特征;也就是说,细胞分化并最终成熟。
尽管细胞分裂本身并不增加生长实体的体积(Green, 1969, 1976),但细胞的增加是多细胞生物生长的基本要求。细胞分裂和细胞扩大是生长过程的不同阶段,其中细胞扩大决定了植物的最终大小。
图5.5
图示两种大小的*Lupinus*小叶边缘的分生组织活动:A、B,$600\upmu\mathrm{m}$长;C、D,$8500\upmu\mathrm{m}$长。短线表示分裂细胞的赤道面或细胞板。分裂图通过连续切片记录并组装,A和C中为垂周分裂(anticlinal division),B和D中为平周分裂(periclinal division)。边缘的平周分裂建立了叶片的层数。垂周分裂扩展了各层(板状分生组织活动)。(来自Esau, 1977;重绘自Fuchs, 1968。)
及其部分。作为细胞个体发育(development of an individual entity)的一个完整步骤,细胞的扩大(expansion)是分裂和成熟阶段之间的过渡(Hanson and Trewavas, 1982)。
细胞分裂很少不伴随细胞扩大,至少在一定程度上,分裂细胞群中维持了原始细胞的大小。一些被子植物胚胎在这方面是个例外。在合子发育成胚胎的前两到三个细胞分裂周期中,几乎检测不到细胞扩大(Dyer, 1976)。在无实体大小增加的情况下发生的细胞分裂也出现在小孢子(花粉粒)内雄配子体的形成过程中。同样,当多核胚乳转化为细胞组织时,细胞分裂也不伴随细胞扩大。然而,通常生长可以大致分为两个阶段:通过细胞分裂和有限的细胞扩大进行的生长,以及没有细胞分裂但伴随大量细胞扩大的生长。
图5.6
木本被子植物示意图,展示了茎和根的分枝,通过次生生长(secondary growth)增加茎和根的厚度,以及在增厚的轴上形成周皮(periderm)和树皮(bark)。主茎和侧枝(腋生)的顶端带有不同大小的叶原基(leaf primordia)。根毛出现在主根(直根)和侧根顶端的一定距离处。(来自Esau, 1977;改编自Rauh, 1950。)
由于顶端分生组织(apical meristem)存在于所有茎和根的顶端,无论是主茎还是侧枝,因此在一株植物中其数量相对较多。经历茎和根次生增厚的维管植物(图5.6)还拥有广泛的分生组织,即维管形成层(vascular cambium)和木栓形成层(cork cambium)。植物在顶端分生组织中启动的初生生长(primary growth)扩展了植物体,决定了其高度,并通过增加其表面积,扩大了与空气和土壤的接触面积。最终,初生生长还产生了生殖器官。由形成层活动引起的次生生长增加了传导组织的体积,并形成了支持和保护组织。
通常,植物上存在的所有顶端分生组织不会同时活跃。在顶芽活跃生长时抑制侧芽生长(顶端优势(apical dominance);Cline, 1997, 2000;Napoli et al., 1999;Shimizu-Sato and Mori, 2001)是一种常见现象。然后,形成层的活动强度会有所不同,顶端和侧生分生组织的分生组织活动可能会表现出季节性波动,在温带地区冬季细胞分裂会减慢或完全停止。
❙ 分化(DIFFERENTIATION)
术语和概念
植物的发育包括紧密相关的生长( growth )、分化( differentiation )和形态发生( morphogenesis )现象。分化是指分生组织衍生物的后代在形态、结构和功能上的一系列变化,以及它们组织成组织和器官的过程。我们可以谈论单个细胞的分化、组织( histogenesis )的分化、器官( organogenesis )的分化以及整个植物的分化。分化也指受精卵细胞产生后代细胞的过程,这些细胞表现出越来越明显的异质性、特化和模式化组织。这个术语并不精确,尤其是当它被用来对比分化细胞和未分化细胞时。分生细胞和卵细胞在细胞学上是复杂的,它们本身就是分化的产物。将这些细胞描述为未分化只是一种惯例(Harris, 1974)。
分化的程度和伴随的特化(对特定功能的结构适应)差异很大(图5.7)。一些细胞与其分生前体相比变化相对较小,并保留了分裂的能力(各种薄壁细胞)。其他细胞则发生了更深刻的改变,失去了大部分或全部分生潜力(筛管分子、乳汁管、管状分子、各种石细胞)。因此,在多细胞体中分化的细胞不仅与其分生前体不同,也与同一植物其他组织中的细胞不同。
从某种意义上说,各种分化的细胞可以被称为成熟细胞,因为它们已经达到了某种特化和生理稳定性,这通常是成年植物某些组织组成部分的特征。这种成熟的定义必须包括一个限定条件,即具有完整原生质体的成熟细胞在适当刺激下可能会重新恢复分生活动。这种刺激可能是由意外伤害、寄生虫入侵或病原体感染引起的(Beers and McDowell, 2001)。正常的内应力导致组织的选择性分解可能会引发类似于“修复反应”的生长反应。这种反应在轴次生增粗过程中的树皮中以及叶片或其他器官通常从植物上脱落的离区中很常见。通过将细胞从植物中分离出来并在体外培养以刺激其恢复生长,已成为研究成熟细胞分生潜力的特别有用的实验方法(Street, 1977)。
在研究非分生细胞恢复分生活动的过程中,术语去分化( dedifferentiation )——失去先前获得的特征——和再分化( redifferentiation )——获得新特征——经常被使用。整个过程被称为转分化( transdifferentiation )。与分化一样,去分化也不是一个精确的术语。去分化的细胞不会恢复到受精卵的状态,甚至不会恢复到胚胎细胞的状态,但它们可能会失去一些特化特征,并增加与DNA和蛋白质合成相关的亚细胞成分的数量。
关于分化(differentiation)的讨论可能会涉及到决定(determination)的概念(McDaniel, 1984a, b; Lyndon, 1998),这一现象可以被视为分化的一个方面。决定意味着对特定发育过程的渐进性承诺,导致恢复生长能力的减弱或丧失。一些细胞比其他细胞更早、更完全地决定,而一些细胞在分化后仍保持其全能性(totipotency)。分化与生长相关,这两种现象都发生在从亚细胞结构到整个植物的所有形态学水平上。在没有分化的情况下生长见于异常结构,如肿瘤。愈伤组织(callus tissue)也可能被诱导在几乎没有分化的情况下生长。
术语"能力(competence)"经常出现在分化的讨论中。正如McDaniel (1984a, b)所定义的,能力指的是细胞响应特定信号(如光)发育的能力。它意味着有能力的细胞能够识别信号并将其转化为反应。
在发育过程中,植物呈现出特定的形态。因此,植物经历形态发生(morphogenesis)(来自希腊语中表示形状和起源的单词)。该术语通常用于指代外部形态和内部组织,就像分化一样,形态发生在从细胞成分到整个植物的所有组织水平上都有体现。然而,D. R. Kaplan和W. Hagemann (1991)强调,尽管
图5.7
图示了一些可能起源于原形成层(procambium)或维管形成层(vascular cambium)分生组织细胞(meristematic cell)的细胞类型。这里描绘的分生组织细胞(中心)具有单个大液泡,是维管形成层分生组织细胞的典型特征。原形成层细胞通常含有几个小液泡。所有这些细胞的分生组织细胞或前体都具有相同的基因组。不同的细胞类型之所以彼此不同,是因为它们表达其他细胞类型不表达的基因集。在描绘的四种细胞类型中,薄壁组织细胞(parenchyma cell)是最不特化的。成熟的导管分子(vessel element)(专门用于水分传导)和成熟的纤维(fiber)(专门用于支持)都缺乏原生质体(protoplast)。成熟的筛管分子(sieve-tube element)(专门用于糖类和其他同化物的运输)保留了活的原生质体,但没有细胞核和液泡。它依赖其姐妹细胞——伴胞(companion cell)来维持生命。(来自Raven等,2005年。)
植物解剖学和形态学的某些方面是相关的,但细胞和组织分化遵循器官发生(organogenesis)或形态发生。注意到一些植物生物学家在解释植物发育机制时倾向于混淆解剖学特征和形态学特征,D. R. Kaplan (2001)进一步强调"虽然解剖学可能由形态学决定...,但解剖学并不决定形态学。"
衰老(程序性细胞死亡)(Senescence, Programmed Cell Death)
植物因衰老而自然终止生命可以被视为植物发育的一个正常阶段,是分化和成熟事件的后续(Leopold, 1978; Noodén和Leopold,
1988; Greenberg, 1996)。术语衰老(senescence)特指导致生物体死亡的一系列变化(Noodén and Thompson, 1985; Greenberg, 1996; Pennell and Lamb, 1997)。衰老可能影响整个生物体或其某些器官、组织或细胞。一年生植物(monocarpy: 仅结果一次)在其生命周期中仅开花一次,在一个季节内衰老。在落叶树中,叶子通常在季节性生长结束时衰老。果实在几周内成熟和衰老,离体的叶子和花朵在几天内衰老。衰老的单个细胞是根冠细胞,它们不断从生长的根上脱落。由于衰老在植物生命中有序发生,并且是一个活跃的退化过程,因此被认为是由基因控制的或程序化的——一个程序性细胞死亡(programmed cell death)的过程(Buchanan-Wollaston, 1997; Noodén et al., 1997; Dangl et al., 2000; Kuriyama and Fukuda, 2002)。
衰老可以由化学物质(包括生长物质)和环境条件控制(Dangl et al., 2000)。例如,用生长素(auxin)和细胞分裂素(cytokinins)处理大豆叶片,可以防止通常由种子发育引起的衰老(Thimann, 1978)。处理过的叶片保持了光合作用和氮同化能力,而不是将储备物质释放到生殖结构中并变得衰老。相反,乙烯(ethylene)可以诱导衰老(Grbic and Bleecker, 1995),它刺激了一系列衰老相关基因(senescence-associated genes, SAGs)的表达(Lohman et al., 1994)。
尽管衰老(senescence)一词源自拉丁语senesco,意为变老,但它并不被认为是与老化(aging)同义的(Leopold, 1978; Noodén and Thompson, 1985; Noodén, 1988)。与衰老一样,老化是个体生物生命周期的一个组成部分,并且不容易与衰老区分开来。老化被定义为降低生物体活力但不致命的累积变化。然而,老化可能导致衰老。老化一词的模糊性因其在实验工作中的使用而增强,用于表示在刺激代谢活动增加的条件下培养贮藏组织切片的做法。这种"老化"应称为复壮(rejuvenation)(Beevers, 1976)。
叶片衰老细胞中常见的变化包括叶绿素含量下降、红色(花青素)和黄色(类胡萝卜素)色素含量增加、蛋白质降解和核酸含量减少,以及细胞通透性增加(Leopold, 1978; Huang et al., 1997; Fink, 1999; Jing et al., 2003)。通透性的增加与膜脂质(membrane lipids)的紊乱有关(Simon, 1977; Thompson et al., 1997)。在自然衰老的小麦叶片中,叶绿体以质体小球(plastoglobuli)的形式积累脂质,基粒(grana)和基粒间片层(intergrana lamellae)膨胀并破裂成囊泡,基质(stroma)解体,最终叶绿体被膜破裂并释放细胞器内容物(Hurkman, 1979)。在衰老过程中,细胞的大部分生化过程都用于回收和重新分配代谢物和结构物质,特别是氮和磷的储备。过氧化物酶体(peroxisomes)转化为乙醛酸循环体(glyoxysomes),将脂质转化为糖类。在绿色细胞中,大部分蛋白质由位于叶绿体基质相中的Rubisco(核酮糖-1,5-二磷酸羧化酶/加氧酶)组成。迄今为止,已在多种植物物种中鉴定出100多个所谓的衰老相关基因(senescence-associated genes),这些基因的表达水平在叶片衰老期间上调(参见Jing et al., 2003引用的文献)。
植物中程序性细胞死亡(programmed cell death)的其他例子包括: - 导管分子(tracheary elements)的成熟(第10章;Fukuda, 1997); - 根部通气组织(aerenchyma tissue)的形成(第7章),以应对由洪水引起的缺氧(hypoxia)(Drew et al., 2000); - 胚胎发生过程中胚柄(suspensor)的破坏(Wredle et al., 2001); - 大孢子发生(megagametogenesis)期间四个大孢子中三个的死亡; - 谷物糊粉层细胞(aleurone cells)在产生大量$\upalpha$-淀粉酶后的死亡,这些酶是分解和动员淀粉以提供幼苗发育所需能量的关键(Fath et al., 2000; Richards et al., 2001); - 叶片形状的发育重塑(Gunawardena et al., 2004)。
程序性细胞死亡还在抵抗病原体(pathogens)中发挥重要作用(Mittler et al., 1997)。由病原体攻击引发的快速细胞死亡——称为超敏反应(hypersensitive response, HR)——与主动抗性密切相关(Greenberg, 1997; Pontier et al., 1998; Lam et al., 2001; Loake, 2001)。HR抵抗病原体的确切机制仍存在争议。有观点认为,HR通过直接杀死病原体和/或干扰其营养获取来限制其生长(Heath, 2000)。
植物中的程序性细胞死亡(programmed cell death)由激素信号触发,涉及胞质$\mathrm{Ca}^{2+}$浓度的变化(He et al., 1996; Huang et al., 1997),以及液泡中隔离的水解酶的激活。随着液泡的崩溃,酶被释放出来,使其能够攻击原生质体的细胞核和细胞质成分。乙烯(ethylene)在缺氧后诱导根部的程序性细胞死亡和通气组织(aerenchyma)的形成,并且如前所述,促进叶片衰老(He et al., 1996; Drew et al., 2000)。当添加到刚刚完成S期的烟草TBY-2细胞时,乙烯在细胞周期的${\bf G}_{2}/{\bf M}$检查点导致了一个显著的死亡高峰,这支持了程序性细胞死亡可能与细胞周期检查点紧密相关的假设(Herbert et al., 2001)。糊粉层细胞(aleurone cells)中的程序性细胞死亡由赤霉酸(gibberellic acid)启动(Fath et al., 2000),而油菜素内酯(brassinosteroids)已被证明可以诱导管状分子(tracheary elements)中的程序性细胞死亡(Yamamoto et al., 2001)。
术语程序性细胞死亡和细胞凋亡(apoptosis)经常互换使用。然而,细胞凋亡最初用于指代动物细胞中程序性细胞死亡的特定特征(第2章; Kerr et al., 1972; Kerr and Harmon, 1991)。这些特征包括核收缩、染色体凝聚、DNA断裂、细胞收缩、膜泡化以及形成被邻近细胞吞噬和降解的膜结合“凋亡小体(apoptotic bodies)”。迄今为止,植物细胞中记录的程序性细胞死亡均不具备细胞凋亡的所有特征(Lee and Chen, 2002; Watanabe et al., 2002; 以及其中引用的文献)。
分化过程中的细胞变化
在分化过程中,组织多样性源于单个细胞特征的变化以及细胞间关系的改变。或多或少分化细胞的共同特征,包括单个细胞组分的结构和功能,将在第2章和第3章中描述。细胞分化过程中细胞壁结构的变化将在第4章中讨论。初生和次生细胞壁厚度的差异增加、细胞壁质地和化学性质的变化以及特殊雕刻图案的发育引入了细胞之间的差异。
被子植物分化细胞中常见的细胞学现象是内多倍性
内多倍性(Endopolyploidy)是指在核膜内发生DNA复制周期而不形成纺锤体的情况。因此,新形成的DNA链保留在同一核内,使核成为多倍体。这种类型的DNA复制周期称为内周期(Endocycle)(Nagl, 1978, 1981)。在一些内周期中,会发生类似于有丝分裂的结构变化,复制的DNA链成为独立的染色体(内周期有丝分裂周期)。植物中最常见的内周期是内复制(Endoreduplication)或内复制(Endoreplication)周期,其中不发生类似有丝分裂的结构变化(D’Amato, 1998; Traas et al., 1998; Joubès and Chevalier, 2000; Edgar and Orr-Weaver, 2001)。在内复制过程中,会形成多线染色体(Polytene chromosomes)。这些染色体包含许多以电缆形式并排连接的DNA链。因此,多线性是由于DNA复制而不分离姐妹染色体,因此染色体数量不变的结果。
内周期有时被解释为没有功能意义的异常现象。根据另一种观点,涉及内周期的生长具有重要的优势,因为它提供了一种增加基因表达水平的机制(Nagl, 1981; Larkins et al., 2001)。此外,在内周期期间,RNA合成不会像在有丝分裂周期中那样中断。因此,细胞具有持续高水平的RNA和蛋白质合成,这些活动促进了快速生长和早期进入功能状态。相比之下,正在进行有丝分裂活动的生长组织在承担成熟生理活动方面表现出延迟。例如,当Phaseolus的胚体仍然表现出分生组织活动时,含有多线染色体的胚柄是一种代谢高度活跃的结构,为生长的胚胎提供营养。
越来越多的证据表明,倍性水平与细胞大小之间存在正相关关系(Kondorosi et al., 2000; Kudo and Kimura, 2002; Sugimoto-Shirasu et al., 2002)。因此,内复制可能是细胞生长的重要策略(Edgar and Orr-Weaver, 2001)。它也可能是特定细胞类型分化所必需的。例如,在拟南芥(Arabidopsis)中,毛状体(Trichome)的起始与内复制的开始密切相关(第9章; Hülskamp et al., 1994)。
正如Nagl(1978)所指出的,内周期可以被理解为一种进化策略。在整个物种中具有较低基本核DNA含量的门总是表现出内多倍性,而那些主要具有高DNA值的物种则缺乏内多倍性。正如Mizukami(2001)所提出的,“内复制可能已经作为一种发育手段进化,以在具有小基因组的物种中提供差异基因表达。”
在分化组织中最先可见的变化之一是细胞大小的不均等增加。一些细胞继续分裂,但大小增加不大,而另一些细胞停止分裂并显著增大(图5.8)。细胞大小差异生长的例子包括:原形成层细胞的伸长与相邻髓和皮层薄壁细胞缺乏类似伸长;根中初生韧皮部(最早形成的)筛管分子的伸长,与相邻的周缘细胞继续横向分裂形成对比(图5.8A);导管分子的加宽与周围细胞保持狭窄形成对比(图5.8E)。两个相邻细胞之间的大小差异也可能源于不对称或不等分裂,这些分裂产生具有不同命运的细胞(Gallagher and Smith, 1997; Scheres and Benfey, 1999)。例如,在花粉形成过程中,不对称细胞分裂产生一个较大的管细胞或营养细胞和一个较小的生殖细胞(Twell et al., 1998)。在一些植物中,根毛从原表皮细胞不对称分裂形成的两个姐妹细胞中较小的细胞发育而来(图5.8B, C;第9章)。不等分裂也发生在气孔的形成过程中(第9章;Larkin et al., 1997; Gallagher and Smith, 2000)。
细胞大小的增加可能沿所有直径相对均匀,但细胞经常在一个方向上比其他方向增大更多。这样的细胞可能与其分生组织前体在形状上显著不同(长的初生韧皮部纤维、分支的石细胞)。然而,许多细胞通过增加细胞面数但保留多面体形状以更温和的方式发生改变(Hulbary, 1944)。
组织中主要的细胞排列可能由其分生组织的生长形式决定(肋状分生组织、板状分生组织)。连续细胞行中壁的相对位置也赋予组织独特的外观(Sinnott, 1960)。与细胞行成直角的壁可能在相邻行中交替出现,或者可能出现在同一平面上。
图5.8
组织分化过程中的细胞间调整。A,烟草根尖的一系列细胞。薄壁细胞继续分裂;韧皮部细胞停止分裂并开始伸长。B, C,根毛从原表皮细胞横向分裂形成的两个姐妹细胞中较小的细胞发育而来。C,根毛细胞在与根成直角的方向上延伸,但不在根的伸长方向上延伸。显然,在根毛相邻的细胞中,壁部分$^a$和$c$继续伸长,而部分$^b$在根毛原基形成后停止伸长。D, E,形成层和由此类形成层发育的木质部,均为切向切面。E,展示了形成层衍生物发育变化的结果:此类衍生物的横向分裂形成薄壁细胞,导管分子横向扩展,纤维通过顶端侵入性生长伸长。
分化组织中的细胞间调节涉及协调和侵入性生长
分化组织中细胞的扩大和形状改变伴随着细胞间空间关系的或多或少深刻的变化。一个熟悉的现象是沿着三个或更多细胞结合线出现的细胞间隙(intercellular spaces)(第4章)。在某些组织中,细胞间隙的形成不会改变细胞的总体排列;而在其他组织中,它深刻地改变了组织的外观(Hulbary, 1944)。细胞骨架,特别是微管(microtubules)和纤维素微纤维(cellulose microfibrils)的定向在细胞形状形成中的作用将在第4章中讨论。
关于组织分化过程中细胞壁的生长,可以设想两种细胞间调节方式:(1) 属于两个相邻细胞的相邻生长壁层不分离,而是共同扩展;(2) 相邻壁层分离,生长细胞侵入由此产生的空间。第一种生长方式最初被称为共质生长(symplastic growth)(Priestley, 1930),在器官的初生生长过程中扩展时很常见。无论复合体中的所有细胞是否都在分裂,或者某些细胞已经停止分裂并在长度和宽度上增加,相邻细胞的壁似乎在没有分离或弯曲的情况下同步生长。在这种协调生长中,两个细胞之间的共同壁的一部分可能在扩展,而另一部分则没有。
涉及细胞侵入其他细胞之间的细胞间调节被称为侵入性生长(intrusive growth)(Sinnott和Bloch, 1939)或插入生长(interpositional growth)(Schoch-Bodmer, 1945)。这种生长的证据基于光学显微镜观察(Bailey, 1944; Bannan, 1956; Bannan和Whalley, 1950; Schoch-Bodmer和Huber, 1951, 1952)。它在延长的形成层初始细胞、维管组织中的初生和次生纤维、管胞(tracheids)、乳汁管(laticifers)和一些石细胞(sclereids)中很常见。侵入性生长可能异常强烈,如在某些木本百合科植物中,次生管胞比其分生组织对应物长15到40倍(Cheadle, 1937)。延长的细胞在其顶端生长(顶端侵入性生长(apical intrusive growth)),通常在两端。特定扩展基因表达在分化中的Zinnia木质部细胞末端的定位表明,扩展蛋白(expansins)可能参与了这些细胞初生细胞壁通过侵入性生长的延长(Im等, 2000)。延长的细胞侵入的细胞间物质可能在前进的尖端前水解,相邻细胞的初生壁以与细胞间隙形成期间相同的方式彼此分离(第4章)。
如果存在胞间连丝(plasmodesmata),它们可能会被生长细胞的侵入而破裂。报道的初生纹孔对(pit-pairs)成员的分离(Neeff, 1914)表明这种破裂的发生。纹孔对后来出现在通过侵入性生长接触的细胞对之间(Bannan, 1950; Bannan和Whalley, 1950)。这种纹孔对的特征是存在次生胞间连丝(secondary plasmodesmata)(第4章)。侵入性生长还与细胞的横向扩展有关,这些细胞获得了相当大的宽度,例如木质部中的导管分子(vessel elements)(第10章)。
早期的植物学家推测,滑动生长(gliding growth)发生在细胞侵入其他细胞之间的差异伸长或侧向扩张过程中。在滑动生长中,生长细胞的一部分壁被认为会分离并在相邻细胞的壁上滑动(Krabbe, 1886; Neeff, 1914)。这一概念后来被侵入生长(intrusive growth)所取代。这种局部细胞延伸是否涉及新壁部分在与旧壁接触时的滑动(Bannan, 1951),或者新壁是否沿着分离细胞的自由表面并置(插入生长; Schoch-Bodmer, 1945),目前仍不确定。
❙ 分化中的因果因素
关于分化和形态发生的研究包括对正常发育的植物和发育受到实验操作的植物的观察。实验处理的例子包括使用生长调节化学物质、外科手术、暴露于辐射、限制在受控温度和光照下、干扰正常重力效应以及在选定的日长条件下生长。已经收集了大量关于机械扰动对植物影响的证据。轻微的摩擦或弯曲茎会导致所有测试物种的长度生长明显延迟和径向生长增加。对机械干扰的反应被称为接触形态发生(thigmomorphogenesis)(Jaffe, 1980; Giridhar and Jaffe, 1988),thigm在希腊语中意为触摸。在自然界中,风显然是导致接触形态发生的最主要环境因素。分子遗传学方法在研究分化和形态发生中的应用,包括识别干扰感兴趣过程的突变,极大地促进了我们对调节植物发育各个方面因素的理解(Žárský and Cvrckova, 1999)。
组织培养技术对确定生长和分化需求非常有用
对完整植物和实验处理植物的研究清楚地表明,高等植物的有组织模式发育依赖于内部控制机制,其作用在一定程度上受到环境因素的影响(Steward et al., 1981)。
植物中模式分化(patterned differentiation)的需求对细胞的分生潜能(meristematic potentialities)施加了限制。当这种限制因从植物的有组织体中切除而中断时,活细胞能够恢复生长。在体外组织培养(tissue culture in vitro)的研究中,利用完整植物中控制机制的释放来探索有利于分生活动(meristematic activity)的条件,或者相反,诱导分化和形态发生(morphogenesis)(Gautheret, 1977; Street, 1977; Williams and Maheswaran, 1986; Vasil, 1991)。由于细胞在组织培养中对刺激的生长反应能力并不一定可预测(Halperin, 1969),许多组织培养研究涉及测试来自不同分类群和植物不同部位的外植体(explant)的分生潜能。这项研究的另一个目的是研究培养基的各种成分,特别是生长调节物质(growth-regulating substances)对外植体的影响。最初,植物组织培养主要用于专门的植物学研究。后来,该技术被广泛用于经济重要植物的繁殖、获得无病植物,以及培养细胞和组织作为药用和其他植物成分的来源(Murashige, 1979; Withers and Anderson, 1986; Jain et al., 1995; Ma et al., 2003)。对分离的*Zinnia*叶肉细胞(mesophyll cells)的培养研究为植物细胞分化和程序性细胞死亡(programmed cell death)提供了宝贵信息(第10章)。
在早期的组织培养工作中,胡萝卜根的次生韧皮部组织(secondary phloem tissue)是流行的实验材料(图5.9; Steward et al., 1964)。在含有椰子胚乳(coconut endosperm)的液体培养基中以解离状态培养时,外植体首先发育成随机增殖的愈伤组织(callus tissue),然后产生一种更有序的生长类型:具有中央木质部和木质部外韧皮部的结节(nodule)(Esau, 1965, p. 97)。结节最终产生根,然后在根的对面产生芽。由此产生的小植株呈现出年轻胡萝卜植物的形态,当转移到土壤中时,形成典型的直根(tap root)并开花。分离的胡萝卜细胞可以通过其他方式而不是通过愈伤组织进行形态发生(Jones, 1974)。通常,小的、液泡稀少的细胞从原始外植体中脱离,并呈现出胚状体(embryoid)的形态,这些胚状体在发育成植物时类似于合子胚(zygotic embryo)。从植物体细胞(somatic cells)启动和发育胚状体的过程称为体细胞胚胎发生(somatic embryogenesis)(Griga, 1999)。
技术的改进使得通过酶法去除单细胞的细胞壁来分离原生质体(protoplast)成为可能。这样的原生质体使得质膜(plasma membrane)
图5.9
从组织培养中的细胞发育成胡萝卜植物。培养的细胞来自胡萝卜直根的韧皮部。(经许可改编自F. C. Steward, M. O. Mapes, A. E. Kent, 和 R. D. Holsten. 1964. 培养植物细胞的生长和发育. Science 143, 20–27. © 1964 AAAS.)
膜可用于广泛的实验。分离的原生质体可以被诱导融合并产生体细胞杂种,这种技术对于植物育种方法成功率有限的植物尤其有价值,例如马铃薯植物 (Shepard et al., 1980)。分离的原生质体最终会再生细胞壁,并可能经历分裂并产生完整的植物 (Power and Cocking, 1971; Lörz et al., 1979)。如今,基因工程——重组DNA技术的应用——允许将单个基因以精确且简单的方式插入植物细胞中,无论是否去除细胞壁 (Slater et al., 2003; Peña, 2004; Poupin and Arce-Johnson, 2005; Vasil, 2005)。此外,参与基因转移的物种不必能够相互杂交。
许多细胞培养研究基于花药和花粉粒的使用 (Raghavan, 1976, 1986; Bárány et al., 2005; Chanana et al., 2005; Maraschin et al., 2005)。在适当的培养条件下,包裹在花药中的花粉粒可以产生胚状体,当花药打开时,这些胚状体被释放出来。对于分离的花粉培养,花药或整个花蕾在液体培养基中研磨,悬浮液经过过滤以分离花粉,然后在悬浮液或琼脂上进行培养。
在成功的培养中,花粉粒从正常的配子体发育转向营养孢子体发育,直接或通过愈伤组织生长形成胚状体 (Geier and Kohlenbach, 1973)。这个过程被称为雄核发育 (androgenesis)。常见的途径是通过营养细胞 (Sunderland and Dunwell, 1977; Street, 1977 第9章)。
由于花粉粒只含有一个基因组,因此可以获得单倍体植物。这些单倍体植物在植物育种中有许多用途,并且在突变研究中尤为重要。诱导的突变会立即在单倍体表型中表现出来,而在二倍体高等植物中,通常的隐性突变只有在诱变植物的后代中才会显现。
遗传嵌合体分析可以揭示发育植物中的细胞分裂和细胞命运模式
遗传嵌合体 (genetic mosaic) 一词指的是由不同基因型的细胞组成的植物。在开花植物中,遗传嵌合体,也称为嵌合体 (chimeras),出现在茎尖分生组织 (shoot apical meristem) 中 (图5.10) (Tilney-Bassett, 1986; Poethig, 1987; Szymkowiak and Sussex, 1996; Marcotrigiano, 1997, 2001)。在一些茎尖分生组织中,发现了整个平行的细胞层,这些细胞层在基因上彼此不同。这种嵌合体被称为周缘嵌合体 (periclinal chimeras)。在其他情况下,只有部分层(或几层)在基因上不同(部分周缘嵌合体,mericlinal chimeras);还有一些情况下,基因不同的细胞的清晰边界延伸穿过所有层(扇形嵌合体,sectorial chimeras)。这些差异可以作为标记,通过连续的细胞谱系追踪到茎尖分生组织细胞层中的类似差异。一些嵌合体具有二倍体和多倍体核的细胞层组合(细胞嵌合体,cytochimeras)。多倍化
图5.10
嵌合体茎尖。A,周缘嵌合体;B,部分周缘嵌合体;C,扇形嵌合体。右侧显示横切面;左侧显示由线指示的平面上的纵切面。
通过用秋水仙素(colchicine)处理茎尖(图5.11),可以诱导细胞核的多倍化。结果,顶端分生组织(apical meristem)中的某一层会被多倍体(polyploid)细胞核占据,这种变化会通过该层的后代细胞传递到分化中的植物体(Dermen, 1953)。在具有缺陷、无色质体(plastid)的突变体中,也可以发现周缘嵌合体(periclinal chimera)。与核嵌合体(nuclear chimera)一样,这种异常特征——在这里是有缺陷的质体——可以通过顶端分生组织到成熟组织的细胞谱系来追踪(Stewart et al., 1974)。花青素(anthocyanin)色素沉着是另一个常见的标记。
另一种类型的遗传嵌合体(genetic mosaic)是遗传上不同的细胞克隆(clone)散布在植物体中(图5.12)。这种克隆通常简称为遗传嵌合体,可以通过电离辐射(ionizing radiation)实验产生。由此产生的染色体重排(chromosomal rearrangement)使得隐性细胞自主突变(recessive cell-autonomous mutation)得以表型表达。来自这些细胞的细胞谱系或克隆被永久标记,对这些克隆的分析可以用来生成植物体任何区域细胞的命运图谱(fate map)。正如Poethig(1987)所指出的,他通过克隆分析研究了叶片发育(Poethig, 1984a; Poethig and Sussex, 1985; Poethig et al., 1986),然而,这种技术并不能替代植物发育的组织学研究。为了准确解释克隆模式,"必须对所研究系统的发育组织学和形态学有清晰的理解"(Poethig, 1987)。
基因技术极大地提高了我们对植物发育的理解
最终决定植物特征的是基因。DNA测序技术的进步使得对整个基因组进行测序成为可能,并催生了基因组学(genomics)这一新科学。基因组学涵盖了对整个基因组的内容、组织和功能的研究(Grotewold, 2004)。第一个被完整测序的植物基因组是拟南芥(Arabidopsis thaliana)(Arabidopsis Genome Initiative, 2000)。最近,水稻(Oryza sativa)基因组的高精度测序也已完成(International Rice Genome Sequencing Project, 2005)。
基因组学的一个广泛目标是识别基因,确定哪些基因被表达(以及在什么条件下),并确定它们的功能或其蛋白质产物的功能。如何确定一个基因的功能?一个非常成功的方法是揭示对植物发育有可见或表型影响的突变。已经筛选了大量经诱变剂处理的拟南芥植株,寻找此类突变。通过插入一段DNA片段使基因失活的突变体集合,可以用于研究基因功能。
图5.11
来自二倍体植物(左上)和几个周缘细胞嵌合体(periclinal cytochimeras)的*Datura*茎尖。染色体组合由每张图下方的数值表示。每组三个数值中的第一个数值代表第一层表皮原(tunica layer);第二个数值代表第二层表皮原;第三个数值代表原体层(corpus)的初始层。这三层通常被命名为L1、L2和L3。八倍体细胞最大,其细胞核用黑色表示以强调;四倍体细胞稍小,其细胞核用点状表示;二倍体细胞最小,其细胞核用圆圈表示。表皮原层的染色体特征仅在这些层及其衍生物中得以延续(表皮原中的垂周分裂);原体初始层的染色体特征会立即传递到其下方的层(不同平面的分裂)。(引自Satina等人,1940年。)
大片段DNA,如*Agrobacterium tumefaciens*的T-DNA,也被开发用于大量基因的研究(Bevan, 2002)。这些所谓的敲除突变体(knockout mutants),每个突变体都有一个不同的基因失活,然后通过筛选它们在特定环境中的表型变化或功能变化。任何被识别的变化都可以追溯到特定的突变序列。关于*Arabidopsis*,已经识别出负责胚胎发生(embryogenesis)主要事件的基因(Laux和Jürgens, 1994),负责茎尖分生组织(shoot apical meristem)形成和维持的基因(Bowman和Eshed, 2000; Doerner, 2000b; Haecker和Laux, 2001),以及控制花形成和花器官发育的基因(Theißen和Saedler, 1999)。
图5.12
在叶片开始形成之前,烟草(*Nicotiana tabacum*)叶片的表皮下层(subepidermal layer)中的克隆(clones)被照射($\mathbf{axis}=100\upmu\mathbf{m}$)。在这个阶段,克隆通常仅限于上表皮下层(黑色)或下表皮下层(灰色)。没有一个克隆从边缘延伸到中脉。(重绘自Poethig, 1984b。引自:*Pattern Formation*。Macmillan。© 1984。经McGraw-Hill Companies许可复制。)
在基因的初级作用与其最终表达之间有一系列的过程。基因对分化的初始影响的解释是在分子水平上进行的。它涉及基因激活和抑制、转录(从双链DNA螺旋的一条链的一部分合成信使RNA)和翻译(由mRNA的核苷酸序列指导的多肽合成)。多细胞生物中许多细胞类型之间的差异是选择性基因表达的结果——即只有某些基因被表达并转录成mRNA。因此,介导细胞分化的蛋白质被选择性地合成。在给定的细胞中,一些基因持续表达,另一些基因仅在需要其产物时表达,还有一些基因根本不表达。控制基因表达的机制——即“开启”和“关闭”基因——统称为基因调控(gene regulation)。
极性是生物模式形成的关键组成部分,并与梯度现象相关
极性(polarity)指的是空间中的活动方向。它是生物模式形成(biological pattern formation)的重要组成部分(Sachs, 1991)。极性在植物生命早期就显现出来。它表现在卵细胞中,细胞核位于合点端(chalazal end),而大液泡位于珠孔端(micropylar end),也表现在合子发育成胚胎的双极(bipolar)发育过程中。随后,极性表现在植物组织成根和茎的过程中,在细胞水平的各种现象中也很明显(Grebe et al., 2001)。移植研究(Gulline, 1960)和组织培养研究(Wetmore and Sorokin, 1955)表明,不仅整个植物表现出极性,其各个部分也表现出极性,即使这些部分与植物分离。茎的极性是一个常见的现象。例如,在用茎插条繁殖的植物中,根会在茎的下端形成,叶和芽会在上端形成。此外,通过将茎插条倒置种植,无法改变极性。
极性的稳定性在分化蕨类孢子(fern spores)的离心实验中得到了清晰的证明(Bassel and Miller, 1982)。在*Onoclea sensibilis*中,孢子的正常第一次分裂之前,细胞核从椭圆形孢子的中心迁移到其一端。随后发生高度不对称的分裂。大细胞形成原丝体(protonema),小细胞发育成假根(rhizoid)。孢子的离心作用不会改变这种分裂模式,即使孢子的内容物发生位移和分层。只有当离心作用发生在有丝分裂(mitosis)或胞质分裂(cytokinesis)之前或期间时,不对称分裂才会被阻止。
完整植物中单个细胞的极性行为通过不等分裂(unequal division)表现出来,这种分裂会产生生理上、通常也是形态上不同的子细胞(Gallagher and Smith, 1997)。在一些根的表皮(epidermis)中,发生不等分裂后,两个分裂产物中较小的一个形成根毛(root hair)。在分裂之前,富含细胞器的细胞质大部分积累在细胞的近端(proximal end)(朝向根尖的一端)或远端(distal end)。细胞核向同一方向迁移,然后分裂。细胞板(cell-plate)的形成将未来的小根毛细胞与不产生根毛的较长表皮细胞分开(Sinnott, 1960)。两种细胞之间的生化差异也变得明显(Avers and Grimm, 1959)。通常的假设是,不等分裂依赖于细胞质的极化(polarization),因为没有证据表明染色体物质(chromosomal material)的不等分布(Stebbins and Jain, 1960)。
极性(polarity)与梯度现象(gradients)相关,因为植物轴两极之间的差异以梯度系列的形式出现。存在生理梯度(physiological gradients),例如表现在代谢过程速率、生长素(auxins)浓度和传导系统中糖浓度的梯度;也存在解剖分化(anatomical differentiation)和外部特征发育的梯度(Prat, 1948, 1951)。植物轴在根和茎之间的过渡区域显示出过渡性的解剖学和组织学特征。分生组织(meristems)衍生细胞的分化通常以梯度系列的形式发生,相邻但不同的组织可能表现出不同的梯度。外部形态上,沿轴的连续叶片形态的变化显示出梯度发育,从通常较小且简单的幼态形式逐渐过渡到较大且更复杂的成体形式(图5.13)。随后,在诱导生殖状态后,逐渐产生较小的叶片,最终以支持花序(inflorescence)分支或单个花的花序苞片(inflorescence bracts)完成这一系列变化。
植物细胞根据位置分化
尽管细胞分化(cellular differentiation)依赖于基因表达的控制,但植物细胞的命运——即它将成为何种类型的细胞——是由其在发育器官中的最终位置决定的。即使建立了不同的细胞谱系(cell lineages),例如根中的细胞谱系,决定细胞命运的是位置而非谱系。多细胞生物中细胞的功能由其在该生物体中的位置早期决定的概念可以追溯到19世纪下半叶(Vöchting, 1878, p. 241)。然而,直到20世纪70年代初,嵌合体(chimeras)中偶尔观察到的细胞位移才提供了证据,表明茎和叶中的细胞命运是由位置而非谱系决定的,即使在发育的晚期阶段也是如此(Stewart and Burk, 1970)。此后,通过对遗传嵌合体(genetic mosaics)的分析,积累了确凿的证据,表明细胞的位置而非其克隆起源决定了其命运(Irish, 1991; Szymkowiak and Sussex, 1996; Kidner et al., 2000)。如果一个未分化的细胞从其原始位置位移,它将分化成适合其新位置的细胞类型,而不会对植物的组织结构产生任何影响(Tilney-Bassett, 1986)。对拟南芥(Arabidopsis)根尖的激光消融实验(van den Berg et al., 1995)也表明,消融的细胞可以被其他谱系的细胞替代,这些“替代细胞”根据其新位置进行分化。
图5.13
马铃薯(Solanum tuberosum)主茎上的前10片叶片。叶片经历了从单叶到羽状复叶的过渡。$(\times0.1$ 。引自McCauley and Evert, 1988。)
鉴于植物细胞的命运取决于它们在植物体内的位置,显然细胞之间必须能够相互通信,即交换位置信息。位置信息已被证明在玉米叶片光合作用细胞类型的分化(differentiation)中起作用(Langdale et al., 1989),在拟南芥叶片表皮毛(trichome)的间距中起作用(Larkin et al., 1996),并在维持拟南芥茎尖和根尖分生组织(apical meristem)细胞类型平衡中起作用(Scheres and Wolkenfelt, 1998; Fletcher and Meyerowitz, 2000; Irish and Jenik, 2001)。植物细胞间信号传导的机制基础仍有待阐明。植物中的一些信号传导过程似乎由跨膜受体样激酶(transmembrane receptor-like kinases)介导(Irish and Jenik, 2001);其他则利用胞间连丝(plasmodesmata)(第4章; Zambryski and Crawford, 2000)。
❙ 植物激素(PLANT HORMONES)
植物激素(phytohormones)是化学信号,在调节生长和发育中起主要作用,因此在此简要讨论(Davies, P. J., 2004; Taiz and Zeiger, 2002; Crozier et al., 2000; Weyers and Paterson, 2001)。激素(hormone)一词(来自希腊语horman,意思是启动)是从动物生理学中借用的。动物激素的基本特征——它们在远离其合成部位的地方起作用——并不完全适用于植物激素。虽然一些植物激素在一个组织中产生并运输到另一个组织,在那里产生特定的生理反应,但其他植物激素在产生它们的同一组织内起作用。在这两种情况下,它们都通过作为细胞之间的化学信使或信号来帮助协调生长和发育。
植物激素具有多种活性。一些激素不是作为刺激物,而是具有抑制作用。对特定激素的反应不仅取决于其化学结构,还取决于其靶组织如何"解读"它。一种给定的激素可以在不同的组织中或在同一组织的不同发育阶段引起不同的反应。一些植物激素能够影响另一种激素的生物合成或干扰另一种激素的信号转导。组织可能需要不同量的激素。这种差异被称为敏感性(sensitivity)的差异。因此,植物系统可以通过改变激素浓度或改变对已经存在的激素的敏感性来调节激素信号的强度。
传统上,植物激素的五大类受到了最多的关注:生长素(auxins)、细胞分裂素(cytokinins)、乙烯(ethylene)、脱落酸(abscisic acid)和赤霉素(gibberellins) (Kende and Zeevaart, 1997)。然而,越来越清楚的是,植物还使用了其他化学信号(Creelman and Mullet, 1997),包括油菜素内酯(brassinosteroids)——一类天然存在的多羟基类固醇,已在许多植物中被鉴定,并且似乎是大多数植物组织正常生长所必需的;水杨酸(salicylic acid)——一种结构与阿司匹林相似的酚类化合物,其产生与抗病性相关,并与过敏反应有关;茉莉酸类(jasmonates)——一类被称为氧脂素(oxylipins)的化合物——在种子萌发、根生长、贮藏蛋白积累和防御蛋白合成的调节中发挥作用;系统素(systemin)——一种18个氨基酸的多肽——由受伤细胞分泌,然后通过韧皮部运输到上部未受伤的叶片,以激活对食草动物的化学防御,这种现象称为系统获得性抗性(systemic acquired resistance) (Hammond-Kosack and Jones, 2000);多胺(polyamines)——低分子量、强碱性的分子——对生长和发育至关重要,并影响有丝分裂和减数分裂过程;以及气体一氧化氮(nitric oxide, NO),已被发现作为激素和防御反应中的信号。据报道,NO抑制拟南芥(Arabidopsis)的花期转变(He, Y., et al., 2004)。在它们的多种活动中,激素之间相互作用;实际上,生长物质之间的相互作用和平衡,而不是单一物质的活动,调节正常的生长和发育。
在接下来的段落中,将考虑传统植物激素类群的一些显著特征。
生长素(Auxins)
主要的天然生长素是吲哚-3-乙酸(indole-3-acetic acid, IAA)。IAA主要在叶原基和幼叶中合成,并涉及植物发育的许多方面,包括植物根-茎轴的整体极性,这是在胚胎发生期间建立的。这种结构极性可追溯到IAA在植物中的极性或单向运输。极性生长素运输通过特定膜结合流入(AUX1)和流出(PIN)载体的作用以细胞到细胞的方式进行(Steinmann et al., 1999; Friml et al., 2002; Marchant et al., 2002; Friml, 2003; Volger and Kuhlemeier, 2003)。从叶片向下到茎的生长素稳定流动导致生长素沿狭窄的细胞列流动,并导致连续维管组织束的形成(Aloni, 1995; Berleth and Mattsson, 2000; Berleth et al., 2000)——Sachs (1981)的管道化假说(canalization hypothesis)。
在茎和根中,极性运输(polar transport)始终是向基的(basipetal)——从茎尖和叶片向下运输到茎部,以及从根尖向根部基部(根-茎连接处)运输。极性生长素运输(auxin transport)的速度——每小时5到20厘米——比被动扩散(passive diffusion)的速度要快。除了生长素的极性运输外,最近还发现,成熟叶片中合成的大部分IAA显然是通过韧皮部以非极性的方式长距离运输到整个植物中,其速度远高于极性运输。在*Ricinus communis*的韧皮部(筛管)汁液中检测到相对较高浓度的游离IAA,表明生长素可能通过韧皮部长距离运输(Baker, 2000)。进一步的研究表明,在*Arabidopsis*中,生长素流入载体AUX1参与了叶片中的韧皮部装载(phloem loading)和根中的韧皮部卸载(phloem unloading)(Swarup et al., 2001; Marchant et al., 2002),这进一步支持了生长素在韧皮部中的运输。在具有次生生长的植物中,生长素运输也发生在维管形成层(vascular cambium)区域(Sundberg et al., 2000)。
在一项巧妙的研究中,Aloni及其同事(2003)结合分子和定位程序,展示了发育中的*Arabidopsis*叶片中游离生长素(IAA)产生的模式(图5.14)。托叶(stipules)是第一个主要的游离生长素高产部位。在发育中的叶片中,排水器(hydathodes)是游离生长素高产的主要部位,首先是叶尖的排水器,然后沿着边缘向基部推进。毛状体(trichomes)和叶肉细胞(mesophyll cells)是游离生长素产生的次要部位。在叶片发育过程中,游离生长素产生的部位和浓度从伸长的叶尖向扩展的边缘向基部转移,最后转移到叶片的中央区域。游离生长素产生部位和浓度的有序变化可能控制了叶片中脉序模式的形成和维管分化(vascular differentiation),排水器中生长素的大量产生诱导了中脉和次生维管束的分化,而叶片中——特别是与毛状体相关的区域——低游离生长素的产生诱导了三级和四级脉及脉端的分化。这项研究的结果与Aloni(2001)提出的叶脉假说(leaf-venation hypothesis)一致,该假说解释了真双子叶植物叶片中维管分化的激素控制。
一个名为VASCULAR HIGHWAY1 (VH1)的基因,其表达是原维管/原形成层细胞特异性的,已在*Arabidopsis*的发育叶片中被鉴定出来(Clay and Nelson, 2002)。VH1的表达模式与发育叶片中脉的形成模式相对应,并且正如Clay和Nelson(2002)所指出的,这与基于生长素产生和分布的模式化维管分化的管道化假说(canalization hypothesis)一致(Sachs, 1981)。
图5.14
在拟南芥(*Arabidopsis*)叶原基发育过程中,自由IAA(生长素)产生的位点(由点表示)和浓度(由点的大小表示)逐渐变化。IAA的初始产生发生在托叶(s)中(A)。箭头表示在叶片中,从分化的排水器(hydathodes)向下的基向极性IAA运动方向(B-D);箭头表示叶片中次级自由生长素产生位点的位置(D, E)。实验证据表明,尽管中脉向顶发育(B),但它是由基向极性IAA流诱导的。(引自Aloni, 2004, 图1。© 2004,经Springer Science and Business Media友好许可。)
实验证据还表明,极性生长素运输在水稻(*Oryza sativa*)叶片的维管模式中起作用(Scarpella et al., 2002)。有研究提出,水稻的*Oshox1*基因在原形成层细胞中表达(Scarpella et al., 2000),通过增加其生长素传导特性促进原形成层细胞的命运决定(Scarpella et al., 2002)。
生长素提供了协调植物体内多个发育过程的信号(Berleth and Sachs, 2001)。生长素被认为在调节细胞分裂、伸长和分化的模式中起作用(Chen, 2001; Ljung et al., 2001; Friml, 2003)。在拟南芥叶片中,高水平的IAA与高细胞分裂率密切相关。分裂的叶肉组织中的IAA水平是仅通过伸长生长的组织的十倍。尽管最年轻的叶片表现出最高的IAA合成能力,但拟南芥幼苗的其他部分(包括子叶、扩展中的叶片和根)也显示出从头合成IAA的能力(Ljung et al., 2001)。由极性运动引起的生长素梯度在胚胎发生(Hobbie et al., 2000; Berleth, 2001; Hamann, 2001)、叶片维管模式(Mattsson et al., 1999; Aloni et al., 2003)以及茎和根的侧器官形成(Reinhardt et al., 2000; Casimiro et al., 2001; Paquette and Benfey, 2001; Scarpella et al., 2002; Bhalerao et al., 2002)中提供了重要的发育信号。生长素被认为在向重性和向光性(Marchant et al., 1999; Rashotte et al., 2001; Muday, 2001; Parry et al., 2001)以及茎和根顶端分生组织的组织和维持(Sachs, 1993; Sabatini et al., 1999; Doerner, 2000a, b; Kerk et al., 2000)中起作用。与乙烯一起,生长素在拟南芥根毛的发育中起重要作用(Rahman et al., 2002)。生长素的其他一些活性包括作为顶端优势现象的一部分抑制腋芽发育以及延缓脱落。
细胞分裂素(Cytokinins)
细胞分裂素(cytokinins)之所以得名,是因为它们与生长素(auxin)共同作用,促进细胞分裂。根部是细胞分裂素的丰富来源,它们通过木质部从根部运输到茎部(Letham, 1994)。关于根部合成的细胞分裂素的调节功能之一,是触发侧芽从休眠状态中释放,与生长素的作用相反,后者抑制侧芽的生长。然而,通过转基因植物的实验结果表明,释放芽从休眠状态需要的是局部合成的细胞分裂素,而非根部来源的细胞分裂素(Schmülling, 2002)。根部来源的细胞分裂素更可能的作用是传递关于营养状态的信息,特别是氮营养,在根和茎之间(Sakakibara et al., 1998; Yong et al., 2000)。根冠(rootcap)中产生的细胞分裂素与拟南芥(Arabidopsis)根部对重力的早期反应有关(Aloni et al., 2004)。细胞分裂素在胚胎发生过程中原维管组织(provascular tissue)的形成(Mähönen et al., 2000)以及胚胎后发育过程中分生组织(meristem)活性和器官生长的控制中起着重要作用(Coenen and Lomax, 1997)。尽管它们是茎部发育的促进者,细胞分裂素却是根部发育的抑制剂(Werner et al., 2001)。
乙烯(Ethylene)
乙烯(ethylene),一种简单的碳氢化合物 $\left(\mathrm模板:H_{2}\mathrm模板:C{=}\mathrm模板:CH_{2}\right)$,几乎可以由种子植物的所有部分产生(Mattoo and Suttle, 1991)。作为一种气体,它通过扩散从其合成部位移动。乙烯的产生速率在植物组织之间有所不同,并取决于发育阶段。幼苗的茎尖是乙烯产生的重要部位,茎的节区域也是如此,它们产生的乙烯比节间多得多(在相同组织重量的基础上)。
乙烯的产生在叶片脱落和一些果实成熟期间增加。在鳄梨、番茄和苹果、梨等核果类果实的成熟过程中,细胞呼吸显著增加。这一阶段被称为呼吸跃变期(climacteric),这些果实被称为呼吸跃变型果实(climacteric fruits)。在呼吸跃变型果实中,乙烯合成的增加先于许多成熟过程,并对其负责。乙烯产生的增加也发生在大多数组织中,以响应生物(疾病、昆虫损害)和非生物(洪水、温度、干旱)胁迫(Lynch and Brown, 1997)。如前所述,溶生通气组织(lysigenous aerenchyma)的形成是乙烯介导的对洪水的响应(Grichko and Glick, 2001)。
乙烯的作用通常与生长素相反。生长素阻止叶片脱落,而乙烯促进叶片脱落。脱落区(abscission zone)中的乙烯产生受生长素调节。在大多数植物物种中,乙烯对细胞伸长有抑制作用(Abeles et al., 1992);而生长素促进细胞伸长。然而,在一些半水生植物(Ranunculus sceleratus, Callitriche platycarpa, Nymphoides peltata, 深水稻)中,乙烯引发茎的快速生长。
脱落酸(Abscisic Acid)
脱落酸(Abscisic Acid, ABA)这个化合物的名称其实是个误称。之所以这样命名,是因为最初人们认为它与脱落(abscission)有关,而现在已经知道脱落是由乙烯(ethylene)触发的。ABA几乎在所有含有淀粉体(amyloplast)或叶绿体(chloroplast)的细胞中合成,因此可以在从根尖到茎尖的活体组织中检测到(Milborrow, 1984)。ABA在木质部和韧皮部中都有运输,尽管在韧皮部中通常含量更高。根部响应水分胁迫合成的ABA通过木质部向上运输到叶片,在那里可以诱导气孔关闭(第9章;Davies和Zhang, 1991)。
在许多植物物种中,ABA水平在种子发育早期增加,刺激种子贮藏蛋白(seed storage proteins)的产生(Koornneef等, 1989)并防止过早萌发。许多种子的休眠打破与种子中ABA水平的下降有关。
赤霉素(Gibberellins)
赤霉素(Gibberellins, GAs)是四环二萜类化合物(tetracyclic diterpenoids)。已经鉴定出125多种GAs,但只有少数已知具有生物活性。发育中的种子和果实表现出最高的GA水平。豌豆幼苗中正在活跃生长的幼芽、叶片和上部节间已被确定为GA合成的部位(Coolbaugh, 1985; Sherriff等, 1994)。茎中合成的GAs可以通过韧皮部运输到整个植株。
GAs通过刺激细胞分裂和细胞伸长对茎和叶的伸长有显著影响。它们在茎生长中的作用在应用于许多矮化植物时最为明显。在GA处理下,这些植物与正常的非突变植物无法区分,表明突变体无法合成GA,而生长需要GA。拟南芥gal-3矮化突变体(Zeevaart和Talon, 1992)说明了GA缺乏的多重影响。除了矮化外,这些植物更浓密,叶片颜色更深。此外,gal-3开花延迟,gal-3花雄性不育,gal-3种子无法萌发。添加GA后,突变体的所有野生型特征都得以恢复。对烟草和豌豆的研究表明,茎中正常的$\mathbf{GA}_{1}$生物合成需要来自顶芽的IAA(Ross等, 2002)。$\mathbf{GA}_{1}$可能是控制茎伸长的唯一GA。$\mathbf{GA}_{1}$诱导的伸长通常伴随着IAA含量的增加。
GAs控制着广泛的植物发育过程(Richards等, 2001)。它们对豌豆的正常根伸长(Yaxley等, 2001)、种子发育和拟南芥的花粉管生长(Singh等, 2002)很重要,并且对许多植物物种的种子萌发至关重要(Yamaguchi和Kamiya, 2002)。在许多种子植物中,GAs可以替代种子萌发所需的打破休眠的低温或光照。如前所述,在谷物中,GAs调节酶($\upalpha$-淀粉酶)的产生和分泌,导致胚乳中储存的淀粉水解。GAs也可能作为长日照开花信号(King等, 2001)。对长日照植物和二年生植物施用GAs可能会导致抽薹和开花,而无需适当的低温或长日照暴露。第一章 植物体的结构和发育——概览
